Решите ситуационную задачу.
При качественном анализе бесцветного раствора получены следующие результаты аналитических проб:
1. При действии соляной кислоты – выпал белый осадок, растворимый в горячей воде.
2. При действии серной кислоты - выпал белый осадок.
3. При действии K2CrO4 – выпал желтый осадок.
Какой катион находится в исследуемом растворе? Приведите ваши рассуждения и составьте молекулярные и ионные уравнения происходящих реакций.
Решение: В исследуемом растворе находится катион 2 аналитической группы, так как при действии группового реактива HCI выпал белый осадок, растворимый в горячей воде. Согласно результатам анализа 2 пробы, при действии серной кислоты выпал белый осадок. При действии K2CrO4 выпал желтый осадок (проба 3). В испытуемом растворе присутствует катион свинца.
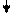 Проба 1: Pb(NO3)2 + 2 HCI = PbCI2 + 2 HNO3
Проба 1: Pb(NO3)2 + 2 HCI = PbCI2 + 2 HNO3
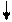
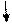 Pb 2+ + 2 NO3- + 2 H+ + 2CI - = PbCI2 + 2 H+ + 2NO3- Pb 2+ + 2CI - = PbCI2
Pb 2+ + 2 NO3- + 2 H+ + 2CI - = PbCI2 + 2 H+ + 2NO3- Pb 2+ + 2CI - = PbCI2
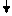 Проба 2: Pb(NO3)2 + H2SO4 = PbSO4 + 2 HNO3
Проба 2: Pb(NO3)2 + H2SO4 = PbSO4 + 2 HNO3
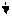 Pb 2+ + 2NO3 - + 2H+ + SO42- = PbSO4 + 2 H + + 2NO3-
Pb 2+ + 2NO3 - + 2H+ + SO42- = PbSO4 + 2 H + + 2NO3-
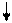 Pb 2+ + SO42- = PbSO4
Pb 2+ + SO42- = PbSO4
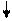
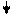 Проба 3: Pb(NO3)2 + K2CrO4 = Pb CrO4 + 2KNO3
Проба 3: Pb(NO3)2 + K2CrO4 = Pb CrO4 + 2KNO3
Pb2+ + 2NO3 - + 2K+ + CrO42- = Pb CrO4 + 2K + + 2 NO3-
 Pb2+ + CrO42- = Pb CrO4
Pb2+ + CrO42- = Pb CrO4
 2015-08-12
2015-08-12 1860
1860








