К анализируемому раствору добавили соляную кислоту, в результате чего выпал белый осадок.
На присутствие каких катионов это указывает?
Как разделить находяшиеся в осадке катионы?
Приведите ваши рассуждения и составьте молекулярные и ионные уравнения происходящих реакций.
Решение: В исследуемом растворе находятся катионы 2 аналитической группы, так как при действии группового реактива HCI выпал белый осадок. Если осадок не растворяется в горячей воде, но растворется в аммиаке, то это катион Ag+. Если осадок растворяется в горячей воде, то это катион свинца.
Если в растворе находятся катионы серебра и свинца, то к полученным осадкам необходимо прилить горячую воду. Хлорид свинца растворится в горячей воде, а хлорид серебра останется в виде осадка.
 AgNO3 + HCI = AgCI + HNO3
AgNO3 + HCI = AgCI + HNO3
 Ag+ + NO3- + H + + CI- = AgCI + H+ + NO3-
Ag+ + NO3- + H + + CI- = AgCI + H+ + NO3-
 Ag+ + CI- = AgCI
Ag+ + CI- = AgCI
AgCI + 2NH3 = [Ag(NH3)2]CI
 [Ag(NH3)2]CI + 2HNO3 = AgCI + 2 NH4NO3
[Ag(NH3)2]CI + 2HNO3 = AgCI + 2 NH4NO3
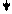 [Ag(NH3)2]+ + CI- + 2 H+ + 2NO3 - = AgCI + 2NH4+ + 2NO3-
[Ag(NH3)2]+ + CI- + 2 H+ + 2NO3 - = AgCI + 2NH4+ + 2NO3-
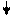 [Ag(NH3)2] + + CI- + 2H + = AgCI + 2 NH4 +
[Ag(NH3)2] + + CI- + 2H + = AgCI + 2 NH4 +
Pb(NO3)2 + 2 HCI = PbCI2 + 2 HNO3
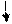 Pb 2+ + 2 NO3- + 2H+ + 2CI - = PbCI2 + 2 H+ + 2NO3-
Pb 2+ + 2 NO3- + 2H+ + 2CI - = PbCI2 + 2 H+ + 2NO3-
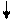 Pb 2+ + 2CI - = PbCI2
Pb 2+ + 2CI - = PbCI2
 2015-08-12
2015-08-12 1364
1364








