Термическое разложение тригидрата уранилоксалата на воздухе при температуре выше 500 °С приводит к образованию закиси-окиси урана:
3UO2C2O4 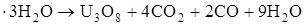 (9.10)
(9.10)
При прокаливании без доступа воздуха возможно получение диоксида урана:
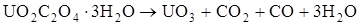 (9.11)
(9.11)
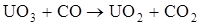 (9.12)
(9.12)
Из реакций (9.11) и (9.12) следует, что восстановитель (СО) получается только в стехиометрических количествах. При проведении процесса разложения в атмосфере аргона при температурах 400—900 °С в газовой фазе содержание С02 составляло 52—57 %, а СО — 5-10 %. Из этих данных следует, что скорость разложения уранилоксалата выше скорости восстановления триоксида урана оксидом углерода.
Следовательно, получить диоксид урана из уранилоксалата в статических условиях невозможно. Для получения диоксида необходим непрерывный процесс, причем в аппарате должны быть две температурные зоны: зона разложения и зона восстановления с циркуляцией газовой фазы в зоне восстановления после удаления влаги, для уменьшения продолжительности процесса необходимо увеличивать температуру в зоне восстановления (620—900 °С), желательно также добавление водорода.
Образующийся в результате термического разложения уранилоксалата диоксид урана обладает высокой реакционной способностью, при обычных условиях он пирофорен, необходима его защита от воздуха. Лучше всего это достигается путем совмещения процессов прокаливания, восстановления и гидрофторирования, когда полученный диоксид урана обрабатывают фтористым водородом с получением гетрафторида урана.
 2015-08-13
2015-08-13 702
702








