Вопросы белок-липидных взаимодействий давно привлекают внимание исследователей» так как in vivo большинство ферментативных реакций протекает вблизи или на поверхности биомембран. Поэтому иммобилизация ферментов на природных лк-пидных носителях (конструирование ансамблей белок-липид) может рассматриваться как наиболее близкое приближение к условиям функционирования ферментативных систем в живой клетке.
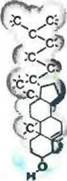
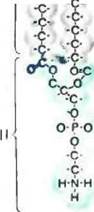
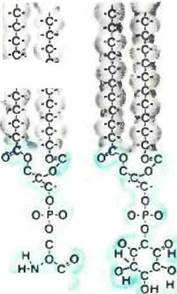
Для пел ей такой иммобилизации» как правило, используются природные лнпиды — компоненты бномембран. Структуры наиболее распространенных природных лнпидов изображены на рис. I,
Обычно лнпндные носители применяются в виде монослоев на различных поверхностях или бислоев (как правило, сферической формы).
Монослои лнпидов на поверхности воды. Лнпиды, имеющие в своем составе хотя бы небольшую полярную «голову», способны образовывать мономолекуляркые пленки на границе раздела фаз (вода и воздух или вода и неполярный растворитель). Липидные молекулы в монослое расположены таким образом, что их полярные головные группы погружены в водную фазу, а углеводородные части направлены в воздух или погружены в органический растворитель. Такая пленка способна сорбировать белковые молекулы. Изучение монослоев лнпидов, содержащих белок, помогает понять природу взаимодействия лнпидов и белков в биологической мембране (сорбцию белка на липиднон поверхности, электростатические и гидрофобные
 |
 |
| it •?■• |
| -этанопамин |
 и
и
ир* *?
'#.1
6 О-РО
О с
| н о |
н Ч(?"н н * н
Фосфатвдил -
- серии - инозит - холин (лецитии)
' "
г» '
О
0 0 б'С
V
-ее 0-РО
-i-'V У
<®ж,
о
' 0-Р-О h
ф
-с-
(HCW - -С^| Сфингом+*елнк
■*.«*
j -С-' /
И А-
он " Ц^реброэид
Рис. L Основные типы мембранных -1ипидов;
о — глицеродипнды; б — сфинголипнды; в — холестерин; черточки — атомы водорода; полуокружности -объемы, занимаемые негтолярнымн хвостам и (/| у полярными головами лнпнлов (/Л
взаимодействия этих соединений, влияние поверхности на кон-формацию белка).
Получение мои о ело ев липидов на поверхности воды требует специальной техники и является весьма трудоемкой процедурой, что ограничивает их применение.
Монослои лип и да на твердой поверхности. Эти системы в качестее носителей были предложены О. М, Полтораком и Е. С- Чухрай (1966). Суть метода состоит в нанесении л и тш дно го монослоя на твердую подложку (сил ик а гель, сажа, аэроснл) с последующей адсорбцией белка из водно то раствора. В качестве л и пн д нон матрицы используют обычно лецитин, фосфатидил-этаноламин и холестерин. Разработан также метод получения искусственных смешанных лецитин-холестериновых слоев.
Возможность варьировать структуру и ориентацию молекул в лнпидных слоях достигается подбором полярности носителя и природы используемого растворителя ли пи да. Если липид с молекулами дифкльной природы, растворенный в неполярном органическом растворителе (бензол» гептан), адсорбировать на полярном силикагеле, то в монослое лнпида углеводородные цепи будут ориентированы наружу. При адсорбции лнпида из полярного растворителя на неполярной графитовой саже можно получить гидрофильный монослой, в котором полярные головные группы ориентированы в сторону растворителя.
Лилосомы. Впервые лнпосомы были описаны А. Бэнгэмом в 1964 г. Для их приготовления наиболее часто используются фосфятидилхолипы (лецитины), фосфатидилэтаноламин, фосфат-ндилсерин, кардиолипин, сфингомиелин, причем они образуются как из чистых лип идо и, так и смесей.
Существует три различных типа липосом: мультиламелляр-ные, моноламеллярные и макровезикулярные. Мультиламелляр-ные лнпосомы представляют собой замкнутые упорядоченные структуры, состоящие из нескольких концентрических липндных бислоев, отделенных один от другого водной средой. Расстояние между соседними лнпнднымн бнслпями равно 7,5 нм, диаметр центрального водного ядра равен приблизительно 0,15 мкмт а* суммарный диаметр мультиламеллярных лнпосом колеблется» от 1—2 до 50 мкм.
Ультразвуковая обработка мультиламеллярных липосом приводит к трансформации их в простые, или моноламеллярные. При такой обработке размеры частиц уменьшаются; диаметр моноламеллярных липосом составляет от 20,0 до 50,0 нм.
Третий тип лнпосом - макровезикулярные липосомы, образующиеся, например, путем слияния малых липосом, индуцируемого ионами Са2+, а также присутствием фосфолипидов с отрицательно заряженными головными группами. Такие липосомы состоят из одного бнслоя и могут иметь диаметр от 60,0 нм до 100 мкм.
Размер и форма лнпосом зависят от способа их приготовления, а также от таких факторов, как кислотность среды, при-
сутствие неорганических солей и природы используемого липида. Широкое применение липосом как носителей для ферментов и лекарственных препаратов обусловлено простотой получения, легкостью регенерации иммобилизованного материала, а также возможностью использования in vivo благодаря близости свойств этих липидов носителей и природных биомембран.
$ 6. Синтетические аналоги липидов (поверхностно-активные вещества)
Поверхностно-активные вещества (ПАВ) состоят из молекул дифилыгой природы» имеющих в своем составе как полярную головную группу, так и неполярную углеводородную часты В принципе уже рассмотренные природные лнпнды также относятся к ПАВ. Синтетические ПАВ — это соединения, многие из которых являются продуктами крупнотоннажного производства.
В зависимости от того, какие группы присутствуют в головной части молекулы, все ПАВ можно разделить на четыре основных типа: анионные, катионцые, неиоцкые и цвиттерионные. В качестве примеров можно назвать следующие:
О О
II II
НЭС— (Н2С)з—СН^СН*—О—С—СН—СНг—С—
I Л,.* '
SO3 Na
—О—СНг—СН— {СН 2) з—СНз
I Н2С—СН3
бно-2-этнл гене иловый афнр натриевой соли сульфоянтзрной кислоты — анионное ПАВ
СН3 I НзС-bN—(СН2) is—СНэВг"
СНз
цегилтрниетнламмоннйбромнд — катнониое ПАВ
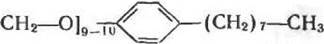 |
НО—[СНг
полы (9—10) окснэтнлена октютфснилоцый эфир <трнтон X-10Q — иеионнм
йлкилдниетилкарбонснб*танн — цвнттерномное ПАВ,
где п = 10—18,
Приведенные примеры не исчерпывают всего многообразия промышленных ПАВ. Так, например, фирмой «Serva» выпускается более 30 наименований только неионных ПАВ различного
 |
| Таблица 5. Немонные ЛАВ,•спускаемые фирмой cServa» Типы структур ПАВ |
| HD—(Et—О]^^—----- ~ (простые эфиры полнокснэтилена) НО—f Et—О) й-СО-------------- (сложные эфнры полиокснэтнлена) —О—[ Et—О] й- |
| /Ня~Т хн—cw |
| ион снон сн3—о—со- (окснзтнлнрованнш1 эфнры ангнд-росорбнта и жирных кислот) |
| НО—tEt—О]й (полиоксиэтилсиалкилфениловыс эфиры) |
| п | Углеводородный Название | |
| фрагмент | ||
| Гексадецил | Бридж 52 | |
| Долепил | Бридж 30 | |
| Гексадецил | Бридж 56 | |
| Гексадецнл | Бридж 58 | |
| Додецнл | Бридж 35 | |
| Стеаронл | т Мирдж 45 | |
| Стеароил | Мирдж 32 | |
| Стеаронл | Мирдж 59 | |
| Трнолеонл | Спаи 85 | |
| Триетеа роил | Спаи 65 | |
| Олеонл | Спан 60 | |
| Стеароил | Слан 60 | |
| Пальмнтоил | Спаи 40 | |
| Лауройл | Спаи 20 | |
| Стеаронл | Тайн 61 | |
| Трнстеароил | Твин 65 | |
| Триолеоил | Твин 85 | |
| Стеароил | Твии 60 | |
| Олеоил | Твии 80 | |
| Пальмитоил | Твин 40 | |
| Лауроил | Твин 20 | |
| Октил | Тритон Х-15 | |
| Октил | Тритон Х-35 | |
| Нокил | Тритон N-57 | |
| Октил | Тритон Х-45 | |
| а-9 | Октил | Тритои Х-П4 |
| 9—10 | Октил | Тритои Х-100 |
| 12—13 | Октнл | Тритон Х-102 |
| Октнл | Тритои Х-165 | |
| Окгил | Тритон Х-305 | |
| Октил | Тритои Х-405 |
строения (табл. Ь). Список промышленных ПАВ с обсуждением их свойств можно найти в справочнике «Поверхностные явления и поверхностно-активные вещества» {под ред. А, А. Абрам-зона и Е. Д. Щукина, 1984).
Рассмотрим некоторые примеры использования ПАВ в качестве носителей для ферментов.
Обращенные мицеллы ПАВ в органических растворителях. Оки представляют собой ассоциаты, в которых полярные головные группы молекул ПАВ образуют ядро мицеллы, а углеводородные остатки этих молекул направлены в органический растворитель. В полярную внутреннюю полость обращенной мицеллы может быть включено (солюбилнзовано) значительное количество воды (до нескольких десятков молекул воды на каждую молекулу ПАВ) и других полярных веществ. Размеры внутренней полости обращенных мицелл можно целенаправленно
 2015-08-13
2015-08-13 835
835








