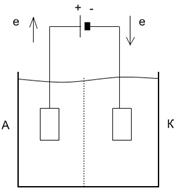
15. Приведите схему электролизера с электролитом - водным раствором какой - либо соли. Укажите анод, катод, направление движения электронов в проводниках первого рода и направление движения ионов в проводнике второго рода. Укажите материал электродов. Укажите состав продуктов в анодном и в катодном пространствах в случае электролиза водного раствора поваренной соли.
Ответы. При электролизе водного раствора поваренной соли
на аноде протекает электродная полуреакция окисления: 2CI-(в) – 2е = CI2(г)
на катоде протекает электродная полуреакция восстановления: Н2О(ж) + 2е = Н2(г) + 2ОН-(в)
16. Законы электролиза Фарадея.
Пусть на электроде протекает полуреакция
Х ± nе = Y (знак + для катода, знак – для анода) (1)
1 - й закон Фарадея:
m (Y) = k (Y) · I · t
где m (Y) – масса вещества Y, выделившегося на электроде при протекании через него тока силой I А в течение времени t с
2 - й закон Фарадея:
k (Y) = М (Y)/ nF
где k (Y) - электрохимический эквивалент вещества Y,
М (Y) – молекулярная масса вещества Y, кг/моль,
n – безразмерная величина, определяемая из уравнения (1) электродной полуреакции,
F - постоянная Фарадея: F = е · N А = 96500 Кл/моль,
Справка: е = 1.602 · 10-19 Кл, 1 Кл = 1 А · 1 с, 1 Вт = 1 А · 1 В, 1 Вт = 1 Дж/1 с
17. Электрохимические методы очистки сточных вод: 1) анодное окисление и катодное восстановление анионов и катионов вредных веществ (приведите примеры), 2) электрокоагуляция, 3) электродиализ, 4) электрофлотация.
Примеры окисления и восстановления на аноде и на катоде:
анодное окисление цианид-иона: 2 СN- + 8 OH- - 10e = 2 CO2 + N2 + 4 H2O
катодное восстановление дихромат-иона: Cr2O72- + 14 H+ + 12e = 2 Cr + 7 H2O.
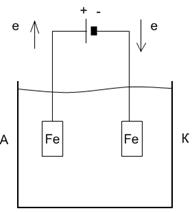
18. Электрокоагуляция. Очистка сточной воды с использованием метода электрокоагуляции основана на электрохимическом растворении железного анода с последующим образованием объемного студенистого осадка гидроксида железа(III) при участии растворенного в воде кислорода. Нарисуйте схему электролизера. Составьте уравнения полуреакций, протекающих на аноде и на катоде, считая, что на катоде происходит восстановление воды. Какова роль растворенного в воде кислорода? От какого вида примесей очищается вода методом электрокоагуляции?
На аноде: Fe(т) – 2e = Fe2+(в)
На катоде: 2Н2О(ж) + 2е = Н2(г) + 2ОН-(в)
При смешивании анодного и катодного растворов образуется объемный студенистый осадок Fe(OH)2, который захватывает коллоидные и другие примеси, содержащиеся в воде. Осадок Fe(OH)2 затем доокисляется содержащимся в воде кислородом до еще менее растворимого Fe(OH)3. Осадок Fe(OH)3 вместе с осажденными и адсорбированными на нем дисперсными и молекулярными примесями затем отделяют от воды в отстойнике. Процесс периодического действия.
19. Электродиализатор – это электролизер, межэлектродное пространство которого разделено на несколько (нечетное число) камер с помощью попеременно расположенных катионо - и анионообменных пористых мембран. Поскольку катионообменные мембраны пропускают через поры только катионы, а анионообменные – только анионы, то камеры поочередно обедняются и обогащаются электролитами. В результате исходный раствор электролита делится на два потока – обессоленный и концентрированный. Электродиализ с использованием селективных мембран применяется для очистки сточных вод от ионных примесей.
Приведите схему электродиализатора, используемого для обессоливания воды. Почему катионообменная мембрана не пропускает анионы в направлении к аноду? Почему анионообменная мембрана не пропускает катионы в направлении к катоду? Приведите поясняющую схему ионообменной мембраны.
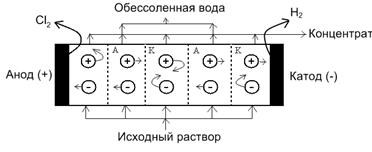
Схема электродиализатора. Пунктиром изображены последовательно слева направо анионо (А) и катионообменные (К) мембраны.
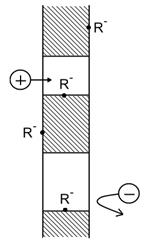
Схема катионообменной мембраны, на стенках которой расположены анионоактивные группы.
Составьте уравнения полуреакций, протекающих на аноде и на катоде электродиализатора в случае, когда исходная вода содержит только хлорид натрия.
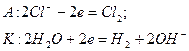
 2015-08-13
2015-08-13 802
802