У молекулярно-кінетичній теорії (МКТ), як звичайно, користуються ідеалізованою моделлю газу – ідеальним газом. Газ уважатимемо ідеальним, якщо: а) власним об’ємом його молекул можна знехтувати, тобто вважати молекули матеріальними точками; б) сили взаємодії між молекулами газу на відстані не діють, молекули абсолютно пружно взаємодіють лише під час зіткнень.
 Стан ідеального газу заданої маси описують трьома параметрами: р – тиск, V – об’єм і Т – абсолютна температура (Т =273, 15 + t °C). За умови зміни параметрів газу говорять про процес переходу газу з одного стану в інший. Ще до створення МКТ експеримен-тально були виведені три газові закони для ізотермічного, ізобарного та ізохорного процесів.
Стан ідеального газу заданої маси описують трьома параметрами: р – тиск, V – об’єм і Т – абсолютна температура (Т =273, 15 + t °C). За умови зміни параметрів газу говорять про процес переходу газу з одного стану в інший. Ще до створення МКТ експеримен-тально були виведені три газові закони для ізотермічного, ізобарного та ізохорного процесів.
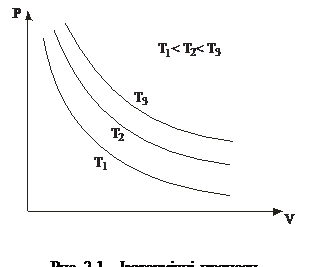
1. Ізотермічний процес – це процес, який відбувається з газом за сталої температури. Його описує закон Бойля–Маріотта: для заданої маси газу за сталої температури добуток тиску газу на його об’єм є сталою величиною:
pV =const, (T = const, m = const). (2.1)
У координатах pV графік процесу показаний гіперболою (рис. 2.1).
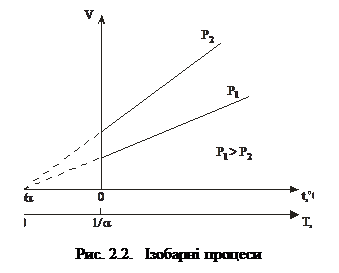 2. Ізобарний процес – це процес, який відбувається з газом за сталого тиску. Його описує закон Гей–Люссака: об’єм заданої маси газу за сталого тиску залежить від температури лінійно:
2. Ізобарний процес – це процес, який відбувається з газом за сталого тиску. Його описує закон Гей–Люссака: об’єм заданої маси газу за сталого тиску залежить від температури лінійно:
V = V 0(1+a t °C), (2.2)
(р =const, m =const). (2.2)
Тут коефіцієнт a=1/273,15 К-1, V 0 – об’єм газу за температури t =0оС. Якщо у (2.2) ввести абсолютну температуру Т, то рівняння ізобарного процесу набуде вигляду
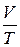 =const. (2.3)
=const. (2.3)
Графіки процесів у координатах V t і VT зображені на рис. 2.2.
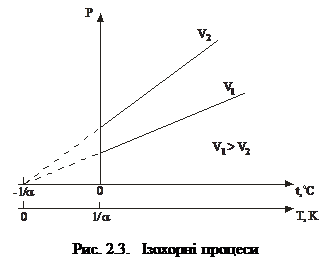 3. Ізохорний процес – це процес, який відбувається з газом за сталого об’єму. Його описує закон Шарля: тиск заданої маси газу за сталого об’єму залежить від температури лінійно:
3. Ізохорний процес – це процес, який відбувається з газом за сталого об’єму. Його описує закон Шарля: тиск заданої маси газу за сталого об’єму залежить від температури лінійно:
р = р 0(1+a t °C), (2.4)
(V = const, m = const), (2.4)
або 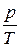 =const (2.5)
=const (2.5)
Графіки ізохорних процесів пока-зані на рис. 2.3.
У загальному випадку незалежно від процесів, які відбуваються з ідеальним газом, його стан описує рівняння Клайперона–Менделєєва:
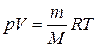 , (2.6)
, (2.6)
де m – маса газу; М – його молярна маса, R – універсальна газова стала. Рівняння (2.6) можна вивести, розглянувши два процеси переходу газу зі стану з параметрами p 1, V 1, T 1 у стан p 2, V 2, T 2 через проміжний стан p 2, 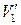 , T 1 та скориставшись рівняннями (2.3), (2.5), (2.6).
, T 1 та скориставшись рівняннями (2.3), (2.5), (2.6).
Рівняння стану ідеального газу можна записати в іншій формі, врахувавши, що m = N × m 0, де N – кількість молекул газу; m 0 – маса молекули; молярна маса M = N A× m 0, а R = k × N A. Підставимо ці співвідношення у (2.6) і отримаємо:
p=nkT, (2.7)
де n = N / V – концентрація молекул газу.
Отже, за сталої температури тиск газу прямопропорційний до концентрації його молекул.
 2015-08-21
2015-08-21 1431
1431








