Если в электрохимической цепи протекает электрический ток, то она находится в неравновесном состоянии. В цепи идет электрохимическая реакция с конечной скоростью в одном определенном направлении. В неравновесных условиях свойства электрохимических систем отличаются от свойств соответствующих равновесных систем. Отличия заключаются в следующем.
- Скорость электрохимической реакции в анодном и катодном направлениях не одинакова.
- Масса электродов и состав растворов вблизи них изменяются по сравнению с состоянием равновесия.
- Потенциал электрода φ под током не равен равновесному электродному потенциалу, а поэтому и значение напряжения отличается от обратимого значения ЭДС. Величины φ и Е зависят не только от природы системы, ее температуры и давления, но и от силы тока. Таким образом, для неравновесной электрохимической цепи должна существовать определенная связь между силой тока и значением ЭДС.
Изменение массы электродов и состава растворов вблизи них под действием электрического тока свидетельствует о наличии химических превращений. Следовательно, должна существовать определенная зависимость между количеством электричества и массой прореагировавших веществ. Эта зависимость выражается законами Фарадея (1833—1834).
Первый закон: количество (т) вещества, выделяющееся при электролизе на электроде, прямо пропорционально количеству электричества, прошедшего через электролит (q):
m=k Э q (13)
где k Э — электрохимический эквивалент, который равен массе превращенного вещества при протекании единицы количества электричества (г/Кл). Его физический смысл можно установить, если принять q=1 Кл. Тогда m = k, т.е. коэффициент k представляет собой количество вещества (г), выделяемого на электроде при пропускании 1 Кл электричества.
Второй закон: при прохождении через различные электролиты одного и того же количества электричества массы различных веществ, участвующих в электродных реакциях, пропорциональны их химическим эквивалентам Э ;
m1:m2:m3 = Э1:Э2:Э3 (14)
Количество электричества в кулонах (Кл) равно произведению силы тока (в амперах) на время (в секундах):
q = I τ
Подставив значение q в уравнение (13), получаем:
m = k I τ (15)
Для выделения 1 г-экв любого вещества (Э) требуется пропустить через электролит одно и то же количество электричества, равное приблизительно 96 500 Кл. Из пропорции Э: 96 500 = k: 1 можно определить величину электрохимического эквивалента:
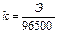
Подставив значение kв выражение (15), получим объединенную формулу двух законов Фарадея:
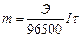
Количество вещества, выделившегося на электродах при электролизе, прямо пропорционально количеству прошедшего электричества и химическому эквиваленту данного вещества .
Из второго закона следует, что для электрохимического превращения одной молярной массы эквивалента (моль) любого вещества требуется одинаковое количество электричества. Это количество электричества равно числу F,называемому постоянной Фарадея: F= 96485 (≈96500) Кл/моль.
Законы Фарадея являются общими и точными законами электрохимии. Однако в большинстве случаев электрохимическому изменению подвергается меньшая масса данного вещества по сравнению с тем, которое можно ожидать по закону Фарадея. Такое кажущееся отступление от законов Фарадея объясняется тем, что превращению подвергается не одно вещество, а несколько веществ. Поэтому на данное вещество приходится доля эквивалента.
Чтобы учесть влияние побочных реакций, было введено понятие выхода по току АI. Выход по току — это часть протекшего количества электричества, приходящаяся на долю данной электрохимической реакции:
A I = 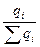 , или в % A I =
, или в % A I = 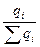 100 (16)
100 (16)
где qi— количество электричества, расходуемое на данную реакцию; ∑qi— общее количество прошедшего электричества.
Если из нескольких возможных процессов желателен только один, то выход по току должен быть высоким. Системы, в которых весь ток расходуется только на одну электрохимическую реакцию, используются в приборах — кулонометрах, применяемых для измерения количества прошедшего электричества.
 2015-08-21
2015-08-21 2729
2729
