Рассмотрим систему, в которой не один, а два каких-нибудь металла, например цинк и медь, в виде пластинок опущены в растворы своих солей, разделенные диафрагмой. Каждый из металлов может выделить в раствор то количество ионов, которое отвечает равновесию его с раствором. Однако отвечающие такому равновесию потенциалы этих металлов неодинаковы. Цинк обладает более высокой способностью выделять ионы в раствор, чем медь, и поэтому приобретает более высокий отрицательный заряд.
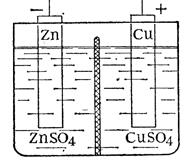
Рис.1. Схема гальванического
элемента.
Если пластинки соединить проволокой, то разница этих потенциалов пластинок и образование контактной разности потенциалов металлов Zn/Cu приводит к переходу соответствующего числа электронов с цинковой пластинки на медную. Это нарушает равновесие двойного слоя на обеих пластинках и с цинковой пластинки выделится вновь некоторое число ионов Zn2+ в раствор, а на медной пластинке разрядится соответствующее число ионов Сu2+. Таким образом, снова возникает разность в зарядах пластинок, вызывающая переход электронов с цинковой пластинки на медную, и дальнейшее течение описанных переходов ионов. В результате возникает самопроизвольно протекающий процесс, при котором цинковая пластинка будет растворяться, а на медной будут разряжаться ионы Сu2+ и выделяться металлическая медь. Переход электронов по проволоке от цинковой пластинки к медной дает электрический ток.
Гальванический элемент, основанный на описанном процессе, может служить источником получения электрического тока. Такой элемент был предложен в середине прошлого века Даниелем, Б. С. Якоби и др. Известно большое число других гальванических элементов подобного рода.
В основе всякой гальванической цепи лежит окислительно-восстановительная реакция, проводимая так, что на одном из электродов (отрицательном) происходит окисление (в элементе Якоби— растворение цинка), а на другом (положительном) —восстановление (в элементе Якоби — выделение меди).
Так, в основе работы элемента Якоби лежит реакция
Zn+Cu2+=Zn2++Cu или Zn+CuSO4=ZnSO4+Cu
Проводя указанную реакцию в гальваническом элементе, мы разделяем процессы окисления и восстановления, осуществляя их на различных электродах.
Zn0-2e-→Zn2+ - окисление (происходит на отрицательном электроде);
Cu2++e-→Cu0 – восстановление (происходит на положительном электроде).
В практике применяют иногда концентрационные гальванические элементы, которые состоят из двух одинаковых электродов (например, серебряных), опущенных в растворы одного и того же электролита (например, АgNО3), но разных концентраций. Источником электрического тока в таком элементе служит работа переноса электролита из более концентрированного в более разбавленный раствор.
Поскольку металл электродов одинаков (Ag), то растворимость обоих электродов будет одна и та же. Однако различие в концентрациях растворов приводит к тому, что равновесие Ag↔Ag+ + e- у поверхности двух электродов будет неодинаковым. В более концентрированном растворе оно несколько сдвинуто влево по сравнению с равновесием в менее концентрированном растворе. Поэтому на электроде в менее концентрированном растворе избыток электронов окажется большим и этот электрод будет более отрицательным, а второй—менее электроотрицательным.
При замыкании электродов возникает ток. В результате работы элемента концентрации растворов постепенно выравниваются. В менее концентрированном растворе содержание AgNO3 увеличивается вследствие перехода ионов серебра с пластинки в раствор и поступления ионов NO-3 из более концентрированного раствора через пористую перегородку. В более концентрированном растворе количество ионов серебра уменьшается, благодаря осаждению их на поверхности пластинки; одновременно с этим освободившиеся ионы NO-3 перемещаются в менее концентрированный раствор. Следовательно, концентрация AgNO3 в растворе уменьшается. На электродах, находящихся в растворах AgNO3 меньшей и большей концентрации, протекают реакции
Ag0-e-↔Ag+ Ag++e-↔Ag0
 2015-08-21
2015-08-21 1386
1386








