Берется медная пластинка, тщательно зачищается наждачной бумагой и последовательно промывается дистиллированной водой и спиртом. Подготовленный медный электрод помещается в электродный сосуд, заполненный раствором медного купороса, определенной концентрации.
Для определения потенциала медного электрода составляют гальваническую цепь:
Cu | CuSO4 | KCl | KCl | AgCl |AgCl
насыщ |1,0 н
Медно-сульфатный электрод помещают в стаканчик с насыщенным раствором хлористого калия вместе с электродом сравнения (хлорсеребряным электродом).
Измеренная э.д.с, цепи равна
Еизм = Екатода – Еанода = ЕCu/Cu+2 – EAg/AgCl/Cl-
отсюда
ЕCu/Cu+2 = Еизм + EAg/AgCl/Cl-
(Для 1,0 н КСl EAg/AgCl/Cl- = 0,23В)
Обычно EAg/AgCl/Cl- проверяют опытным путем, измеряя его по отношению к водородному или хингидронному электроду (см.выше). Измеряют ЕCu/Cu+2 в растворах сульфата меди различной концентрации, идя от разбавленных растворов к концентрированным. Результаты измерений заносят в таблицу:
| Концентрация CuSO4, н | Еизм, В | ЕCu/Cu 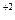 , В , В |
| 0,0001 | ||
| 0,001 | ||
| 0,01 | ||
| 0,1 | ||
| 1.0 |
Строится график зависимости ECu/Cu от логарифма концентрации CuS04. Определяется тангенс угла наклона прямой 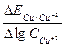 и сравнивается с теоретическим значением
и сравнивается с теоретическим значением 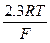 = 0,0295 при t = 250C.
= 0,0295 при t = 250C.
 2015-08-21
2015-08-21 958
958








