Позначимо початковий стан як φ0 (діедральний кут =0).Оскільки, основні конформаційні стани досягаються при послідовному повороті однієї частини молекули відносно початкового положення на 60º то відповідно далі ідуть φ1, φ2, φ3, φ4, φ5. Питання лише в тому, яку затінену форму слід вважати φ0?
Правило 1. Якщо у атома відносно якого розглядаємо конформаційністаниє всі замісники різні, то визначаємо найбільш старшу групу за правилом послідовності.
Правило 2. Якщо у атома є два замісники однакові, а третій інший, то незалежно від старшинства вибираємо саме цей „ унікальний ” замісник.
Тоді у положенні φ0 ці обрані нами групи біля першого і другого атома мають затіняти одна одну.
Другий спосіб – номенклатура Кана – Інгольда - Прелога. Для розуміння принципів цієї номенклатури розділимо проекційні формули затінених і загальмованих станів трьома площинами.
Горизонтальна площина А поділяє формулу на дві частини і проходить через центри атомів обраного зв’язку. Верхня називається син-, а нижня анти-. Дві вертикальні площини проводимо перпендикулярно до площини А і паралельно одна одній (по мітках у 60˚ від нуьової точки зліва із права).
В результаті отримаємо частину простору між цими двома площинами Б і В, який називається періпланарною (міжплощиною) і дві частини, що знаходяться зовні від площини Б і В. Вони називаються клінальними.
(див. мал.)
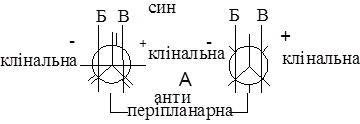
Для точної назви необхідно вказати у якій ділянці простору знаходиться вибраний замісник біля другого атома по відношенню до положення вибраного замісника біля першого атома. Спочатку вказується син- або анти-, а далі періпланарна або клінальна. Назви конформерів І-VI для бутану за двома способами наведино в таблиці. Як бачимо по два рази зустрічаються назви синклінальна та антиклінальна. Прийнято відхилення другої вибраної групи від першої вправо позначити значком (+), а вліво — знаком (-). Тоді кожне значення буде однозначне. Крім повної назви часто вживають скорочені позначення з двох літер латинського алфавіту, які ми теж подаємо в таблиці.
Таблиця №1. Назви конформерів бутану.
| I | II | III | IV | V | VI |
| φ0 | φ1 | φ2 | φ3 | φ4 | φ5 |
| синпері-планарна | + син- клінальна | + анти- клінальна | антипері-планарна | - анти- клінальна | - син- клінальна |
| sp | +sc | +ac | ap | -ac | -sc |
Конформаційні стани властиві і для неорганічних молекул. Зокрема для таких сполук як гідрогенпероксид, гідразин, гідроксиламін та інші.
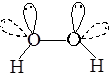
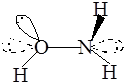
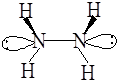
У оксигену є дві вільні пари електронів, а у нітрогену одна і таким чином формально можна говорити про псевдотетраедричну будову таких сполук, оскільки валентні кути тут відрізняються від 109,28'.
У гідроген пероксиду унікальними біля обох атомів є атоми гідрогену, а у гідразину — пари електронів (позначимо їх літерою n).
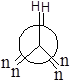
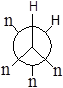
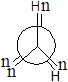
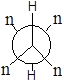
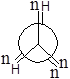

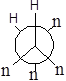
φ0 sp φ1 +SE φ2 +AS φ3 AP φ4 –AS φ5 –SE
Тут своєрідна ситуація, яку очевидно слід пояснити не лише ефектами відштовхування і притягування, а і явищами електроннї взаємодії. Найбільш вигідним буде стан з торсійним кутом ±111° (ближче до φ2 і φ4, де φ=120 ˚ та 240˚) Для антипперіпланарної конформацій (φ3) енергія вища на 4,6 кДж/моль, а для + та – синклінальних станів 30 кДж/моль. Подібна ситуація спотерігається і для гідразину та гідроксиламіну.
 2015-08-21
2015-08-21 364
364







