Таблица 6. Произведения растворимости
Произведение растворимости – одна из основных характеристик осадка, численное значение которой необходимо для решения многих химико-аналитических задач:
1) расчёт растворимости осадков при заданных условиях:
- в воде (через ПР0 при μ → 0 или через ПР при μ > 0);
- в присутствии одноимённых ионов (через ПР0 при μ → 0 или через ПР при μ > 0);
- в присутствии разноимённых ионов (через ПР);
2) расчёт условий растворения и осаждения осадков:
- условий количественного осаждения малорастворимого соединения (см. Пример 4);
- условий начала образования осадка;
- условий, при которых осадок не выпадает;
3) прогнозирование возможности выпадения осадка при смешении растворов заданной концентрации (путём сравнения ПР0 и ПС);
4) выбор осадителя и осаждаемой формы для конкретного иона (см. Пример 5);
5) оценка возможности обнаружения или количественного определения конкретного иона с использованием реакций осаждения (см. Пример 6).
При решении некоторых из этих задач используются следующие условия, требования и количественные критерии.
| Ø Осадок выпадает при условии ПС ³ ПР0. Ø Осадок растворяется при условии ПС < ПР0. Ø Осаждение считается количественным, если остаточная концентрация осаждаемого иона в растворе не превышает 10–6 моль/л. Ø Осадитель должен образовывать с определяемым ионом как можно менее растворимое соединение. Ø В качестве осаждаемой формы пригодны только те осадки, для которых ПР0 £ 10–8 (для бинарных электролитов). |
l Пример 4. При какой концентрации фторид-ионов магний (II) количественно осадится в виде MgF2?
Равновесие
MgF2¯ «Mg2+ + 2F–
характеризуется табличной величиной произведения растворимости:
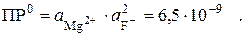
Поскольку в насыщенном растворе малорастворимого электролита μ → 0, то активности можно заменить на концентрации. После подстановки [Mg2+] = 10–6 моль/л получим:
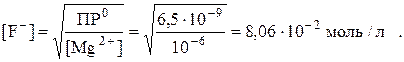
l Пример 5. Выбрать осаждаемую форму и осадитель для гравиметрического определения алюминия (III).
Из приведённых в таблице осадков, содержащих ион алюминия (III), наименее растворимым является Al(OH)3, следовательно, он является подходящей гравиметрической формой, а в качестве осадителя можно использовать щёлочи либо гидроксид аммония. Однако в избытке щелочей амфотерный гидроксид Al(OH)3 растворяется, поэтому осаждение надо проводить раствором NH4OH.
l Пример 6. Можно ли использовать реакцию образования MgC2O4 для количественного определения магния (II) с использованием гравиметрического или перманганатометрического методов
анализа?
По значению ПР0 = 8,6·10–5 можно сделать вывод, что осадок MgC2O4 в заметной степени растворим, следовательно, он не может служить осаждаемой формой в гравиметрическом методе анализа и не позволит с достаточной точностью провести титриметрическое определение.
Таблица 6
Произведения растворимости важнейших
малорастворимых веществ
| Формула вещества | ПР |
| Ag3AsO3 | 1∙10–17 |
| Формула вещества | ПР |
| Ag3АsО4 | 1∙10–22 |
| AgBO2 | 4∙10–3 |
| AgBr | 5,3∙10–13 |
| AgBrO3 | 5,5∙10–5 |
| AgC2H3O2 | 4∙10–3 |
| AgCN | 1,4∙10–16 |
| Ag2CO3 | 1,2∙l0–12 |
| Ag2C2O4 | 3,5∙10–11 |
| AgCl | 1,78∙10–10 |
| AgClO2 | 2∙10–4 |
| AgClO3 | 5,0∙10–2 |
| Ag2CrO4 | 1,1∙10–12 |
| Ag2Cr2O7 | 1∙10–10 |
| Ag3Fe(CN)6 | 1∙10–22 |
| Ag4Fe(CN)6 | 8,5∙10–45 |
| Ag2HVO4 | 2∙10–14 |
| AgI | 8,3·10–17 |
| AgIO3 | 3,0·10–8 |
| AgMnO4 | 1,6·10–3 |
| Ag2MoO4 | 2,8·10–9 |
| AgN3 | 2,9·10–9 |
| AgNO2 | 6,0·10–4 |
| Ag2O (Ag+,OH–) | 1,95·10–8 |
| AgOCN | 2,3·10–7 |
| Ag3PO4 | 1,3·10–20 |
| AgReO4 | 7,95·10–5 |
| Ag2S | 6,3·10–50 |
| AgSCN | 1,1·10–12 |
| Ag2SO3 | 1,5·10–14 |
| AgSO3NH2 | 1·10–1 |
Продолжение табл. 6
| Ag2SO4 | 1,6·10–5 |
| AgSeCN | 4,0·10–16 |
| Ag2SeO3 | 9,8·10–16 |
| Ag2SeO4 | 5,6·10–8 |
| AgVO3 | 5·10–7 |
| Ag2WO4 | 5,5·10–12 |
| AlAsO4 | 1,6·10–16 |
| А1(ОН)3 | 3,2·10–34 |
| A1PO4 | 5,75·10–19 |
| Ba3(AsO4)2 | 7,8·10–51 |
| Ba(BrO3)2 | 5,5·10–6 |
| BaCO3 | 4,0·10–10 |
| BaC2O4 | 1,1·10–7 |
| BaCrO4 | 1,2·10–10 |
| BaF2 | 1,1·10–6 |
| Ba2Fe(CN)6 | 3·10–8 |
| Ba(IO3)2 | 1,5·10–9 |
| BaMnO4 | 2,5·10–10 |
| BaMoO4 | 4·10–8 |
| Ba3(PO4)2 | 6·10–39 |
| Ba2P2O7 | 3∙10–11 |
| BaSO3 | 8∙10–7 |
| BaSO4 | 1,1∙10–10 |
| BaS2O3 | 1,6∙10–5 |
| BaSeO4 | 5∙10–8 |
| BeCO3 | 1∙10–3 |
| BeMoO4 | 3,2∙10–12 |
| Be(OH)2 | 4,9∙10–22 |
| BiAsO4 | 2,8∙10–10 |
| BiI3 | 8,1∙10–19 |
| Bi(OH)3 | 3,2∙10–32 |
| BiPO4 | 1,3∙10–23 |
| Bi2S3 | 1∙10–97 |
| Ca3(AsO4)2 | 6,8∙10–19 |
| CaC4H4O6 (тартрат) | 7,7∙10–7 |
| CaCO3 | 3,8∙10–9 |
| CaC2O4 | 2,3∙10–9 |
| CaCrO4 | 7,1∙10–4 |
| CaF2 | 4,0∙10–11 |
| Ca(NH4)2Fe(CN)6 | 4∙10–8 |
| Са(IO3)2 | 7,0∙10–7 |
| Ca(OH)2 | 6,5∙10–6 |
| Ca3(PO4)2 | 2,0∙10–29 |
| CaPO3F (Ca2+, PO3F2–) | 4∙10–3 |
| CaSO3 | 3,2∙10–7 |
| CaSO4 | 2,5∙10–5 |
| CaSeO3 | 4,7∙10–6 |
| CaSiF6 | 8,1∙10–4 |
| CaWO4 | 9,0∙10–9 |
| Cd3(AsO4)2 | 2,2∙10–33 |
| Cd(CN)2 | 1,0∙10–8 |
| CdCO3 | 1,0∙10–12 |
| CdC2O4 | 1,5∙10–8 |
| Cd2Fe(CN)6 | 4,2∙10–18 |
| Cd(OH)2 | 5,9∙10–15 |
| CdS | 1,6·10–28 |
| CdSeO3 | 5,0·10–9 |
| Ce(IO3)4 | 5·10–17 |
Продолжение табл. 6
| Ce(OH)3 | 1,5·10–20 |
| CoCO3 | 1,05·10–10 |
| CoC2O4 | 6,3·10–8 |
| Co2Fe(CN)6 | 4,8·10–38 |
| Co(IO3)2 | 1,0·10–4 |
| Co(OH)2 | 2,0·10–16 |
| Co(OH)3 | 4·10–45 |
| CoS α | 4,0·10–21 |
| CoS β | 2,0·10–25 |
| CoSeO3 | 1,6·10–7 |
| CrAsO4 | 7,8·10–21 |
| Cr(OH)2 | 1,0·10–17 |
| Cr(OH)3 | 6,3·10–31 |
| CrPO4 | 2,4·10–23 |
| CsClO4 | 4∙10–3 |
| Cu3(AsO4)2 | 7,6∙10–36 |
| CuBr | 5,25∙10–9 |
| CuCN | 3,2∙10–20 |
| CuCO3 | 2,5∙10–10 |
| CuC2O4 | 3∙10–9 |
| CuCl | 1,2∙10–6 |
| CuCrO4 | 3,6∙10–6 |
| Cu2Fe(CN)6 | 1,3∙10–16 |
| CuI | 1,1∙10–12 |
| Сu(IO3)2 | 7,4∙10–8 |
| CuN3 | 5,0∙10–9 |
| Cu2O (2Cu+, OH–) | 1∙10–14 |
| Cu(OH)2 | 8,3∙10–20 |
| Cu2(OH)2CO3 | 1,7∙10–34 |
| Cu2P2O7 | 8,3∙10–16 |
| CuS | 6,3∙10–36 |
| Cu2S | 2,5∙10–48 |
| CuSCN | 4,8∙10–15 |
| CuSe | 1∙10–49 |
| CuSeO3 | 1,7∙10–8 |
| FeAsO4 | 5,8∙10–21 |
| FeCO3 | 3,5∙10–11 |
| FeC2O4 | 2∙10–7 |
| Fe4[Fe(CN)6]3 | 3,0∙10–41 |
| Fe(OH)2 | 7,1∙10–16 |
| Fe(OH)3 | 6,3∙10–38 |
| FePO4 | 1,3∙10–22 |
| FeS | 5∙10–18 |
| HgS | 1,6∙10–52 |
| In(OH)3 | 1,2∙10–37 |
| In2S3 | 5,75∙10–74 |
| K3AlF6 | 1,6∙10–9 |
| K(C6H5)4B | 2,25∙10–8 |
| K3Co(NO2)6 | 4,3∙10–10 |
| K2PdCl6 | 6,0∙10–6 |
| K2PtCl6 | 1,1∙10–5 |
| La2S3 | 2,0∙10–13 |
| Li3PO4 | 3,2∙10–9 |
| Mg3(AsO4)2 | 2,1∙10–20 |
| MgCO3 | 2,1∙10–5 |
| MgC2O4 | 8,6∙10–5 |
| MgF2 | 6,5∙10–9 |
| Mg(IO3)2 | 3∙10–3 |
Продолжение табл. 6
| MgK2Fe(CN)6 | 5∙10–9 |
| Mg(NH4)2Fe(CN)6 | 4∙10–8 |
| MgNH4PO4 | 2,5∙10–13 |
| Mg(OH)2 | 7,1∙10–12 |
| Mg3(PO4)2 | 1∙10–13 |
| MgSO3 | 3∙10–3 |
| MgSeO3 | 4,4∙10–6 |
| Mn3(AsO4)2 | 1,9∙10–29 |
| MnCO3 | 1,8∙10–11 |
| MnC2O4 | 5∙10–6 |
| Mn2Fe(CN)6 | 7,9∙10–13 |
| MnNH4PO4 | 1∙10–12 |
| Mn(OH)2 | 1,9∙10–13 |
| Mn(OH)3 | 1∙10–36 |
| MnS | 2,5∙10–10 |
| MnSeO3 | 5,4∙10–8 |
| (NH4)3AlF6 | 1,6∙10–3 |
| (NH4)3Co(NO2)6 | 7,6∙10–6 |
| (NH4)2IrCl6 | 3∙10–5 |
| (NH4)2PtCl6 | 9∙10–6 |
| Na3AlF6 | 4,1∙10–10 |
| NaSb(OH)6 | 4∙10–8 |
| Na2SiF6 | 2,8∙10–4 |
| Ni3(AsO4)2 | 3,1∙10–26 |
| Ni(CN)2 | 3∙10–23 |
| NiCO3 | 1,3∙10–7 |
| NiC2O4 | 4∙10–10 |
| Ni(ClO3)2 | 1∙10–4 |
| Ni2Fe(CN)6 | 1,3∙10–15 |
| Ni(IO3)2 | 1,4∙10–8 |
| Ni(OH)2 | 2,0∙10–15 |
| Ni2P2O7 | l,7∙10–13 |
| NiS | 3,2∙10–19 |
| NiSeO3 | 1,0∙10–5 |
| Pb3(AsO4)2 | 4,1∙10–36 |
| PbBr2 | 9,1∙10–6 |
| Pb(BrO3)2 | 8,0∙10–6 |
| PbCO3 | 7,5∙10–14 |
| PbC2O4 | 4,8∙10–10 |
| РbС12 | 1,6∙10–5 |
| РbСrO4 | 1,8∙10–14 |
| PbF2 | 2,7∙10–8 |
| Pb2Fe(CN)6 | 9,55∙10–19 |
| PbI2 | 1,1∙10–9 |
| Рb(IO3)2 | 2,6∙10–13 |
| РbМоO4 | 4,0∙10–6 |
| Pb(N3)2 | 2,6∙10–9 |
| Рb(ОН)2 | 7,9∙10–16 |
| Рb3(РО4)2 | 7,9∙10–43 |
| PbS | 2,5∙10–27 |
| Pb(SCN)2 | 2,0∙10–5 |
| PbSO4 | 1,6∙10–8 |
| PbS2O3 | 4,0∙10–7 |
| PbSe | 1∙10–38 |
| PbSeO3 | 3∙10–12 |
| PbSeO4 | 1,45∙10–7 |
| PbWO4 | 4,5∙10–7 |
| Pb(OH)4 | 3,0∙10–66 |
Окончание табл. 6
| Sc(OH)3 | 5,0∙10–37 |
| SnI2 | 8,3∙10–6 |
| Sn(OH)2 | 6,3∙10–27 |
| Sn(OH)4 | 1∙10–57 |
| SnS | 2,5∙10–27 |
| Sr3(AsO4)2 | 1,3∙10–18 |
| SrCO3 | 1,1∙10–10 |
| SrC2O4 | 1,6∙10–7 |
| SrCrO4 | 3,6∙10–5 |
| SrF2 | 2,5∙10–9 |
| Sr(IO3)2 | 3,3∙10–7 |
| SrMoO4 | 2∙10–7 |
| Sr(OH)2 | 3,2∙10–4 |
| Sr3(PO4)2 | 1∙10–31 |
| SrSO3 | 4∙10–8 |
| SrSO4 | 3,2∙10–7 |
| SrSeO3 | 4,4∙10–6 |
| Y(OH)3 | 6,3∙10–25 |
| Zn3(AsO4)2 | 1,3∙10–28 |
| Zn(CN)2 | 2,6∙10–13 |
| ZnCO3 | 1,45∙10–11 |
| ZnC2O4 | 2,75∙10–8 |
| Zn2Fe(CN)6 | 2,1∙10–16 |
| Zn(IO3)2 | 2,0∙10–8 |
| Zn(OH)2 | 1,4∙10–17 |
| Zn3(PO4)2 | 9,1∙10–33 |
| ZnS | 1,6∙10–24 |
| ZnSe | 1∙10–31 |
| ZnSeO3 | 1,9∙10–8 |
Таблица 7. Значения рН осаждения гидроксидов металлов
Значения рН начала осаждения гидроксидов металлов, практически полного их осаждения, а также начала растворения и полного растворения осадков амфотерных гидроксидов необходимы во всех случаях выбора оптимального интервала значений рН с целью обнаружения, разделения и количественного определения ионов многовалентных металлов.
l Пример 7. В какой среде можно оттитровать комплексонометрически ион Fe3+ при его концентрации в растворе ~ 0,01 моль/л?
Поскольку гидроксид железа (III) из 0,01 М раствора начинает осаждаться при рН = 2,3, то титрование можно провести только в кислой среде.
l Пример 8. Можно ли разделить ионы Cr3+ и Mg2+ при их концентрациях 0,01 моль/л, регулируя значение рН раствора?
Cr(OH)3 практически полностью осаждается при рН = 6,8, а начинает растворяться при рН = 9,4. Mg(OH)2 начинает осаждаться при рН = 10,4, полнота осаждения его достигается при рН = 12,4. Следовательно, в интервале 6,8 < рН < 9,4 ион Cr3+ будет находиться в осадке, а ион Mg2+ – в растворе, т. е. разделение возможно.
Таблица 7
 2015-09-06
2015-09-06 2310
2310
