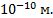В молекулярной физике принято характеризовать массы атомов и молекул не их абсолютными значениями, например в килограммах, а относительными безразмерными величинами – относительными атомной Ar и молекулярной Mr массами. В качестве атомной единицы массы (а.е.м., или mu) принимается 1/12 массы mC изотопа углерода 12C: mu = mC /12 = 1,66⋅10 –27 кг. Следовательно, масса любого атома равна m = muA = 1,66⋅10 –27 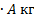 , где А – атомная масса элемента. Например, для водорода А = = 1,00797 кг и масса его атома
, где А – атомная масса элемента. Например, для водорода А = = 1,00797 кг и масса его атома 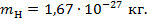 Относительной атомной массой Ar называют отношение абсолютного значения массы данного атома к атомной единице массы. Аналогично определяется и относительная молекулярная масса Mr = m / mu, где m – абсолютная масса молекулы.
Относительной атомной массой Ar называют отношение абсолютного значения массы данного атома к атомной единице массы. Аналогично определяется и относительная молекулярная масса Mr = m / mu, где m – абсолютная масса молекулы.
В молекулярной физике широко используется понятие количества вещества, выражаемое в молях. Моль равен такому количеству вещества, которое содержит столько же структурных элементов (атомов, молекул), сколько их атомов содержится в 0,012 кг изотопа углерода 12C. Следовательно, моль любого вещества содержит, по определению, одинаковое число структурных элементов, которое называют постоянной Авогадро, или числом Авогадро:
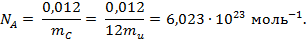 |
В молекулярной физике помимо относительной молекулярной массы часто используют молярную массу, т.е. массу вещества, взятого в количестве одного моля. Молярная масса M равна произведению массы молекулы данного вещества m на число Авогадро NA: M = mNA. Она имеет разное значение для каждого вещества, но всегда содержит одинаковое число молекул. Молярная масса вещества, состоящего из одноатомных молекул, содержит одинаковое число атомов, и ее в этом случае называют атомной массой. Для углерода (12C) молярная масса в точности равна 0,012кг/моль и, следовательно, масса его атома:
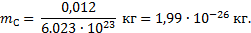
Молярную массу M можно выразить через относительную молекулярную массу Mr. Так как относительная молекулярная масса 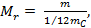 то масса молекулы то масса молекулы 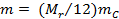 . Следовательно, молярная масса . Следовательно, молярная масса
|
 2015-09-06
2015-09-06 3183
3183

 Например, молярная масса углекислого газа СО2 равна 0,044 кг/моль, так как его относительная молекулярная масса равна 44. Произведем теперь оценку размеров молекул. Рассмотрим пример с молекулой воды. Молярная масса воды
Например, молярная масса углекислого газа СО2 равна 0,044 кг/моль, так как его относительная молекулярная масса равна 44. Произведем теперь оценку размеров молекул. Рассмотрим пример с молекулой воды. Молярная масса воды 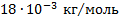 , а так как плотность воды
, а так как плотность воды 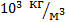 , то 1 моль воды занимает объем
, то 1 моль воды занимает объем 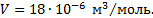 В этом объеме содержится NA молекул, а число молекул в единице объема равно
В этом объеме содержится NA молекул, а число молекул в единице объема равно 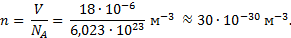 Так как в жидкости молекулы расположены довольно плотно одна к другой, то принимая, что на каждую молекулу приходится кубик со стороной а, то имеет место равенство а 3 n = 1. Следовательно, линейный размер молекулы воды будет приблизительно равен
Так как в жидкости молекулы расположены довольно плотно одна к другой, то принимая, что на каждую молекулу приходится кубик со стороной а, то имеет место равенство а 3 n = 1. Следовательно, линейный размер молекулы воды будет приблизительно равен 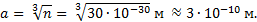 Линейные размеры молекул других веществ представляют собой также величины порядка
Линейные размеры молекул других веществ представляют собой также величины порядка