Перший закон термодинаміки – це закон збереження енергії для систем, у яких істотну роль відіграють теплові процеси. Чітке формулювання першого закону термодинаміки виявилося можливим завдяки енергетичній еквівалентності теплоти і роботи, що було доведено Ю.Р. Майєром у 1842 р. і Дж. Джоулем у 1843 р.
Якщо термодинамічній системі надати ззовні деяку кількість теплоти 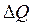 і виконати над цією системою роботу
і виконати над цією системою роботу 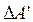 зовнішніми силами, то внутрішня енергія цієї системи зміниться на величину
зовнішніми силами, то внутрішня енергія цієї системи зміниться на величину 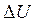 :
:
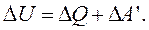 (2.11)
(2.11)
Робота 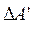 зовнішніх сил над системою дорівнює за величиною і протилежна за знаком роботі
зовнішніх сил над системою дорівнює за величиною і протилежна за знаком роботі 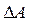 , виконаній системою проти зовнішніх сил:
, виконаній системою проти зовнішніх сил: 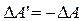 . 3 урахуванням цього рівнянню (2.11) можна надати вигляду:
. 3 урахуванням цього рівнянню (2.11) можна надати вигляду:
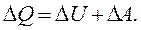
 (2.12)
(2.12)
Для нескінченно малої зміни стану системи маємо:
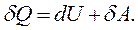 (2.13)
(2.13)
Це і є математичний запис першого закону термодинаміки, який можна сформулювати в такий спосіб:
„Теплота, що надається системі, витрачається на зміну внутрішньої енергії системи і на здійснення системою роботи проти зовнішніх сил”.
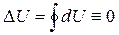 У випадку колових процесів, коли система проходить ряд змін і поверта-ється у вихідний стан, і
У випадку колових процесів, коли система проходить ряд змін і поверта-ється у вихідний стан, і 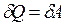 , тобто перший закон тер-модинаміки стверджує:
, тобто перший закон тер-модинаміки стверджує:
„Якщо система виконує цикловий процес, то повна кількість теплоти, надана системі в цьому процесі, дорівнює виконаній нею роботі”. Приблизно так було сформульовано перший законтермодинаміки у 1847 р. Г. Гельмгольцем.
На підставі рівняння (2.13) знаходимо: якщо у випадку колових процесів 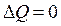 ,то і
,то і 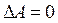 . Звідси випливає таке формулювання першого закону термодинаміки:
. Звідси випливає таке формулювання першого закону термодинаміки:
„Неможливий процес, єдиним результатом якого було би виконання роботи без яких-небудь змін в інших тілах”, чи „Неможливий вічний двигун (перпетуум-мобіле) першого роду”.
Уся ця різноманітність формулювань першого закону термодинаміки виражає єдину його суть – закон збереження енергії системи у випадку теплових процесів.
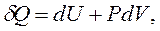 Для однорідних тіл, здатних виконати роботу тільки у разі зміни об’єму, рівняння (2.13) можна записати у вигляді:
Для однорідних тіл, здатних виконати роботу тільки у разі зміни об’єму, рівняння (2.13) можна записати у вигляді:
(2.14)
а з урахуванням рівняння (2.10), одержуємо:
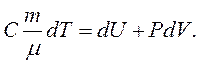 |
(2.15)
 2015-09-06
2015-09-06 1431
1431








