Запишем уравнение Менделеева-Клапейрона:
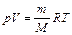 , (2.3)
, (2.3)
где R - газовая постоянная; 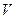 - объем газа;
- объем газа; 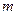 - масса газа;
- масса газа; 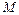 - молярная масса газа;
- молярная масса газа; 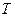 - термодинамическая температура газа.
- термодинамическая температура газа.
Постоянная 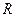 одинакова для всех газов. Выразим ее из (2.3):
одинакова для всех газов. Выразим ее из (2.3):
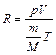 , (2.4)
, (2.4)
где 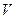 - объем воздуха в колбе вместе с подводящими трубками при комнатной температуре.
- объем воздуха в колбе вместе с подводящими трубками при комнатной температуре.
Объем легко вычислить, если рассмотреть уравнение Менделеева-Клапейрона для двух различных состояний газа:
· при комнатной температуре 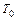 :
: 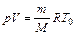 (2.4)
(2.4)
· при температуре 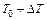 :
: 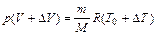 . (2.5)
. (2.5)
Поделив уравнение (2.5) на уравнение (2.4), получим: 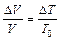 , откуда объем V газа равен:
, откуда объем V газа равен:
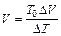 . (2.6)
. (2.6)
Учитывая, что масса газа может быть найдена как произведение плотности воздуха 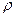 на объем
на объем 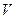 , окончательно получим:
, окончательно получим:
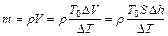 , (2.7)
, (2.7)
где 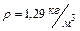 ;
; 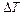 - приращение температуры, выбранное экспериментатором.
- приращение температуры, выбранное экспериментатором.
Так как нагрев воздуха происходит при постоянном давлении, то, продифференцировав уравнение Менделеева-Клапейрона по объему, получим:
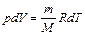 , откуда
, откуда 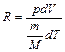 (2.8)
(2.8)
Газоваяпостоянная R численно равна работе одного моля газа при изобарном нагревании его на один градус. Следовательно, зная работу расширения газа можно найти постоянную 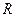 из соотношения (2.8). Однако в нашей работе, чтобы исключить ошибки при измерениях
из соотношения (2.8). Однако в нашей работе, чтобы исключить ошибки при измерениях 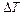 и
и 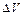 рекомендуется определить газовую постоянную при исследовании зависимости изменения объема газа от температуры
рекомендуется определить газовую постоянную при исследовании зависимости изменения объема газа от температуры 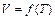 , которая представляет собой уравнение Менделеева-Клапейрона, записанное в виде:
, которая представляет собой уравнение Менделеева-Клапейрона, записанное в виде:
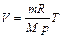 (2.9)
(2.9)
Величина, равная 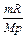 , является постоянной в данной лабораторной работе. Введем обозначение:
, является постоянной в данной лабораторной работе. Введем обозначение:
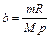 , (2.10)
, (2.10)
где 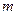 - масса газа, найденная ранее,
- масса газа, найденная ранее, 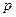 - атмосферное давление.
- атмосферное давление.
Выразим из (2.10) газовую постоянную R:
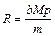 , (2.11)
, (2.11)
Учитывая (2.10), выражение (2.9) можно представить в виде:
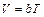 (2.12)
(2.12)
Выражение (2.12) представляет собой уравнение прямой, для которой 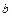 - угловой коэффициент.
- угловой коэффициент.
Таким образом, построив по экспериментальным данным график зависимости объема 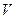 от температуры
от температуры 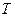 можно определить значение углового коэффициента
можно определить значение углового коэффициента 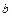 , равного тангенсу угла наклона, а затем, используя выражение (2.11) рассчитать значение газовой постоянной R.
, равного тангенсу угла наклона, а затем, используя выражение (2.11) рассчитать значение газовой постоянной R.
 2015-09-06
2015-09-06 5046
5046
