Приклад 1. За наведеною схемою:
PbS + HNO3 → S + NO +Pb(NO3)2 +H2O
складіть рівняння хімічної реакції і розставте в ній коефіцієнти методом електронного балансу.
Розв’язання. Під час розставлення коефіцієнтів у рівнянні хімічної реакції методом електронного балансу дотримуються такого алгоритму:
1. Спочатку визначають ступені окиснення елементів у речовинах і встановлюють, які елементи змінили свої ступені окиснення.
2. Потім складають схеми процесів окиснення і відновлення.
3. Підбираючи відповідні множники зрівнюють число відданих та прийнятих електронів – складають електронний баланс.
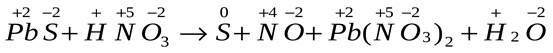 4. Розставляють коефіцієнти в рівнянні хімічної реакції, спочатку зрівнюючи число атомів елементів, що змінили свій ступінь окиснення, потім елементів-металів, елементів-неметалів, серед яких, як правило, число атомів Оксигену зрівнюють в останню чергу.
4. Розставляють коефіцієнти в рівнянні хімічної реакції, спочатку зрівнюючи число атомів елементів, що змінили свій ступінь окиснення, потім елементів-металів, елементів-неметалів, серед яких, як правило, число атомів Оксигену зрівнюють в останню чергу.
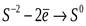 │3│ - процес окиснення, елемент-відновник;
│3│ - процес окиснення, елемент-відновник;
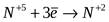 │2│ - процес відновлення, елемент-окисник.
│2│ - процес відновлення, елемент-окисник.
Розставляємо коефіцієнти для елементів, що змінили свій ступінь окиснення. Враховуємо, що не всі атоми нітрогену (в лівій частині рівняння N+5) змінили свій ступінь окиснення, тому отриманий за балансом для нітрогену коефіцієнт 2 ставимо лише перед формулою NO:
3PbS + HNO3 → 3S + 2NO +3Pb(NO3)2 + H2O.
Після цього підраховуємо загальне число атомів Нітрогену у формулах нітрогеновмісних сполук правої частини рівняння (оскільки у цій частині рівняння коефіцієнти перед сполуками, що містять Нітроген, розставлені): 2NO, 3Pb(NO3)2; воно дорівнює 8. Ставимо цей коефіцієнт перед нітратною кислотою:
3PbS + 8HNO3 → 3S + 2NO + 3Pb(NO3)2 + H2O.
Тепер підраховуємо число атомів Гідрогену, у лівій частині рівняння перед формулою HNO3 воно дорівнює 8. Отже, перед формулою H2O ставимо коефіцієнт 4:
3PbS + 8HNO3 → 3S + 2NO + 3Pb(NO3)2 + 4H2O.
Перевіряємо загальне число атомів Оксигену: у лівій і у правій частинах рівняння воно однакове і дорівнює 24. Отже, коефіцієнти у рівнянні хімічної реакції розставлені правильно.
 2015-09-06
2015-09-06 1519
1519








