| Номери колб | Концентрація розчину, моль/л | Адсорбція Г, моль/г | Відношення Со/Г, г/л | |
| вихідного С0 | рівноважного Ср | |||
4. Будують експериментальну ізотерму адсорбції Ленгмюра в координатах Г=f(Ср).
5. Будують пряму в координатах 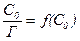 (див. лабораторну роботу №7, рис. 7.3). Граничну адсорбцію Г¥. знаходять як котангенс кута нахилу отриманої прямої до вісі ординат.
(див. лабораторну роботу №7, рис. 7.3). Граничну адсорбцію Г¥. знаходять як котангенс кута нахилу отриманої прямої до вісі ординат.
6. Обчислюють питому адсорбційно-активну площу поверхні адсорбенту S [м2/г] за таким рівнянням.
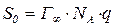 , (8.6)
, (8.6)
де Г¥ – гранична адсорбція; NA – число Авогадро, NA =6,02×1023; q – “посадкова площа” однієї молекули, для кислот жирного ряду q=20×10-20 м2.
7. Одержані результати питомої поверхні адсорбенту порівнюють з паспортними даними для цих адсорбентів.
Питання для самоперевірки
1. Основні положення явища адсорбції, поняття: адсорбція, адсорбент, адсорбат.
2. Характеристика фізичної та хімічної адсорбції.
3. Адсорбція на межі поділу тверде тіло – газ: рівняння ізотерми адсорбції Ленгмюра та його графічне розв’язання, розрахунок ємності моношару та питомої поверхні адсорбенту.
4. Молекулярна адсорбція з розчинів на поверхні твердого тіла. Як розрахувати кількість речовини, адсорбованої одиницею поверхні адсорбенту?
5. Сформулюйте правило вирівнювання полярностей Ребіндера. Покажіть схематично орієнтацію молекул ПАР на межі поділу вода – вугілля та бензол – силікагель.
6. Сформулюйте правило Дюкло- Траубе.
7. Навести приклади гідрофільних та гідрофобних адсорбентів.
 2015-09-06
2015-09-06 410
410








