МЕТОДОМ КЛЕМАНА - ДЕЗОРМА
Цель работы: определение величины отношения теплоемкости воздуха при постоянном давлении к теплоемкости при постоянном объеме.
Приборы и принадлежности: Клапан, сосуд с герметической пробкой, насос ручной, соединительные трубки, датчик давления, измерительный блок L -микро
Введение
1. Идеальным называется газ
- Молекулы которого можно считать материальными точками (другими словами, размеры молекул много меньше расстояния между ними);
- Молекулы газа не взаимодействуют на расстоянии, а испытывают лишь упругие столкновения друг с другом (и со стенками сосуда, в котором находятся).
Идеальный газ описывается уравнением Менделеева – Клапейрона:
pV = 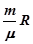 T, (1)
T, (1)
где p – давление газа (измеряется в паскалях); V – объём газа (измеряется в кубических метрах); m – его масса (в килограммах); m - масса одного моля газа (в килограммах на моль); T – термодинамическая температура (в кельвинах), R = 8,31 кг×моль- 1 ×К- 1 – универсальная газовая постоянная.
2. Первое начало (закон) термодинамики утверждает, что количество теплоты d Q, сообщенное системе, расходуется на изменение её внутренней энергии dU и на работу d А, совершаемую системой против внешних сил:
d Q = dU +d A. (2)
Для идеального газа
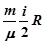 dT, (3)
dT, (3)
Здесь i – число степеней свободы – число независимых параметров, определяющих положение и ориентацию молекулы в пространстве.
Работа газа связана с изменением dV его объёма:
d A = p dV. (4)
В частности, если давление газа не меняется (такой процесс называется изобарным), то, с учётом уравнения (1), можно получить:
d A = 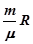 dT. (5)
dT. (5)
Очевидно также, что при V = const dV = 0 и d A = 0.
3. Запишем формулы первого начала термодинамики для основных изопроцессов, которые можно осуществить с идеальным газом.
– Изобарный (р = const ):
d Q = 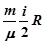 dT +
dT + 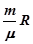 dT, или
dT, или
d Q = 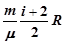 dT. (6)
dT. (6)
– Изохорный (V = const ):
d Q = 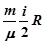 dT. (7)
dT. (7)
– Изотермический (Т = const ):
d Q = p dV. (8)
– Адиабатный (происходящий без теплообмена с окружающей средой, d Q = 0 ):
0 = 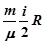 dT + p dV. (9)
dT + p dV. (9)
4. Теплоемкостью газа называется величина равная количеству теплоты, необходимой для нагревания данной массы газа на один кельвин.
с = lim D Q / D T = dQ / dT. (10)
D T ®0
С = с × 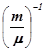 .
.
Получим выражения для теплоёмкости газа в изохорном (при постоянном объёме) C v и изобарном (при постоянном давлении) C p процессах.
– ПриV = const
C v= 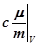 =
= 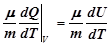 =
= 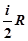 . (11)
. (11)
– При р = const
C p= 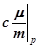 =
= 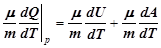 =
= 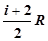 . (12)
. (12)
Из (11) и (12) следует, что
C p= C v + R. (13)
Соотношение (13) носит название уравнения Майера.
5. Пользуясь уравнением Менделеева – Клапейрона (1), формулами (11) и (12) для C v и C p и соотношением (9) – первым началом термодинамики в случае адиабатного процесса, можно получить формулу, связывающую параметры идеального газа при адиабатном процессе. Для этого достаточно продифференцировать обе части уравнения (1) по Т:
p 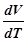 + V
+ V 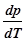 =
= 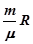 ,
,
откуда
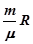 dT = pdV + Vdp,
dT = pdV + Vdp,
и подставить последнее соотношение в формулу (10). Тогда получится:
0 = 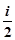 (pdV + Vdp)+ p dV,
(pdV + Vdp)+ p dV,
или
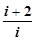 pdV + Vdp = 0.
pdV + Vdp = 0.
d 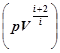 = 0, или
= 0, или
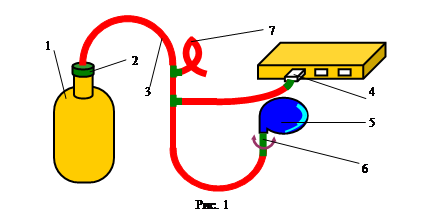
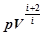 = const. (14)
= const. (14)
С учётом того, что
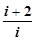 =
= 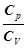 ,
,
формулу (14) можно записать в виде
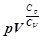 = const. (15)
= const. (15)
Данная формула носит название уравнения Пуассона для адиабатного процесса.
Обозначив отношение C p / C v символом g, уравнение (15) можно переписать:
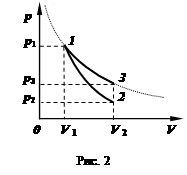 pV g = const. (16)
pV g = const. (16)
В настоящей работе предлагается найти показатель степени в уравнении Пуассона для сухого воздуха, который при комнатных условиях с хорошей точностью можно считать идеальным газом.
 2015-09-06
2015-09-06 302
302








