Типи н основні параметри компресорних машин
Типи компресорних машин
Компресорні машини за величиною тиску поділяються на такі групи:
1) низького тиску (надлишковий тиск до 0,1 кгс/см2) – вентилятори;
2) середнього тиску (надлишковий тиск 0,1-3 кгс/см2) без охолодження - газодувки;
3) високого тиску (надлишковий тиск від 3 кгс/см2 і вище) з охолодженням - компресори;
4) вакуумні (розрідження більше 0,5 кгс/см2) -вакуум-насоси.
Незважаючи на конструктивні відмінності кожної групи машин, принцип дії їх однаковий. Тому газодувки, вентилятори і вакуум-насоси можна розглядати як різновид компресорів.
Компресори діляться на поршневі, ротаційні, відцентрові, осьові і струменеві. Відцентрові компресори називаються турбокомпресорами і турбогазодувками. До відцентрових і осьових компресорів можуть бути віднесені вентилятори. Вакуум-насоси являють собою компресори, в яких газ засмоктується при розрідженні і виштовхується під тиском дещо більшим атмосферного.
Процеси стиснення газу
Роботу, витрачену на стиснення газу в компресорі, можна визначити із узагальненого рівняння Бернуллі (6-38). Зазвичай не враховують відмінності швидкостей газу ω1 і ω2 до і після стиснення, т. б. вважають, що ω1 = ω2. Тоді рівняння має вигляд:
l + q = i2 − i1.
З цього виразу випливає, що витрачена в компресорі робота l і підведене до газу тепло q витрачаються на збільшення ентальпії газу.
Теоретично процес стиснення газу в компресорі може бути адіабатичним або ізотермічним.
При адіабатичному стисненні тепло не підводиться до газу і не відводиться від нього, т. б. q = 0, і рівняння приймає вигляд:
l = i2 − i1.
У цьому випадку вся витрачена в компресорі робота обертається в тепло і витрачається на нагрівання газу, внаслідок чого його ентальпія зростає. При адіабатичному стисненні значно підвищується температура стисненого газу.
В ізотермічному процесі газ стискається при постійній температурі. У цьому випадку внутрішня енергія газу не змінюється (u1 = u2) і дотримується рівність рυ1 = рυ2. oтже, u1 + рυ1 = u2 + рυ2, або і1 = i 2, т. б. ентальпія газу при стисненні не змінюється. Відповідно рівняння приймає вигляд:
l + q = 0, або l = − q
Знак мінус перед q вказує на відведення тепла. Таким чином, при ізотермічному стисненні вся витрачена робота обертається в тепло і відводиться від газу, внаслідок чого температура, внутрішня енергія і ентальпія газу не змінюються. Отже, при ізотермічному стисненні газу необхідно охолоджувати компресор, щоб відводити тепло, еквівалентне витраченій роботі.
Процеси стиснення газу наочно можуть бути зображені на ентропійній, або тепловій, діаграмі Т - S (рис.).
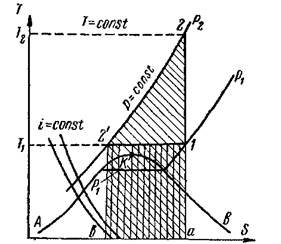
Рис. Діаграма Т – S процесу стиснення газу.
На осі ординат цієї діаграми відкладається абсолютна температура (Т), по осі абсцис - ентропія (S). Як відомо з термодинаміки, ентропія являє собою деяку функцію стану тіла, яка збільшується при підведенні до нього тепла, причому це збільшення тим менше, чим вище температура тіла.
На Т - S діаграмі нанесені лінії, відповідні постійному тиску (ізобари), і лінії, відповідні постійній температурі (ізотерми), які зображуються горизонтальними прямими. Лінія АКВ є прикордонною кривою. Область, що лежить нижче цієї кривої, відповідає вологому пару, гілка АК - рідини при температурі насичення, гілка КВ - сухому насиченому пару. Точка К є критичною точкою. Зліва від гілки АК знаходиться область рідини, праворуч від гілки КВ - область перегрітої пари. Так як випаровування і конденсація рідини протікають при постійних температурах і тиску, то в області вологої пари ізобари співпадають з ізотермами. Конденсація суміші вологих парів протікає при змінній температурі, тому в таких випадках ізобари в області вологої пари не збігаються з ізотермами.
Процеси стиснення газу в компресорі зображуються на діаграмі Т-S наступним чином. При адіабатичному стисненні q = 0, отже за формулою (7-31) Д5 = 0, т. Е. Процес йде без зміни ентропії (S = const). Тому процес зображується вертикальною лінією 1-2, причому точка 1 характеризує стан газу до стиснення і лежить на перетині ізобари pi і ізотерми Ti; точка 2 відповідає
 2015-09-06
2015-09-06 2506
2506







