Организационный момент.
Приветствие учащихся, проверка отсутствующих.
Целеполагание и мотивация деятельности
Сегодня на уроке мы будем повторять, закреплять и обобщать знания по теме «Белки».
На доске эпиграф:
«Задача выполнена, если химическая сторона мира вошла в круг наших понятий».
Мы ответим на устные задания, решим качественные задачи, генетическую цепочку и самостоятельную работу, что направит нас понимание значимости химических знаний для правильного понимания жизненных приоритетов.
Перед изучением нового материала демонстрируем вопрос на экране:
В организме человека и животного белки под влиянием (А) подвергаются (Б), в результате образуются (В), которые используются организмом для синтеза собственных специфических (Г).
(Ответ учащиеся дают после изучения нового материала)
Задаю вопросы (фронтальный опрос):
· Какие органические соединения называются белками?
· Почему белки – высокомолекулярные соединения?
Белки — высокомолекулярные соединения, образующиеся в результате связывания отдельных полипептидных цепей водородными связями. Все белки подразделяются на глобулярные (растворимы в воде) и фибриллярные (нерастворимы в воде). Глобулярные белки компактны, обладают сферической и приближенными к ней формами. Глобулярный белок диаметром 2,5 нм представляет собой полипептидную цепь длиной до 50 нм, свернутую в клубок. Фибриллярные белки обычно вытянуты и входят в состав тканей, мышц, волос.
· Какие химические элементы входят в состав белка?
В состав белка входят: углерод, водород, кислород, азот, сера, фосфор, железо.
· Охарактеризуйте строение белковой молекулы.
Строение белковой молекулы:
- Первичная – образована пептидными связями"
- Вторичная – образована водородными связями"
- Третичная – образована дисульфидными, сложноэфирными, солевыми мостиками"
- Четвертичная – гемоглобин. (комплекс из четырёх макромолекул)
Что необходимо сделать, чтобы получить четвертичную структуру? Ученики объединяются в группы, моделируя молекулы гемоглобина и хлорофилла. Вы сейчас разошлись на свои места. Что случилось с вашей белковой молекулой? (Распалась). Верно, это момент начала процесса денатурации, во время которого происходит разрушение структур белка. Ученики по группам моделируют процесс денатурации: 1 группа - разрушает третичную структуру, 2 группа - разрушает вторичную структуру. Наблюдали ли вы в жизни процессы денатурации белков?
Денатурация белка может происходить под влиянием различных факторов: температуры, кислоты, щелочи, солей и т.д.
Чем выше уровень организации белковой молекулы, тем структура мене прочна.
Нарушение нативной (естественной), уникальной (свойственной только этому белку) структуры белковой молекулы называют денатурацией.
Денатурация может быть вызвана изменением температуры, обезвоживанием, облучением рентгеновскими лучами и другими воздействиями. Вначале разрушается самая слабая структура – четвертичная, затем третичная, вторичная и при наиболее жестких условиях – первичная.
Если при изменении условий среды первичная структура молекулы белка остаётся неизменной, то при восстановлении нормальных условий среды полностью восстанавливается и структура белка.
Процесс восстановления структуры белка называется ренатурацией.
Это свойство белков широко используется в медицинской и пищевой промышленности для приготовления медицинских препаратов, например вакцин и сывороток, для получения пищевых концентратов, сохраняющих в высушенном виде свои питательные функции.
Рассмотрим химические свойства белков
Химические свойства рассматриваются с опорой на строение белков (учитель демонстрирует на столе, учащиеся каждый на своем рабочем месте, результаты учащиеся заносят в таблицу).
| «Химические свойства белков» | |||
| Название опыта | Что делал | Что наблюдал | Объяснение и выводы |
| 1. Денатурация белка. | В пробирку № 1 с раствором белка добавили этанол неразбавленный. В пробирку № 2 с раствором белка добавили соль железа. Пробирку № 3 с раствором белка нагреть. | Во всех трех случаях наблюдается необратимое свертывание белка — денатурация. | При нагревании, действии неразбавленного спирта, солей тяжелых металлов происходит разрушение вторичной и третичной структуры, с сохранением первичной. |
| 2) Биуретовая реакция. | К 2 мл раствора белка добавить раствор сульфата меди (II) и щелочи. | Красно-фиолетовое окрашивание. | При взаимодействии растворов образуется комплексное соединение между ионами Си2+ и полипептидами. |
| 3) Ксантопротеиновая реакция. | К 2 мл раствора белка добавить по каплям концентрирующуюся азотную кислоту. | Желтое окрашивание. | Реакция доказывает, что в состав белков входят остатки ароматических аминокислот. |
3. Гидролиз белков — разрушение первичной структуры в кислом или щелочном растворе с образованием аминокислот.
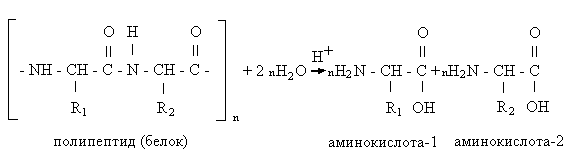
4. Горение белков – с образованием азота, углекислого газа, воды
Вопросы:
Какой процесс происходит при нагревании белка?
Какой химической реакцией можно определить наличие белка в молоке?
Подведение итогов и выставление отметок:
Возвращаемся к вопросу, заданному в начале урока:
А — фермент
Б — гидрому
В — a — аминокислота
Г — белки
Дети делают вывод
- Закрепление пройденного материала
Напишите уравнение реакций, с помощью которых можно осуществить следующие превращения:
Этан 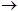 этиловый спирт
этиловый спирт 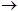 уксусный альдегид
уксусный альдегид 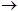 уксусная кислота хлоруксусная кислота
уксусная кислота хлоруксусная кислота 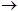 аминоуксусная кислота
аминоуксусная кислота 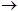 полипептид.:
полипептид.:
С2Н6 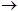 С2Н5Сl
С2Н5Сl 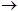 С2Н5ОН
С2Н5ОН 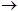 СН3СОН
СН3СОН 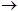 СН3СООН
СН3СООН 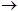 Сl-СН2СООН
Сl-СН2СООН 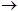 NH2- СН2СООН
NH2- СН2СООН 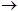 NH2 -СН2 - СО - NH( пептидная группа (связь)) - СН2СООН
NH2 -СН2 - СО - NH( пептидная группа (связь)) - СН2СООН
- С2Н6 + Cl2
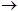 С2Н5Сl +НСl
С2Н5Сl +НСl - С2Н5Сl + НОН
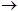 С2Н5ОН + НСl
С2Н5ОН + НСl - С2Н5ОН + О
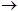 СН3СОН + НОН
СН3СОН + НОН - СН3СОН + Ag2O
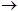 СН3СООН + 2 Ag
СН3СООН + 2 Ag 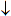
- СН3СООН + Cl2
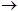 Сl-СН2СООН + НСl
Сl-СН2СООН + НСl - Сl-СН2СООН + NH3
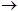 NH2- СН2СООН + НСl
NH2- СН2СООН + НСl - 2 NH2- СН2СООН
 NH2 -СН2 - СО - NH (дипептид) - СН2СООН
NH2 -СН2 - СО - NH (дипептид) - СН2СООН
 2015-10-16
2015-10-16 1040
1040







