Потенціал Z системи характеризує здатність системи виконати корисну роботу (передати у зовнішнє середовище термічну, механічну, хімічну або іншу енергію). При цьому термодинамічний потенціал Z системи зменшиться. В умовах рівноваги Z=const. Окрім того, при стабільній рівновазі, термодинамічний потенціал прагне до абсолютного мінімуму, а при метастабільній рівновазі – до відносного мінімуму.
Наприклад, для суто механічної системи – шару, що котиться по нерівній поверхні, термодинамічним потенціалом Z є потенціальна енергія шару. При зміні положення центру маси шару по висоті на 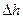 зміна термодинамічного потенціалу системи:
зміна термодинамічного потенціалу системи:
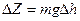 (4)
(4)
де m – маса шару; g – прискорення сили тяжіння.
В термодинамічних системах, що застосовані в металургійному виробництві, взаємно перетворюються декілька видів енергії: механічна, термічна, хімічна і ін. Це обумовлює ускладнення поняття термодинамічного потенціалу у порівнянні з розглянутим прикладом суто механічної системи.
Розглянемо докладніше, якими енергетичними параметрами буде характеризуватися термодинамічний потенціал при різній ступені ізоляції системи.
Термічна і механічна ізоляція (замкнута система): V=const; S=const. Підвищення температури супроводжується підвищенням тиску. Термодинамічний потенціал визначається рівнем накопичених усередині системи усіх видів енергії і носить назву внутрішньої енергії U:
U = f(S, V); dU = TdS - pdV (5)
Тільки термічна ізоляція системи. Підвищення температури супроводжується збільшенням об’єму. Термодинамічним потенціалом системи є тепловміст (ентальпія) H:
H = f(S, p) = U + pV; dH = TdS + Vdp (6)
Тільки механічна ізоляція системи. Виконана усередині робота (наприклад, вибух заряду) викличе підвищення тиску, але не температури. Термодинамічний потенціал у цьому випадку буде відрізнятися від U на величину TS. Він називається "вільна енергія Гельмгольця", або ізотермно-ізохорний потенціал:
F = f(T, V) =U - TS; dF = - SdT - pdV (7)
Системa відкрита (немає ні механічної, ні термічної ізоляції). Термічним потенціалом у цьому випадку виступає "вільна енергія Гіббса", або ізотермно-ізобарний потенціал:
G = f(T, p) = U + pV – TS = H - TS; dG= - SdT + Vdp (8)
Оскільки, згідно другого початку термодинаміки, в ізотермно-ізобарних системах повинно виконуватися рівняння 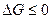 , то реакції і процеси у них можуть відбуватися за умови:
, то реакції і процеси у них можуть відбуватися за умови:
0< 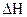 <TS; - TS < Q < 0 (9)
<TS; - TS < Q < 0 (9)
де Q = - 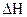 (теплота реакції).
(теплота реакції).
В металургійних конденсованих системах різниця між F і G:
G = F - pV (10)
є невеликою, тому що питомий об’єм конденсованих фаз є невеликим. Ще меншою є різниця між 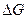 та
та 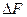 , тому що зміна об’єму при кристалізації і твердофазних перетвореннях зазвичай не перевищує декількох відсотків. Тому параметри G і F часто не розрізняють, називаючи і один і інший вільною енергією, і позначають загальним символом Z.
, тому що зміна об’єму при кристалізації і твердофазних перетвореннях зазвичай не перевищує декількох відсотків. Тому параметри G і F часто не розрізняють, називаючи і один і інший вільною енергією, і позначають загальним символом Z.
Вільна енергія є величиною екстенсивною. У фізичній хімії її зручно приводити до одного молю речовини:
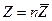 (11)
(11)
де n – число молей; 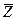 - мольна вільна енергія.
- мольна вільна енергія.
 2015-10-13
2015-10-13 854
854








