Хімічним потенціалом i-компоненту 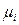 Дж. Гіббс назвав похідну
Дж. Гіббс назвав похідну
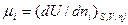 , (12)
, (12)
де S, V, nj – незалежні перемінні: відповідно ентропія, об’єм, число молей компонентів.
Щоб більш наглядно уявити собі сенс хімічного потенціалу атомів і-компоненту, врахуємо, що згідно першої фундаментальної термодинамічної теореми для відкритих систем, повний диференціал внутрішньої енергії для випадку, коли незалежними перемінними є S, V і nj,
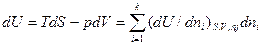 (13)
(13)
У цьому рівнянні усі три похідні внутрішньої енергії по незалежних параметрах є узагальненими силами, або факторами інтенсивності. Іншими словами, 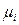 у (12) є фактором інтенсивності, що визначає процес перерозподілу числа молей компонентів у системі. Таким чином, хімічний потенціал при перерозподілі мас компонентів між фазами при фазовому переході відіграє таку саму роль, що і тиск при зміні об’єму або температура у процесі теплообміну.
у (12) є фактором інтенсивності, що визначає процес перерозподілу числа молей компонентів у системі. Таким чином, хімічний потенціал при перерозподілі мас компонентів між фазами при фазовому переході відіграє таку саму роль, що і тиск при зміні об’єму або температура у процесі теплообміну.
 2015-10-13
2015-10-13 346
346








