Кристаллизация может осуществляться как в целях получения кристаллической фазы из растворов и расплавов, так и в целях разделения смесей. Разделение смесей методом кристаллизации основано на обогащении или обеднении жидкой и кристаллической фаз по целевым компонентам при проведении однократной или многократной частичной кристаллизации. Рассмотрим кристаллизационное разделение растворов на примере системы, состоящей из растворителя и двух растворенных разделяемых веществ.
По физическому смыслу методы разделения смесей при их частичной кристаллизации аналогичны методам перегонки, когда система пар-жидкость и процессы частичной конденсации и испарения аналогичны системе жидкость - кристаллы и процессам частичной кристаллизации и растворения. По аналогии с перегонкой отношение концентраций в равновесных кристаллической и жидкой фазах (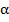 ) называют коэффициентом разделения:
) называют коэффициентом разделения:
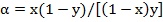 (23.15)
(23.15)
В отличие от перегонки целевой компонент чаще концентрируется в фазе x (твердой фазе), поэтому коэффициент разделения при кристаллизации является обратной величиной по отношению к коэффициенту разделения (относительной летучести) при перегонке.
Коэффициент разделения показывает, насколько целевой компонент сконцентрирован в кристаллической фазе по отношению к жидкой. В случае глубокой очистки, когда х 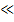 1 и у
1 и у 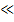 1 являются концентрациями примеси в твердой и жидкой фазах, выражение для коэффициента разделения упрощается, и а = х/у. При а > 1 примесь будет концентрироваться в выпадающих кристаллах, при а<1 содержание примеси будет увеличиваться в маточном растворе.
1 являются концентрациями примеси в твердой и жидкой фазах, выражение для коэффициента разделения упрощается, и а = х/у. При а > 1 примесь будет концентрироваться в выпадающих кристаллах, при а<1 содержание примеси будет увеличиваться в маточном растворе.
Будем в первом приближении считать процесс кристаллизации равновесным с постоянным во времени коэффициентом разделения 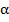 . Принимая исходное количество раствораGн, конечное количество образовавшихся кристаллов Gт.к и количество маточного раствора GK, получим:
. Принимая исходное количество раствораGн, конечное количество образовавшихся кристаллов Gт.к и количество маточного раствора GK, получим:
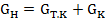 (23.16)
(23.16) 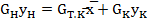 (23.17)
(23.17)
где 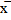 средняя концентрация примеси в кристаллах.
средняя концентрация примеси в кристаллах.
Полученная система уравнений содержит три неизвестных: 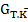 ,
, 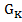 ,
, 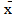 или
или 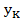 . Для замыкания рассматриваемой системы уравнений составим материальный баланс для бесконечно малого промежутка времени процесса кристаллизации. Обозначим
. Для замыкания рассматриваемой системы уравнений составим материальный баланс для бесконечно малого промежутка времени процесса кристаллизации. Обозначим 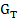 и
и 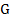 как количество кристаллической и жидкой фаз в текущий момент времени, а y и x- в качестве текущих жидкой и твердой фаз.
как количество кристаллической и жидкой фаз в текущий момент времени, а y и x- в качестве текущих жидкой и твердой фаз.
За бесконечно малое время изменение количества примеси в жидкой фазе будет равно –d(yG). За этот промежуток времени в кристаллическую фазу уйдет xdGT примеси. Приравняв изменение количества примеси в фазах, получим 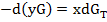
Поскольку -dG = 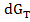 , получим
, получим
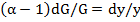 (23.18)
(23.18)
Решая дифференциальное уравнение (23.18) при G=GH,y=yH, 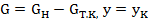 , получим:
, получим:
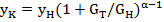 (23.19)
(23.19)
Для любого текущего момента времени последнее выражение
запишется так:
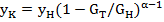 (23.20)
(23.20)
Решение системы уравнений (23.16), (23.17) и (23.19) позволяет определить количество жидкой и твердой фаз 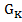 и
и 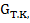 и их концентрации
и их концентрации 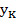 или
или 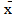 . В частности, среднее содержание примеси в кристаллах определяется таким образом:
. В частности, среднее содержание примеси в кристаллах определяется таким образом:
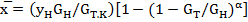 (23.21)
(23.21)
С учетом этого выражения получим среднее значение коэффициента разделения
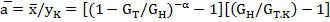 (23.22)
(23.22)
Следует подчеркнуть, что данная методика расчета применима лишь к равновесной кристаллизации при бесконечно большой скорости переноса вещества к поверхности раздела фаз. Поскольку скорость реального процесса кристаллизации конечна, то в этом случае коэффициент разделения связывает составы неравновесных фаз и таким образом становится функцией кинетических параметров массообмена.
Соотношение между коэффициентом разделения (коэффициентом распределения), связывающим равновесные составы фаз (± а), и коэффициентом разделения в неравновесном процессе (±аН) может быть найдено из материального баланса массопереноса в диффузионном пограничном слое у поверхности кристаллической фазы (рис. 23-4).
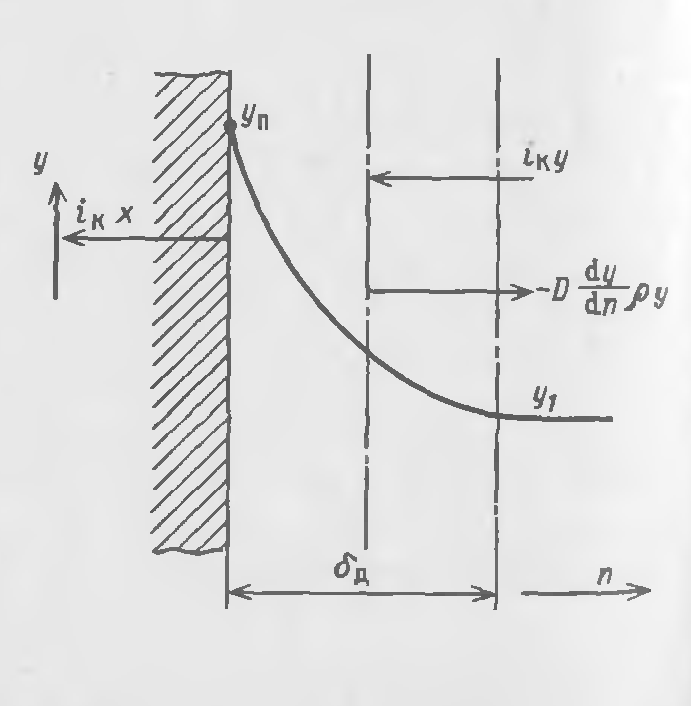
Рис. 23-4. Схема переноса вещества в пограничном слое.
На рис.23-4 iк- плотность потока массы кристаллизующегося вещества;yп- концентрация примесинаповерхностиразделафаз;у1 -концентрация примеси в ядре жидкой фазы; y –концентрация примеси в произвольном сечении диффузионного слоя; ρy-плотность примеси. Плотность потока массы примеси к поверхности раздела фаз ±iK y делится на два потока: массу вещества примеси, переходящего в кристаллы iK х, и массу вещества, уходящего за счет диффузии в область более низкой концентрации - 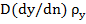 (принято, что избыток массы примеси и, соответственно, ее более высокая концентрация у поверхности кристаллической фазы создаются при условии низких значений коэффициента разделения, т.е. при а < 1).
(принято, что избыток массы примеси и, соответственно, ее более высокая концентрация у поверхности кристаллической фазы создаются при условии низких значений коэффициента разделения, т.е. при а < 1).
Исходя из принятых допущений, получим
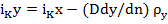
Или
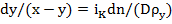
с граничными условиями
n = 0, у=уП и n= 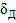 , y=y1
, y=y1
После интегрирования будем иметь
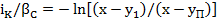 (23.23)
(23.23)
где 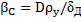 - коэффициент внешней массоотдачи, кг/(м2-с).
- коэффициент внешней массоотдачи, кг/(м2-с).
Поскольку 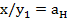 (неравновесный коэффициент разделения),
(неравновесный коэффициент разделения),
а 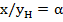 (равновесный коэффициент разделения), уравнение (23.23)
(равновесный коэффициент разделения), уравнение (23.23)
может быть записано в форме, связывающей эти два коэффициента:
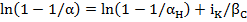 (23.24)
(23.24)
Из уравнений (23.23) и (23.24) видно, что при малых концентрациях примеси (при у<<1) 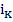 и
и 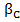 практически не зависят от у а
практически не зависят от у а 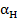
также не зависит от концентрации примеси в жидкости, если а = const. Это позволяет использовать уравнения (23.16)—(23.22) для расчета количеств образующегося маточного раствора и кристаллов, а также концентраций фаз при условии замены 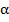 на
на 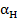 .
.
Кристаллизационное разделение смесей обычно проводят многократной перекристаллизацией, поскольку степень разделения при однократной кристаллизации невелика в результате увеличения содержания маточного раствора в трещинах кристаллов, адсорбционного поглощения примеси поверхностью кристаллов и других причин перекристаллизация, повторенная многократно, позволяет достичь высокой степени разделения. При многократной перекристаллизации используют методы последовательного фракционирования, противоточную кристаллизацию и ряд других.
Последовательное фракционирование осуществляется методом фракционной (дробной) кристаллизации, в котором каждая образующаяся фракция в свою очередь делится на две последующие фракции. Исходный раствор дает на первой ступени две фракции: кристаллическую фазу и маточный раствор; каждая из полученных фракций на второй ступени, в свою очередь, образует две фракции, и т.д. (рис. 23-5).
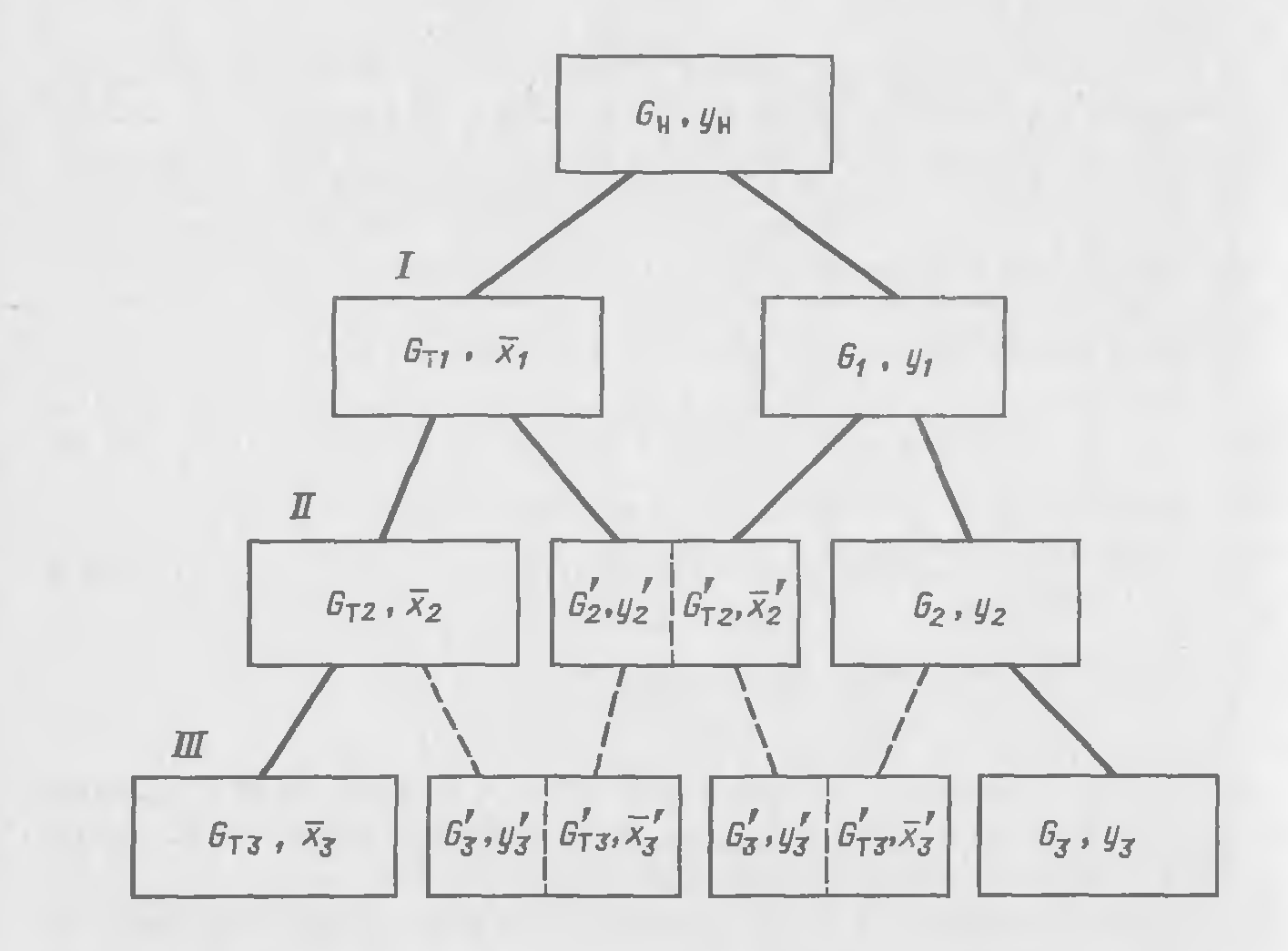
Рис. 23-5. Схема фракционной кристаллизации (/-/// ступени)
Число ступеней разделения выбирают в соответствии с требуемой степенью очистки. Для каждой ступени разделения можно записать систему уравнений материального баланса (23.16), (23.17),(23.19) и (23.22). Наиболее рациональный вариант проведения фракционной кристаллизации требует равенства соотношения количеств твердой и жидкой фаз, образующихся на каждой ступени:
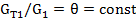
С учетом этого из системы уравнений материального баланса, записанных для каждой ступени, можно получить выражение для концентрации примеси в кристаллах после n-й ступени при условии постоянства коэффициента разделения:
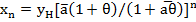 (23.25)
(23.25)
В случае, если а<1, получают очищенную кристаллическую фазу (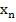 -мало), в противоположном случае, т.е. при а> 1, получают очищенный маточный раствор (
-мало), в противоположном случае, т.е. при а> 1, получают очищенный маточный раствор (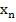 -велико).
-велико).
Метод фракционной кристаллизации обеспечивает высокую степень очистки, но отличается малой производительностью и высокой трудоемкостью ввиду сложности технологического осуществления его многочисленных стадий: кристаллизации, сепарации кристаллов, перемешивания кристаллов с растворителем, перемешивания промежуточных фракций, выпаривания маточных растворов.
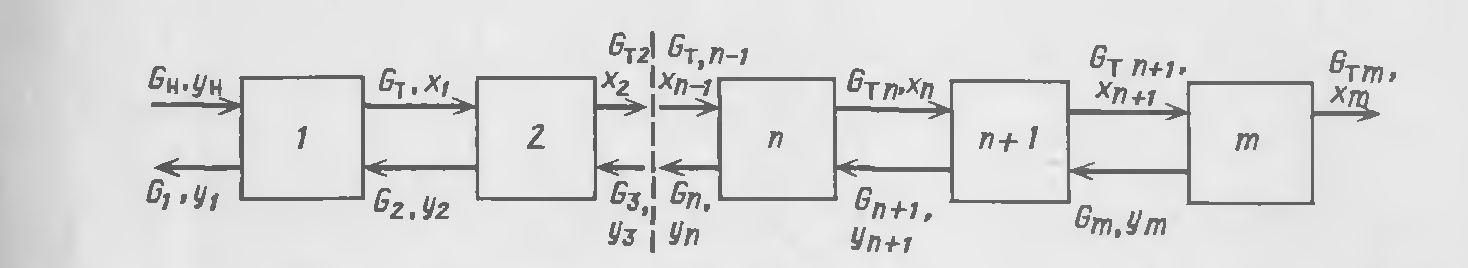
Рис. 23-6. Схема материальных потоков противоточной многоступенчатой кристаллизации
Менее трудоемким и более производительным процессом является противоточная многоступенчатая кристаллизация. Связь достигаемых концентраций в кристаллической и жидкой фазах при противоточной многоступенчатой кристаллизации с числом ступеней m может быть получена из материального баланса (рис. 23-6).
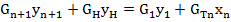
Примем расходы фаз и коэффициент разделения постоянными в каждой ступени:
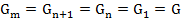
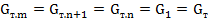
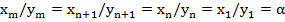
Примем также, что фазы, покидающие ступени кристаллизации, находятся в равновесии (в этом случае ступень является теоретической ступенью изменения концентрации).
С учетом сделанных допущений уравнение материального баланса будет выглядеть так:
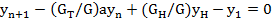 (23.26)
(23.26)
Общее решение полученного уравнения в конечных разностях имеет вид
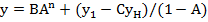 (23.27)
(23.27)
где В константа;
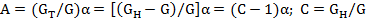
Константа В может быть найдена из граничного условия n = О, 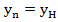 :
:
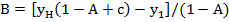
Концентрация жидкости, выходящей из последней ступени, будет определяться следующим образом:
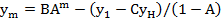 (23.28)
(23.28)
Концентрация примеси в жидкости, выходящей из последней ступени установки, будет вычисляться по формуле
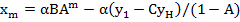 (23.29)
(23.29)
Из уравнения (23.29) найдем число теоретических ступеней изменения концентраций:
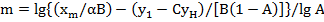 (23.30)
(23.30)
Число действительных ступеней изменения концентраций mД находят с учетом коэффициента полезного действия ступени Е, определяемого экспериментально:
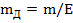 (23.31)
(23.31)
 2015-10-14
2015-10-14 3221
3221
