ТД-параметр состояния системы при бесконечно малом изменении называют энтропией.
Δs = ΔQ / T 49
где: Δs — изменение энтропии, Дж /(кг·К); ΔQ — изменение теплоты в процессе.
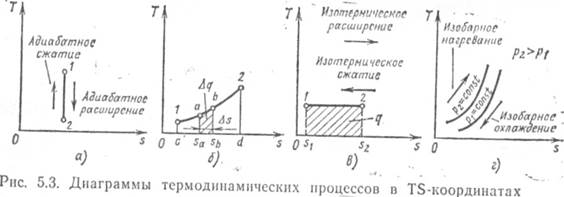
Из 49 следует, что если энтропия в каком то процессе возрастает, то к телу подводится теплота, если уменьшается — теплота отводится. Отсюда следует, что обратимый диабатный процесс - это процесс при постоянной энтропии (рис 5.3, а) Рис 5.3, б — произвольный обратимый процесс 1-2 в Ts диаграмме. Выделим из него бесконечно малый участок а-б, в котором температура практически не меняется. Изменение энтропии обозначим Δs = sа — sб.
Тогда из 49 теплоту можно подсчитать просуммировав все участки. Изотермический процесс (рис 5.3, в) изображают на Ts-диаграмме горизонтальной линией, а его теплоту площадью под кривой:
Q = T(s2 — s1) 50
Процесс 1-2, сопровождающийся подводом теплоты, т.к энтропия возрастает, - то это изотермическое расширение; процесс 2-1 — изотермическое сжатие, сопровождается отводом теплоты. Рис 5.3, г — при изобарном нагреве газа произходит подвод теплоты и энтропия возрастает.
Для обратимого бесконечно малого теплового процесса (с бесконечно малыми изменениями параметров) теплота может быть выражена через изменение энтропии ΔQ = TΔs 51
Учитывая 49, получим обобщенное выражение второго закона ТД: ΔQ ≤ TΔs 52
Для изолированной системы, в которой происходят произвольные процессы, в т.ч и необратимые, так как подвод и отвод теплоты отсутствует, т. е. Q = 0, то Δs > 0 и s2 > s1. Это означает, что энтропия изолированной системы, в которой происходят необратимые процессы, стремится к максимуму, который достигается при выравнивании температуры в этой системе.
Литература:
- Лепешкин а. В., Гидравлические и пневматические системы. Главы 1 и 2.
- Столбов Л. С., Основы гидравлики и гидропривод станков. Главы 1 и 2;
3. Егорушкин В. Е., Основы гидравлики и теплотехники Глава 1, §1 и 2.
 2015-10-14
2015-10-14 494
494







