Двух функциональных групп
| по количеству -ОН групп, включая и входящую в -СООН, бывают двух- и многоатомными | по количеству -СООН групп бывают одно- и многоосновными | бывают a-,.b-, g- и т.д. гидроксикислотами |
Виды изомерии: структурная – по положению 2-й функциональной ОН – группы относительно – СООН; стереоизомерия (энантиомерия, диастереомерия)
Химические свойства
I Гидроксикислоты проявляют общие свойства спиртов и кислот. В зависимости от реагентов и условий проведения реакций взаимодействует ОН или -СООН группа или обе одновременно. Как кислоты они более сильны, чем соответствующие карбоновые кислоты (сказывается –I эффект ОН- группы).
П. Гидроксикислоты проявляют специфические свойства, которые обусловлены взаимным влиянием ОН- и СООН- групп.
1. Например, своеобразная реакция отщепления воды при нагревании.
Она позволяет отличить a-, b-, g- и другие гидроксикислоты.
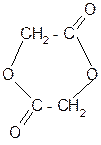
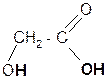 а)
а)
a t°

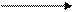
гидролиз + 2H2O
+ H+ или OH-
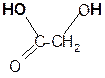
a лактиды
(циклические
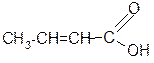
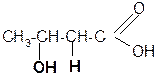 сложные эфиры)
сложные эфиры)
б) b a t°

-H2O
b -оксимасляная кротоновая кислота
кислота
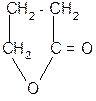 в) b a t°
в) b a t°
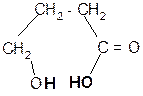
 + H2O
+ H2O
гидролиз
g H+
g-гидроксимасляная g - бутиролактон
кислота (ГОМК)
ГОМК обладает наркотическим действием, нетоксична, применяется в виде натриевой соли как снотворное средство и при неингаляционном наркозе при операциях.
г)
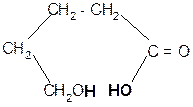
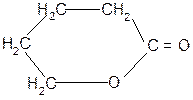 b a
b a
t°
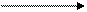
 g + H2O
g + H2O
гидролиз
H+
d
d-гидроксивалериановая d - валеролактон
лактон
Лактиды и лактоны могут гидролизоваться в кислой среде с образованием исходных гидроксикислот.
2. Разложение a-гидроксикислот при нагревании в присутствии H2SO4:
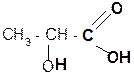 |
a t°, H2SO4
 CH3–CHO + HCOOH
CH3–CHO + HCOOH
Многоосновные кислоты ведут себя так же. Например,
а) при нагревании лимонная кислота будет вести себя как b-гидроксикислоты:
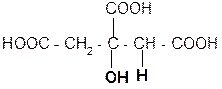 | |||
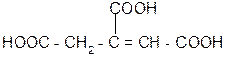 | |||
t°


-Н2О
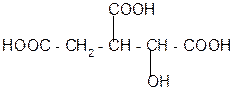 лимонная кислота цис-аконитовая к-та
лимонная кислота цис-аконитовая к-та
+ Н2О

против правила
Марковникова
изолимонная кислота
б) при действии H2SO4 и нагревании она ведет себя как a-гидроксикислота, т.е. разлагается с выделением муравьиной кислоты:
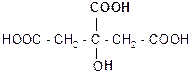
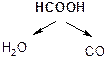
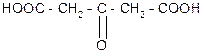 t°, H2SO4
t°, H2SO4
 +
+
ацетондикарбоновая




 кислота
кислота
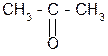 2СO2 +
2СO2 +
Таблица 1
 2015-10-22
2015-10-22 493
493








