| Формула | Тривиальное название | ИЮПАК – номенклатура | Местонахождение в природе и биологическая роль |
 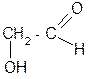 | Гликолевый, или гидроксиуксусный альдегид | 2– гидроксиэтаналь | Предшественник гликолевой кислоты |
| Глицериновый альдегид | 2,3–дигидрокси-пропаналь | Стандарт конфигурации всех «хиральных» соединений: гидрокси- и аминокислот, углеводов и др. | |
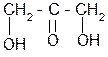 | Дигидроксиацетон | 1,3 – дигидрокси-2-пропанон | В виде фосфорно-кислого эфира встречается как промежуточный продукт при окислении глюкозы в организме |
 Продолжение таблицы 2
Продолжение таблицы 2
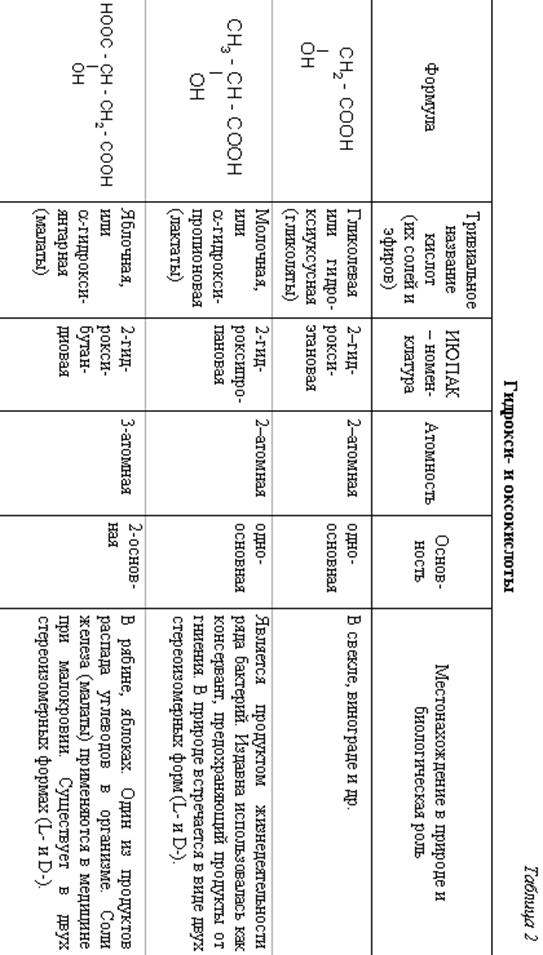
| Формула | Тривиальное Название кислот (их солей и эфиров) | ИЮПАК-номенклатура | Атомность | Основность | Местонахождение в природе и биологическая роль |
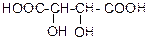 | Винная (виноградная), или a,b-дигидрокси янтарная кислота (тартраты) | 2,3-дигидрокси бутандиовая кислота | 4-х атомная | 2х основная | Содержится в виноградном соке. Является продуктом жизнедеятельности бактерий. Применяется как консервант в пищевой промышленности, в красильном деле. Соли (тартраты) применяются в радиотехнике (пьезокристаллы) и в биохимическом анализе в виде Фелинговой жидкости для обнаружения альдегидов. Существует в трех стереоизомерных формах (L-, D- и мезо-) |
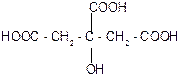 | Лимонная, или b-гидрокси-b-карбокси-глутаровая (цитраты) | 3-гидрокси-3-карбоксипентан диовая | 4-х атомная | 3-х основная | Содержится в лимонах, апельсинах, винограде, в листьях махорки. Играет важную роль в ЦТК. Соли (цитраты) применяются для консервирования донорской крови, соли железа – при малокровии. |
Оксокислоты
Наиболее важные природные оксокислоты представлены в Таблице 3
I. Они проявляют общие свойства, присущие альдегидам или кетонам и кислотам, но как кислоты они сильнее соответствующих карбоновых кислот (сказывается –I эффект карбонильной группы)
П Специфические свойства, обусловленные взаимным влиянием
>C=O и -COOH групп:
1. Расщепление a- и b- оксокислот при нагревании – декарбоксилирование:
 dˉ
dˉ
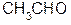 d+ d+ t°, H2SO4разб.
d+ d+ t°, H2SO4разб.
 а) + CO2
а) + CO2
dˉ
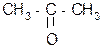 b t° комн.
b t° комн.
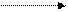
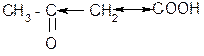 б) + CO2
б) + CO2
 2. Кето-енольная таутомерия b-оксокислот.
2. Кето-енольная таутомерия b-оксокислот.
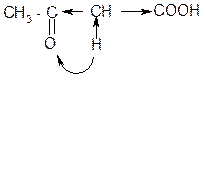 d+ a
d+ a
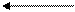

:
–d
кето-форма енольная форма
ацетоуксусная кислота (АУК)
Обе формы известны в свободном состоянии и могут быть при определенных условиях выделены. Однако они обе неустойчивы – легко превращаются в равновесную смесь с содержанием кето-формы (93%) и енольной (17%). Стойкость енола по сравнению с другими енольными формами возрастает из-за сопряжения.
Для доказательства существования обеих форм пользуются соответствующими реакциями. Например, как кетон АУК восстанавливается до вторичного спирта, реагирует с HCN, фенилгидразином и т.д. Как енол АУК или ее этиловый эфир (ацетоуксусный эфир) дает окрашивание при действии разбавленного водного раствора FeCl3 вследствие образования комплексной железной соли (хелата):
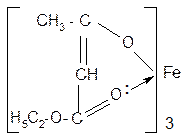 |
Таблица 3
Оксокислоты
| Формула | Тривиальное название кислот (их солей и эфиров) | ИЮПАК-номенклатура | Местонахождение в природе и биологическая роль |
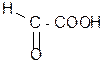 | Глиоксиловая, или формилму-равьиная (глиоксилаты) | 2-оксо-этановая | Это единственная a-альдегидо-кислота. Встречается в недозревших фруктах. |
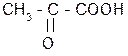 | Пировиноград-ная, ацетилму-равьиная (пируваты). | 2-оксо-пропановая | Ключевой промежуточный продукт при обмене веществ в организме |
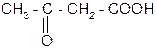 | Ацетоуксусная, b-оксомасляная (ацетоацетаты) | 3-оксобу-тановая | Образуется в процессе метаболизма высших жирных кислот и как продукт окисления b-оксимасляной кислоты, накапливается при сахарном диабете. |
 | Щавелевоуксус-ная, ЩУК (оксалоацетаты) | 2-оксобу-тандиовая | Образуется в ЦТК |
 | a-кетоглутаровая (a-кетоглутара-ты) | 2-оксопен-тандиовая | Образуется в ЦТК и является предшественником важнейших аминокислот: глутаминовой и g-амино-масляной (ГАМК) |
Стереоизомерия
Стереоизомеры отличаются друг от друга пространственным расположением атомов или групп атомов.
Стереоизомеры
 |  |
Энантиомеры Диастереомеры
(оптические,
или зеркальные,
изомеры)
Знание стереоизомерии очень важно для изучения строения природных соединений (биорегуляторов и лекарственных средств – гормонов, витаминов, антибиотиков), так как все они существуют в строго определенных пространственных формах и их биологическая активность тесно связана с пространственным строением.
Так, для построения белковой молекулы используется один вид энантиомеров – L– аминокислоты, а в классе углеводов большее распространение имеют D–сахара. Из двух энантиомерных форм гормона адреналина большей фармакологической активностью обладает D(-)–форма. Стереоспецифично протекают многие биохимические реакции, так как они катализируются ферментами – белковыми молекулами.
Приведем некоторые примеры значения диастереомерии.
Бутендиовая кислота существует в виде двух геометрических изомеров (цис- и транс-), но только один из них – фумаровая кислота (транс–изомер) – служит субстратом для действия фермента.
Ретинол с транс–расположением всех двойных связей более эффективен в процессах зрения, чем его цис–изомер.
В липиды клеточных мембран в качестве структурных составляющих входят также только цис-формы высших жирных кислот.
Энантиомерия осуществляется у так называемых «хиральных» молекул. Хиральными, или асимметрическими, молекулами называются те, которые не могут быть совмещены со своим зеркальным отражением; у них отсутствует плоскость симметрии:
 |



 | |
 | |
 |
Термин «хиральность» произошел от греческого слова «хиро» – рука.
Самым простым наглядным примером хиральных объектов являются правая и левая руки.
Атом углерод с четырьмя различными группами называется асимметрическим, или хиральным, центром.
Для изображения энантиомеров на плоскости используются проекционные формулы Фишера, называемые проекциями Фишера:
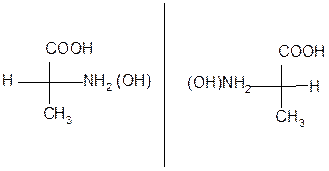 |
Энантиомеры
Относительная и абсолютная конфигурация. Определение абсолютной конфигурации стало возможным только с появлением современных физико-химических методов (рентгеноструктурного анализа) в 50-х годах. Однако нет необходимости устанавливать ее для каждого соединения. Можно охарактеризовать их путем сравнения конфигураций с абсолютной конфигурацией эталонных (ключевых) соединений, т. е. определить их относительную конфигурацию.
За такой эталон условно принят глицериновый альдегид, предложенный в 1906 г. Н.А. Розановым:
 | |||
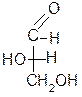 | |||

D- глицериновый L-глицериновый
альдегид альдегид
Считается, что все вещества, родственные глицериновому альдегиду по конфигурации хирального центра, т.е. с расположением групп – ОН, -NH2, - Hal справа, относятся к D–ряду, слева – к L– ряду.
Например:

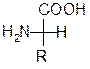
D - аминокислота L – аминокислота
Запомним, что D и L указывают на относительную конфигурацию молекулы. Познакомимся с некоторыми свойствами подобных молекул.
Хиральным соединениям свойственна способность вращать плоскость поляризованного света вправо (+) или влево (-), что называется оптической активностью. Отсюда и другое название энантиомеров – оптические изомеры.
Условиями оптической активности являются:
- Отсутствие плоскости симметрии (хиральность молекулы)
- Наличие в молекуле центров хиральности.
Мерой оптической активности является [a]D - удельное вращения; характеризует угол и направление вращения плоскости поляризованного света. Знак вращения (+) или (-) не связан с конфигурацией D и L и определяется только инструментально на приборе – поляриметре или сахариметре (для сахаров). Например,
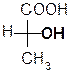
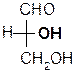
D(-) –молочная D(+)- глицериновый
кислота альдегид
Многие биологически важные вещества содержат в молекуле более одного центра хиральности. Подсчет числа стереоизомеров производится по формуле N= 2n, где n – число хиральных центров.
Представителем соединений с двумя центрами хиральности служит винная кислота. Рассмотрим этот пример подробнее.
У винной кислоты n=2, т.е. N= 22 = 4.
 |  | 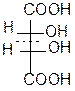 |  | ||||
1 2 3 4
1. D–винная кислота; 2. L-винная кислота; 3 и 4 – мезовинная кислота
1 и 2 – это энантиомеры (D и L). Они отличаются не по физическим и химическим свойствам, а только знаком вращения плоскости поляризованного света. Формулы 3 и 4 являются идентичными. Формулы 1 и 3, 2 и 3 являются пространственными изомерами, но не зеркальными, это диастереомеры. Они отличаются по физическим и химическим свойствам.
При отнесении энантиомеров к D– или L-ряду пользуются «оксикислотным ключом», т.е. сравнивают со стандартом тот хиральный центр, который остался без изменения при переходе от него. В данном случае это верхний хиральный центр (приведите путь превращения глицеринового альдегида в винную кислоту).
D– и L- энантиомеры проявляют оптическую активность. Мезовинная кислота – типичный пример молекулы, содержащей центры хиральности, но в целом являющейся ахиральной из-за наличия плоскости симметрии и потому не проявляющей оптическую активность.
Рацемат – это смесь равных количеств энантиомеров. Оптической активностью не обладает, вследствие компенсации вращения. Таким образом, у винной кислоты существуют 4 формы: 2 энантиомера (D- и L-), 1 мезо-форма и 1 рацемическая смесь. Рацемические смеси получаются синтетическим путем.
Поскольку природные источники не могут удовлетворить потребности современной биоорганической и биологической химии в разнообразных оптически активных соединениях, то либо расщепляют рацематы, либо ведут асимметрический синтез.
Существует несколько способов расщепления рацематов:
а) механический отбор кристаллов по их форме – исторически первый метод, примененный Луи Пастером;
б) биохимический (ферментативный) метод;
в) химический – через диастереомеры;
г) хроматографический на оптически активных сорбентах.
Глоссарий
Лактон – внутренний циклический сложный эфир, образующийся при нагревании g- и d-гидроксикислот.
Лактид – циклический сложный диэфир, образующийся при нагревании
a- гидроксикислот; имеет две сложноэфирные связи.
Ацетоуксусный эфир – этиловый эфир ацетоуксусной кислоты.
Таутомерия – явление существования в растворе равновесных изомерных форм, способных переходить в друг в друга; равновесная динамическая изомерия.
Кето-енольная таутомерия – равновесие между кетонной и енольной формами
Стереоизомеры – это изомеры, отличающиеся пространственным расположением атомов в молекуле.
Плоскость симметрии – это воображаемая плоскость, проходящая через молекулу или атом углерода с его заместителями и делящая молекулу на две симметричные части.
Оптическая активность – способность вещества вращать плоскость поляризованного света вправо или влево.
Хиральность – отсутствие плоскости симметрии, несовместимость со своим зеркальным изображением.
Энантиомеры – это стереоизомеры, молекулы которых относятся между собой как предмет и несовместимое с ним зеркальное изображение.
Диастереомеры – стереоизомеры, не являющиеся зеркальным отражением друг друга, обладающие различными физико-химическими свойствами.
Рацемическая смесь (рацемат) – эквимолярная смесь энантиомеров (1:1)
 2015-10-22
2015-10-22 3252
3252
