 Пьер Бугер – физик-оптик, мореход изучил поглощение света атмосферными и цветными стеклами. В 1729 г. он заметил, что если на тело направить световой поток I0, то вышедший поток света характеризуется интенсивностью It, меньшей, чем I0 (закон ослабления света).
Пьер Бугер – физик-оптик, мореход изучил поглощение света атмосферными и цветными стеклами. В 1729 г. он заметил, что если на тело направить световой поток I0, то вышедший поток света характеризуется интенсивностью It, меньшей, чем I0 (закон ослабления света).
I0 > It
l I0 = In + It + Ir
In = I0 – It= f (C, природы вещества, l).
I0 – интенсивность падающего света;
In – интенсивность поглощенного света;
It – интенсивность прошедшего света;
Ir – интенсивность рассеянного света.
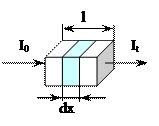 В 1760 г. Иоган Ламберт математически обосновал закон ослабления света и представил модель, подтвердив приоритет Бугера.
В 1760 г. Иоган Ламберт математически обосновал закон ослабления света и представил модель, подтвердив приоритет Бугера.
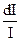 = – k∙dx = – k∙dx | В толщине поглощающей системы Ламберт предложил выделить малый участок dx. При прохождении через слой интенсивность I светового потока уменьшается на величину dI. (–) – уменьшение светового потока; k – коэффициент светопоглощения; |
Проинтегрируем по всей толщине l:
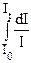 = – k
= – k 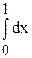
|
ln 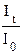 = – kl или
= – kl или
Закон Бугера-Ламберта: Слои равной толщины при прочих равных условиях поглощают равную долю падающего монохроматического излучения.
В 1852 г. Альберт Бер проверил справедливость закона Бугера-Ламберта для растворов и установил, что коэффициент светопоглощения зависит от концентрации:
k = k'с

ln 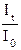 = – k'lс Объединенный закон Бугера-Ламберта-Бера: Количество электромагнитного излучения, поглощающееся раствором, пропорционально концентрации поглощающих частиц и толщине слоя.
= – k'lс Объединенный закон Бугера-Ламберта-Бера: Количество электромагнитного излучения, поглощающееся раствором, пропорционально концентрации поглощающих частиц и толщине слоя.
Закон применим в логарифмической форме, от экспоненциальной легко перейти к логарифмической.
It = I0·e – k'lС –экспоненциальная форма

 It = I0·10 – k'lC lg
It = I0·10 – k'lC lg 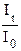 = – k'lс lg
= – k'lс lg 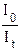 = k'lс
= k'lс
lg 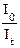 принято называть абсорбцией или оптической плотностью (А).
принято называть абсорбцией или оптической плотностью (А).

 А = lg
А = lg 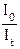 А = k'lс – логарифмическая форма основного закона светопоглощения
А = k'lс – логарифмическая форма основного закона светопоглощения
Графическая интерпретация основного закона светопоглощения
 |
Если в уравнении Бугера-Ламберта-Бера концентрация выражена в моль/дм 3, а толщина поглощающего слоя в см, то оно примет вид:
А = εCl,
где ε – молярный коэффициент светопоглощения; [ε] = 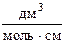 .
.
Молярный коэффициент светопоглощения – это мера чувствительности фотометрических методов. Чем больше ε, тем выше чувствительность метода, тем меньшую концентрацию вещества можно определить.
Факторы, влияющие на ε:
1. Природа вещества
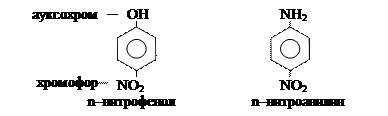
ε n–нитрофенола > ε n–нитроанилина
Если к раствору n–нитрофенола добавить органический растворитель – окраска усилится.
3. Природа фотометрического реагента. Фотометрический реагент (ФМР) – это реактив, который при взаимодействии с определяемым веществом образует окрашенное соединение. Например, при определении Cu 2+ в растворе фотометрическим реагентом является аммиак:
 Cu 2+ + 2NH4OH [Cu(NH3)2] 2+ + 2H2O
Cu 2+ + 2NH4OH [Cu(NH3)2] 2+ + 2H2O
4. рН раствора. ε может уменьшаться или увеличиваться (Например: чай с лимоном – ε уменьшается).
5. Длина волны (λ). Кривая распределения Гаусса описывает зависимость ε от λ и называется спектром поглощения раствора.
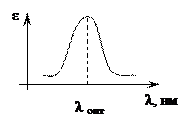 |
6. Температура.
Молярный коэффициент светопоглощения не зависит от концентрации и толщины поглощающего слоя.
Физический смысл ε: если с = 1 моль/дм 3, а толщина слоя l = 1 см, то ε = А.
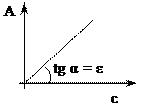 | Графический смысл ε состоит в том, что ε = tg α (α – угол наклона градуировочного графика). Чем α больше, тем более чувствителен метод. |
Закон аддитивности
Основной закон светопоглощения, описывающий поглощение смесью веществ называется законом аддитивности:
Если через систему, содержащую несколько окрашенных частиц различного сорта, пропустить электромагнитное излучение, то оптическая плотность, есть сумма оптических плотностей растворов индивидуальных веществ:
А 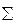 =
= 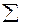 А1 + А 2 + … + Аn или
А1 + А 2 + … + Аn или
А 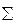 = l
= l 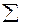 (ε1 С1 + ε2 С2 +…+ ε n С n), при l = const
(ε1 С1 + ε2 С2 +…+ ε n С n), при l = const
Аппаратура метода
Все приборы МАС имеют несколько основных узлов, функции которых одинаковы, несмотря на разнообразие схем.

Рис. 3. Принципиальная схема спектральных приборов: 1 – источник света; 2 – система выделения спектра; 3 – кювета с анализируемым раствором; 4 – система регистрации аналитического сигнала (фотоэлемент и микроамперметр).
В табл. 5 приведена сравнительная характеристика спектральных приборов, работающих в видимой, ультрафиолетовой и инфракрасной областях спектра.
Таблица 5
Сравнительная характеристика спектральных приборов
| Характеристика | УФ-спектро- фотометр | Фотоэлектроколориметр | ИК-спектрофотометр |
| Область спектра, нм | 200–400 | 400–760 | 760–2500 |
| Аналитическая форма вещества | Бесцветные истинные растворы | Окрашенные истинные растворы | Бесцветные безводные истинные растворы |
| Источник излучения | Ртутно-кварце-вая или водородная лампа | Вольфрамовая лампа Лампа Нернста | |
| Система монохроматизации света | Призмы из кварца, дифракционные решетки(Dl=0,5–2 нм) | Светофильтр (D l = 50 нм) | Призмы из NaCl, LiF, KI; дифракционные решетки(Dl= 0,5–2 нм) |
| Система регистрации аналитического сигнала | Фотоэлементы с внешним фотоэффектом, фотоумножители | Фоторезистор, термопара, приемник Голея | |
| Оптика (кюветы, линзы и т.д.) | Кварцевое стекло | Силикатное стекло | Монокристаллы NaCl, LiF, KI |
| Представители | СФ-26, СФ-46 | КФК-2ПМ, ФЭК-56 | ИКС-14, ИКС-24 |
 2015-10-22
2015-10-22 10908
10908








