Атомы в процессе химического взаимодействия могут переходить в возбужденное состояние. При этом появляется дополнительное число неспаренных электронов и атом может образовать большее число связей. Например, углерод в основном состоянии двухвалентен; при переходе в возбужденное состояние он – четырехвалентен (один электрон с 2s подуровня переходит на 2р подуровень: 
Исходя из того, что в возбужденном состоянии у атома углерода на внешнем уровне один s-электрон и три р-электрона, можно было бы ожидать, что характеристики одной связи будут отличаться от других. Однако, все четыре связи(в молекуле метана, например) равноценны. Для устранения этого противоречия была выдвинута идея о гибридизации атомных орбиталей – изменении, а точнее выравнивании, их формы и энергии. Основные принципы, определяющие процесс гибридизации:
1. Атомные орбитали участвующие в процессе гибридизации должны иметь близкие значения энергии.
2. Число гибридных орбиталей должно быть равно числу исходных классических атомных орбиталей.
3. Гибридные орбитали представляют собой линейные комбинации исходных орбиталей.
4. Гибридные орбитали располагаются в пространстве так, чтобы обеспечить между ними минимальное отталкивание.
Основные типы гибридных облаков sp3-,sp2-, sp-. Формы гибридных облаков приведены на рис. 5.

а)Образование sp3-гибридного облака

б)Образование sp2-гибридного облака
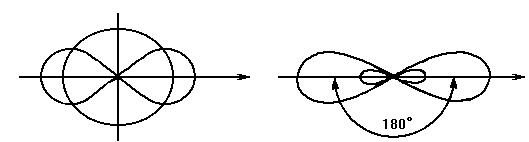
в)Образование sp-гибридного облака
Рис.5
 2015-10-22
2015-10-22 925
925








