Пространственная структура молекул определяется числом атомов в молекуле и направленностью химических связей.
Линейное строение имеют двухатомные молекулы (Н2), трехатомные молекулы СаCl2, С2Н2).
Трехатомные молекулы могут иметь угловое строение (H2S, H2O); пирамидальное (NH3); плоский треугольник (AlCl3, BF3).
Молекулы многоатомные имеют более сложные конфигурации – тетраэдрическая (СН4), октаэдрическая (SF6); циклические (С4Н8, С6Н6) и др.
 фтороводород
фтороводород
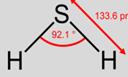
сероводород
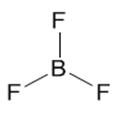 фторд бора
фторд бора
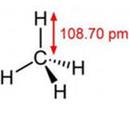 метан
метан
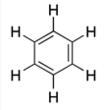 бензол
бензол
Химическая кинетика и равновесие
Химическая кинетика – это раздел химии, изучающий скорость протекания химических реакций и факторы, влияющие на нее. Химические реакции бывают гомогенными и гетерогенными. Если реагирующие вещества находятся в одной фазе – это гомогенная реакция, а если в разных – гетерогенная.
Фаза – это часть системы, отделенная от других частей поверхностью раздела, при переходе через которую свойства системы изменяются скачкообразно.
Примером гомогенной реакции служит взаимодействие растворов AqNO3 и NaCl. Эта реакция протекает быстро и по всему объему:
AqNO3 + NaCl = AqCl + NaNO3.
 Примером гетерогенной реакции является процесс растворения цинка в растворе серной кислоты:
Примером гетерогенной реакции является процесс растворения цинка в растворе серной кислоты:
Zn + H2SO4 = ZnSO4 + H2
Скоростью гомогенной реакции называется изменение концентрации вещества, вступающего в реакцию или образующегося в ходе реакции ∆С в единицу времени ∆t  ,
,
(+) – ставится в том случае, если следят за изменением концентрации продуктов реакции, которая в ходе реакции увеличивается;
(-) – когда следят за изменением концентрации исходных веществ, которая в ходе реакции уменьшается.
Скоростью гетерогенной реакции называется изменение количества вещества, вступающего в реакцию или образующегося в ходе реакции ∆n в единицу времени ∆t на единице площади ∆S:
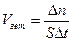 .
.
 2015-10-22
2015-10-22 4108
4108
