Сложный состав нефти и огромное количество содержащихся в ней компонентов заставили искать закономерности её состава. Важнейшими и самыми хорошо изученными среди углеводородов любой нефти являются алканы; именно на их основе и возникла новая отрасль органической химии – химия нефти и газа, основоположником которой является немецкий химик Шорлеммер (1834-1892).
Углеводороды, в молекулах которых углеродные атомы связаны между собой простой (одинарной) связью (σ–связью), причём все единицы валентности, не затраченные на связь между углеродными атомами, насыщены атомами водорода, называются насыщенными или предельными углеводородами.
Атомы углерода находятся в первом валентном состоянии, которому соответствует sp3 – гибридизация, и во всех своих соединениях четырёхвалентны. Все связи в алканах равноценны и находятся под тетраэдрическим углом друг к другу, что обусловливает зигзагообразное строение углеводородной цепочки.
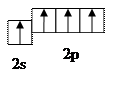
Простая связь (σ–связь) образуется за счёт перекрывания двух орбиталей
s–электронов или перекрыванием орбитали s-электрона (например, атома водорода) с sp3 – гибридными орбиталями атома углерода (при образовании, например, молекулы метана) или за счёт перекрывания двух sp3 – гибридных орбиталей атомов углерода (при образовании С – С –связи в предельных углеводородах).
Вещества, имеющие сходное химическое строение и отличающиеся друг от друга по составу на одну или несколько групп СН2, обладающие близкими химическими и закономерно изменяющимися физическими свойствами, называются гомологами, а группа СН2 – гомологической разностью. Группа гомологов составляет гомологический ряд. Общая формула ряда алканов, или предельных углеводородов, CnH2n+2.
Первые четыре члена гомологического ряда предельных углеводородов (алканов, парафинов) имеют тривиальные названия (метан, этан, пропан, бутан). Названия последующих гомологов производятся от греческих числительных с добавлением окончания – ан:
С5Н12 – пентан, С9Н20 – нонан, С13Н28 – тридекан,
С6Н14 – гексан, С10Н22 – декан, С14Н30 – тетрадекан,
С7Н16 – гептан, С11Н24 – ундекан, С15Н32 – пентадекан,
С8Н18 – октан, С12Н26 – додекан, С16Н34 – гексадекан и т.д.
При отрыве от молекулы алкана одного атома водорода образуется углеводородный радикал. Названия радикалов образуются из названий соответствующих предельных углеводородов заменой окончания - ан на – ил, например, СН4 – метан, СН3 – метил и т.д.
Для органических соединений характерно явление изомерии. Оно заключается в том, что вещества, обладающие одинаковым составом и молекулярной массой, имеют разное строение, а, значит, и различные физические и химические свойства. К таким соединениям, называемым изомерами, относятся, например,
бутадиен–1,3 СН2=СН–СН =СН2 и бутин–1 НС≡С–СН2–СН3.
Известны два типа изомерии – структурная и пространственная. Структурные изомеры различаются последовательностью соединения атомов в молекуле. Существует несколько видов структурной изомерии: изомерия углеродного скелета, изомерия положения кратных связей и изомерия положения функциональных групп.
Для вывода структурных формул изомеров, различающихся последовательностью связей атомов углерода в молекуле: а) составляют структурную формулу углеродного скелета углеводорода нормального строения с заданным числом атомов углерода; б) постепенно укорачивают цепь (каждый раз на один атом углерода) и производят все возможные перестановки одной или нескольких групп СН3 и таким образом выводят все возможные формулы изомеров.
В основу систематической, или международной, номенклатуры положено название самой длинной нормальной (неразветвлённой) углеродной цепи с добавлением в качестве приставки названия боковых ответвлений (радикалов). Для этого выделяют самую длинную цепь атомов углерода и нумеруют её с того конца, к которому ближе расположен радикал. При этом нумерацию атомов С производят таким образом, чтобы цифры, указывающие положение заместителей, были наименьшими. Если же радикалов несколько, то цифрой отмечают каждый из них. Количество одинаковых радикалов обозначается приставками ди-, три-, тетра- и т.д.Сами радикалы перечисляются в порядке возрастания сложности. Более простыми считаются радикалы с меньшим числом углеродных атомов.
Атом углерода называется первичным, вторичным, третичным или четвертичным в зависимости от того, затратил ли он на связь с другими атомами углерода одну, две, три или четыре валентности.
В химическом отношении при обычных условиях алканы менее реакционноспособны, чем углеводороды других классов. В настоящее время известны следующие основные типы реакций, в которые вступают алканы: реакции замещения, окисления, крекинга, дегидрирования.
Все нефти содержат алканы, содержание которых колеблется от 20 до 50%. В парафинистых нефтях содержание алканов может достигать 60% и более; в малопарафинистых нефтях их содержание падает до 1-2%. В нефтях присутствуют как нормальные предельные углеводороды, так и изомеры. В частности, в них найдены все изомеры пентана, гексана, гептана. Из 18 изомеров октана выделено 17, из 35 возможных изомеров нонана – 24. В большинстве случаев в нефти присутствуют наиболее устойчивые малоразветвлённые углеводороды, содержащие один или два радикала метила в главной цепи. Углеводороды с четвертичным атомом практически отсутствуют. В нефтях некоторых типов содержатся заметные количества сильноразветвлённых алканов с регулярным расположением метилов в главной цепи в положении 2, 6, 10, 14 и т. д. Это изопреноидные углеводороды или изопренаны (изопрены). Их количество может достигать 3-4% на нефть.

 2015-10-22
2015-10-22 1448
1448
