ТЕМА: Окислительно-восстановительные реакции
• Окислительно-восстановительными называются реакции, сопровождающиеся изменением степени окисления атомов, входящих в состав реагирующих веществ. Под степенью окисления понимают тот условный заряд атома, который вычисляется исходя из предположения, что молекула состоит только из ионов. Иными словами: степень окисления — это тот условный заряд, который приобрел бы атом элемента, если предположить, что он принял или отдал то или иное число электронов.
Окисление—восстановление — это единый, взаимосвязанный процесс. Окисление приводит к повышению степени окисления восстановителя, а восстановление — к ее понижению у окислителя.
Повышение или понижение степени окисления атомов отражается в электронных уравнениях; окислитель принимает электроны, а восстановитель их отдает. При этом не имеет значения, переходят ли электроны от одного атома к другому полностью и образуются ионные связи или электроны только оттягиваются к более электроотрицательному атому и возникает полярная связь. О способности того или иного вещества проявлять окислительные, восстановительные или двойственные (как окислительные, так и восстановительные) свойства можно судить по степени окисления атомов окислителя и восстановителя.
Атом того или иного элемента в своей высшей степени окисления не может ее повысить (отдать электроны) и проявляет только окислительные свойства, а в своей низшей степени окисления не может ее понизить (принять электроны} и проявляет только восстановительные свойства. Атом же элемента, имеющий промежуточную степень окисления, может проявлять как окислительные, так и восстановительные свойства.
Например:
N5+ (HNO3) S6+ (H2SO4) проявляют только окислительные свойства;
 N4+ (NO2) S4+ (SO2)
N4+ (NO2) S4+ (SO2)
N3+ (HNO2)
N2+ (NO) S2+ (SO) проявляют окислительные и
N1+ (N2O) восстановительные свойства
N0 (N2) S0 (S2, S8)
N1- (NH2OH) S-1 (H2S2)
N2- (N2H4)
N3- (NH3) S2- (H2S) проявляют только восстановительные свойства
При окислительно-восстановительных реакциях валентность атомов может и не меняться. Например, в окислительно-восстановительной реакции Н20 + Cl20 = 2H+ CI- валентность атомов водорода и хлора до и после реакции равна единице. Изменилась их степень окисления. Валентность определяет число связей, образованных данным атомом, и поэтому знака не имеет. Степень же окисления имеет знак плюс или минус.
Пример 1. Исходя из степени окисления (n) азота, серы и марганца в соединениях NН3, НNO2, НNО3, Н2S, Н2SО3, H2SO4, МnО2, КMnO4, определите, какие из них могут быть только восстановителями, только окислителями и какие проявляют как окислительные, так и восстановительные свойства.
Решение. Степень окисления n (N) в указанных соединениях соответственно равна: —3 (низшая), + 3 (промежуточная), +5 (высшая); n (S) соответственно равна: —2 (низшая), +4 (промежуточная), +6 (высшая); n (Мn) соответственно равна: +4 (промежуточная), +7 (высшая). Отсюда: NН3, Н2S — только восстановители; НNО3, H2SO4, КMnO4 — только окислители; НNO2, Н2SО3, МnО2 — окислители и восстановители.
Пример 2. Могут ли происходить окислительно-восстановительные реакции между следующими веществами: a) Н2S и HI; б) Н2S и Н2SО3; в) Н2SО3 и HCIO4?
Решение. а) Степень окисления в Н2S n (S) = —2; в HI n (I) =—1. Так как и сера, и йод находятся в своей низшей степени окисления, то оба взятые вещества проявляют только восстановительные свойства и взаимодействовать друг с другом не могут; б) в Н2S n (S) = —2 (низшая); в Н2SО3 n (S) = +4 (промежуточная). Следовательно, взаимодействие этих веществ возможно, причем Н2SО3 является окислителем; в) в Н2SО3 n (S) = +4 (промежуточная); в HCIO4 n (Cl) = +7 (высшая). Взятые вещества могут взаимодействовать. Н2SО3 в этом случае будет проявлять восстановительные свойства.
Пример 3. Составьте уравнения окислительно-восстановительной реакции, идущей по схеме.

Решение. Если в условии задачи даны как исходные вещества, так и продукты их взаимодействия, то написание уравнения реакции сводится, как правило, к нахождению и расстановке коэффициентов. Коэффициенты определяют методом электронного баланса с помощью электронных уравнений. Вычисляем, как изменяют свою степень окисления восстановитель и окислитель, и отражаем это в электронных уравнениях:
 восстановитель 5 Р3+ - 2 ē = Р5+ процесс окисления
восстановитель 5 Р3+ - 2 ē = Р5+ процесс окисления
окислитель 2 Mn7+ +5 ē = Mn2+ процесс восстановления
Общее число электронов, отданных восстановителем, должно быть равно числу электронов, которое присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов десять. Разделив это число на 5, получаем коэффициент 2 для окислителя и продукта его восстановления, а при делении 10 на 2 получаем коэффициент 5 для восстановителя и продукта его окисления. Коэффициент перед веществами, атомы которых не меняют свою степень окисления, находят подбором. Уравнение реакции будет иметь вид
2KMnO4 + 5H3PO3 + 3H2SO4 = 2MnSO4 + 5H3PO4 + K2SO4 + 3H2O
Пример 4. Составьте уравнение реакции взаимодействия цинка с концентрированной серной кислотой, учитывая максимальное восстановление последней.
Решение. Цинк, как любой металл, проявляет только восстановительные свойства. В концентрированной серной кислоте окислительную функцию несет сера (+6). Максимальное восстановление серы означает, что она приобретает минимальную степень окисления. Минимальная степень окисления серы как р-элемента VIA rpyппы равна —2. Цинк как металл II В группы имеет постоянную степень окисления +2. Отражаем сказанное в электронных уравнениях:
 восстановитель 4 Zn0 – 2 ē = Zn2+ процесс окисления
восстановитель 4 Zn0 – 2 ē = Zn2+ процесс окисления
окислитель 1 S6+ + 8 ē = S2- процесс восстановления
Составляем уравнение реакции:
4Zn + 5H2SO4 = 4ZnSO4 + H2S + 4H2O
Перед H2SO4 стоит коэффициент 5, а не 1, ибо четыре молекулы H2SO4 идут на связывание четырех ионов Zn2+.
I
Контрольные вопросы
221. Исходя из степени окисления хлора в соединениях НС1, НСlO3, HСlO4, определите, какое из них является только окислителем, только восстановителем и какое может проявлять как окислительные, так и восстановительные свойства. Почему? На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме
KBr + KBrO3 + H2SO4 → Br2 + K2SO4 + H2O
222. Реакции выражаются схемами:
P + HIO3 + H2O → H3PO4 + HI
H2S + Cl2 + H2O → H2SO4 + HCl
Составьте электронные уравнения. Расставьте коэффициенты в уравнениях реакций. Для каждой реакции укажите, какое вещество является окислителем, какое — восстановителем; какое вещество окисляется, какое — восстанавливается.
223. См. условие задачи 222.
HNO3 + Zn → N2O + Zn(NO3)2 + H2O
FeSO4 + KСlO3 + H2SO4 → Fe2(SO4)3 + KCl + H2O
224. См. условие задачи 222.
K2Cr2O7 + HCl → Cl2 + CrCl3 + KCl + H2O
Au + HNO3 + HCl → AuCl3 + NO + H2O
225. Могут ли происходить окислительно-восстановительные реакции между веществами: а) NH3 и КМnO4; б) НNO2 и HI; в) НС1 и H2Se? Почему? На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме
KMnO4 + KNO2 + H2SO4 → MnSO4 + KNO3 + K2SO4 + H2O
226. См. условие задачи 222.
HCl + CrO3 → Cl2 + CrCl3 + H2O
Cd + KMnO4 + H2SO4 → CdSO4 + MnSO4 + K2SO4 + H2O
227. См. условие задачи 222.
Cr2O3 + KСlO3 + KOH → K2CrO4 + KCl + H2O
MnSO4 + PbO2 +HNO3 → HMnO4 + Pb(NO3)2 + PbSO4 + H2O
228. См. условие задачи 222.
H2SO3 + HClO3 → H2SO4 + HCl
FeSO4 + K2Cr2O7 + H2SO4 → Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O
229. См. условие задачи 222.
I2 + Cl2 + H2O → HIO3 + HCl
K2Cr2O7 + H3PO3 + H2SO4 → Cr2(SO4)3 + H3PO4 + K2SO4 + H2O
230. Могут ли происходить окислительно-восстановительные реакции между веществами: а) РН3 и НВг; б) K2Cr2O7 и Н3РО3; в) НNО3 и H2S? Почему? На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме
AsH3 + HNO3 → H3AsO4 + NO2 + H2O
231. См. условие задачи 222.
P + HClO3 + H2O → H3PO4 + HCl
H3AsO3 + KMnO4 + H2SO4 → H3AsO4 + MnSO4 + K2SO4 + H2O
232. См. условие задачи 222
NaCrO2 + Br2 + NaOH → Na2CrO4 + NaBr + H2O
FeS + HNO3 →Fe(NO3)2 + S + NO + H2O
233. Составьте электронные уравнения и укажите, какой процесс — окисление или восстановление — происходит при следующих превращениях:
As3- → As5+; N3+ → N3-; S2-→ So
На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме
Na2SO3 + KMnO4 + H2O → Na2SO4 + MnO2 + KOH
234. Исходя из степени окисления фосфора в соединениях РН3, H3РO4, Н3РО3, определите, какое из них является только окислителем, только восстановителем и какое может проявлять как окислительные, так и восстановительные свойства. Почему? На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме
PbS + HNO3 → S + Pb(NO3)2 + NO + H2O
235. См. условие задачи 222.
P + HNO3 + H2O → H3PO4 + NO
KMnO4 + Na2SO3 + KOH → K2MnO4 + Na2SO4 + H2O
236. Составьте электронные уравнения и укажите, какой процесс — окисление или восстановление — происходит при следующих превращениях:
Mn6+ → Mn2+; Cl5+ → Cl-; N3- → N5+
На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме
Cu2O + HNO3 → Cu(NO3)2 + NO + H2O
237. См. условие задачи 222.
HNO3 + Ca → NH4NO3 + Ca(NO3)2 + H2O
K2S + KMnO4 + H2SO4 → S + K2SO4 + MnSO4 + H2O
238. Исходя из степени окисления хрома, йода и серы в соединениях K2Cr2O7, КI и Н2SО3, определите, какое из них является только окислителем, только восстановителем и какое может проявлять как окислительные, так и восстановительные свойства. Почему? На основании электронных уравнений расставьте, коэффициенты в уравнении реакции, идущей по схеме
NaCrO2 + PbO2 + NaOH → Na2CrO4 + Na2PbO2 + H2O
239. См. условие задачи 222.
H2S + Cl2 + H2O → H2SO4 + HCl
K2Cr2O7 + H2S + H2SO4 → S + Cr2(SO4)3 + K2SO4 + H2O
240. См. условие задачи 222.
KClO3 + Na2SO3 → KCl + Na2SO4
KMnO4 + HBr → Br2 + KBr + MnBr2 + H2O
ТЕМА: Электронные потенциалы и электродвижущие силы
При решении задач этого раздела см. табл. 7.
Если металлическую пластинку опустить в воду, то катионы металла на ее поверхности гидратируются полярными молекулами воды и переходят в жидкость. При этом электроны, в избытке остающиеся в металле, заряжают его поверхностный слой отрицательно. Возникает электростатическое притяжение между перешедшими в жидкость гидратированными катионами и поверхностью металла. В результате этого в системе устанавливается подвижное равновесие:
Ме + m H2O ↔ Me(H2O) mn+ + nē
в растворе на металле
где n — число электронов, принимающих участие в процессе. На границе металл — жидкость возникает двойной электрический слой, характеризующийся определенным скачком потенциала — электродным потенциалом. Абсолютные значения электродных потенциалов измерить не удается. Электродные потенциалы зависят от ряда факторов (природы металла, концентрации, температуры и др.). Поэтому обычно определяют относительные электродные потенциалы в определенных условиях — так называемые стандартные электродные потенциалы (Е°).
Стандартным электродным потенциалом металла называют его электродный потенциал, возникающий при погружении металла в раствор собственного иона с концентрацией (или активностью), равной 1 моль/л, измеренный по сравнению со стандартным водородным электродом, потенциал которого при 25°С условно принимается равным нулю (Е° = 0; ∆G° = 0).
Располагая металлы в ряд по мере возрастания их стандартных электродных потенциалов (Е°), получаем так называемый ряд напряжений.
Положение того или иного металла в ряду напряжений характеризует его, восстановительную способность, а также окислительные свойства его ионов в водных растворах при стандартных условиях. Чем меньше значение Е°, тем большими восстановительными способностями обладает данный металл в виде простого вещества и тем меньшие окислительные способности проявляют его ионы, и наоборот. Электродные потенциалы измеряют в приборах, которые получили название гальванических элементов. Окислительно-восстановительная реакция, которая характеризует работу гальванического элемента, протекает в направлении, в котором ЭДС элемента имеет положительное значение. В этом случае ∆G° < 0, так как ∆G° = — nFE°.
Пример 1. Стандартный электродный потенциал никеля больше, чем кобальта (табл. 8). Изменится ли это соотношение, если измерить потенциал никеля в растворе его ионов с концентрацией 0,001 моль/л, а потенциал кобальта — в растворе с концентрацией 0,1 моль/л?
Решение. Электродный потенциал металла (Е) зависит от концентрации его ионов в растворе. Эта зависимость выражается уравнением Нернста:
Е = Е° +  lg C
lg C
где Е° — стандартный электродный потенциал; n — число электронов, принимающих участие в процессе; С — концентрация (при точных вычислениях — активность) гидратированных ионов металла в растворе, моль/л; Е° для никеля и кобальта соответственно равны —0,25 и —0,277 В. Определим электродные потенциалы этих металлов при данных в условии концентрациях:
ENi2+/ Ni = 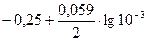 =-0,339 В,
=-0,339 В,
ECo2+/ Co = 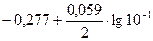 =-0,307 В,
=-0,307 В,
Таким образом, при изменившейся концентрации потенциал кобальта стал больше потенциала никеля.
Таблица 7.Стандартные электродные потенциалы (Eo), некоторых металлов (ряд напряжений)
| Электрод | Eo, В | Электрод | Eo, В | |
| Li+/Li | -3,045 | Cd2+/Cd | -0,403 | |
| Rb+/Rb | -2,925 | Co2+/Co | -0,277 | |
| K+/K | -2,924 | Ni2+/Ni | -0,25 | |
| Cs+/Cs | -2,923 | Sn2+/Sn | -0,136 | |
| Ba2+/Ba | -2,90 | Pb2+/Pb | -0,127 | |
| Ca2+/Ca | -2,87 | Fe3+/Fe | -0,037 | |
| Na+/Na | -2,714 | 2H+/H2 | -0,000 | |
| Mg2+/Mg | -2,37 | Sb3+/Sb | +0,20 | |
| Al3+/Al | -1,70 | Bi3+/Bi | +0,215 | |
| Ti2+/Ti | -1,603 | Cu2+/Cu | +0,34 | |
| Zr4+/Zr | -1,58 | Cu+/Cu | +0,52 | |
| Mn2+/Mn | -1,18 | Hg22+/2Hg | +0,79 | |
| V2+/V | -1,18 | Ag+/Ag | +0,80 | |
| Cr2+/Cr | -0,913 | Hg2+/Hg | +0,85 | |
| Zn2+/Zn | -0,763 | Pt2+/Pt | +1,19 | |
| Cr+3/Cr | -0,74 | Au3+/Au | +1,50 | |
| Fe2+/Fe | -0,44 | Au+/Au | +1,70 |
Пример 2. Магниевую пластинку опустили в раствор её соли. При этом электродный потенциал магния оказался равен —2,41 В. Вычислите концентрацию ионов магния (в моль/л).
Решение. Подобные задачи также решаются на основании уравнения Нернста (см. пример 1):
-2,41=-2,37+ 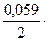 lgC,
lgC,
-0,04=0,0295lgC,
lgC=  -1,3559 = - 2,6441
-1,3559 = - 2,6441
СMg2+=  моль/л
моль/л
Пример 3. Составьте схему гальванического элемента, в котором электродами являются магниевая и цинковая пластинки, опущенные в растворы их ионов с активной концентрацией 1 моль/л. Какой металл является анодом, какой катодом? Напишите уравнение окислительно-восстановительной реакции, протекающей в этом гальваническом элементе, и вычислите его ЭДС.
Решение. Схема данного гальванического элемента

Вертикальная линейка обозначает поверхность раздела между металлом и раствором, а две линейки - границу раздела двух жидких фаз - пористую перегородку -(или соединительную трубку, заполненную раствором электролита). Магний имеет меньший потенциал (-2,37 В) и является анодом, на котором протекает окислительный процесс:
 (1)
(1)
Цинк, потенциал которого -0,763 В - катод, т. е. электрод, на котором протекает восстановительный процесс:
 (2)
(2)
Уравнение окислительно-восстановительной реакции, характеризующее работу данного гальванического элемента, можно получить, сложив электронные уравнения анодного (1) и катодного (2) процессов:

Для определения ЭДС гальванического элемента из потенциала катода следует вычесть потенциал анода. Так как концентрация ионов в растворе равна 1 моль/л, то ЭДС элемента равна разности стандартных потенциалов двух его электродов:

Контрольные вопросы
241. При каком условии будет работать гальванический элемент, электроды которого сделаны из одного и того же металла? Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, в котором один никелевый электрод находится в 0,001 М растворе, а другой такой же электрод — в 0,01 М растворе сульфата никеля. Ответ: 0,0295 В.
242. Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, состоящего из свинцовой и магниевой пластин, опущенных в растворы своих солей с концентрацией [ Рb2+ ] = [Мg2+ ] = 0,01 моль/л. Изменится ли ЭДС этого элемента, если концентрацию каждого из ионов увеличить в одинаковое число раз? Ответ: 2,244 В.
243. Составьте схемы двух гальванических элементов, в одном из которых никель является катодом, а в другом — анодом. Напишите для каждого из этих элементов электронные уравнения реакций, протекающих на катоде и на аноде.
244. Железная и серебряная пластины соединены внешним проводником и погружены в раствор серной кислоты. Составьте схему данного гальванического элемента и напишите электронные уравнения процессов, происходящих на аноде и на катоде.
245. Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, состоящего из пластин кадмия и магния, опушенных в растворы своих солей с концентрацией [Mg2+] = [Cd2+] = 1 моль/л. Изменится ли значение ЭДС, если концентрацию каждого из ионов понизить до 0,01 моль/л? Ответ: 1.967 В.
246. Составьте схему гальванического элемента, состоящего из пластин цинка и железа, погруженных в растворы их солей. Напишите электронные уравнения процессов, протекающих на аноде и на катоде. Какой концентрации надо было бы взять ионы железа (моль/л), чтобы ЭДС элемента стала равной нулю, если [Zn2+] = 0,001 моль/л? Ответ: 7,3·10-15 моль/л.
247. Составьте схему гальванического элемента, в основе которого лежит реакция, протекающая по уравнению
Ni + Pb(NO3)2 = Ni(NO3)2 + Pb
Напишите электронные уравнения анодного и катодного процессов. Вычислите ЭДС этого элементе, если [Ni2+ ] = 0,01 моль/л, [Pb2+] = 0,0001 моль/л. Ответ: 0,064 В.
248. Какие химические процессы протекают на электродах при зарядке и разрядке свинцового аккумулятора?
249. Какие химические процессы протекают на электродах при зарядке и разрядке кадмий-никелевого аккумулятора?
250. Какие химические процессы протекают на электродах при зарядке и разрядке железо-никелевого аккумулятора?
251. В два сосуда с голубым раствором медного купороса, поместили в первый цинковую пластинку, а во второй серебряную. В каком сосуде цвет раствора постепенно пропадает? Почему? Составьте электронные и молекулярное уравнения соответствующей реакции.
252. Увеличится, уменьшится или останется без изменения масса цинковой пластинки при взаимодействии ее с растворами: a) CuSО4; б) MgSО4; в) РЬ(NO3)2? Почему? Составьте электронные и молекулярные уравнения соответствующих реакций.
253. При какой концентрации ионов Zn2+ (в моль/л) потенциал цинкового электрода будет на 0,015 В меньше его стандартного электродного потенциала? Ответ: 0,30 моль/л
254. Увеличится, уменьшится или останется без изменения масса кадмиевой пластинки при взаимодействии ее с растворами: а) AgNO3; б) ZnSO4; в) NiSO4? Почему? Составьте электронные и молекулярные уравнения соответствующих реакций.
255. Марганцевый электрод в растворе его соли имеет потенциал —1,23 В. Вычислите концентрацию ионов Мn2+ (в моль/л). Ответ: 2,02 · 10-2 моль/л.
256. Потенциал серебряного электрода в растворе АgNO3 составил 95% от значения его стандартного электродного потенциала. Чему равна концентрация ионов Аg+ (в моль/л)? Ответ: 0,20 моль/л.
257. Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС медно-кадмиевого гальванического элемента, в котором [Cd2+] = 0,8 моль/л, а [Сu2+] = 0,01 моль/л. Ответ: 0,68 В.
258. Составьте схемы двух гальванических элементов, в одном из которых медь была бы катодом, а в другом — анодом. Напишите для каждого из этих элементов электронные уравнения реакций, протекающих на катоде и на аноде.
259. При какой концентрации ионов Сu2+ (моль/л) значение потенциала медного электрода становится равным стандартному потенциалу водородного электрода? Ответ: 1,89 · 10-12 моль/л.
260. Какой гальванический элемент называется концентрационным? Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, состоящего из серебряных электродов, опущенных: первый в 0,01 н., а второй в 0,1 н. растворы AgNO3. Ответ: 0,059 В.
ТЕМА: Электролиз
Пример 1. Какая масса меди выделится на катоде при электролизе раствора CuSО4 в течение 1 ч при силе тока 4 А?
Решение. Согласно законам Фарадея
 (1)
(1)
где m - масса вещества, окисленного или восстановленного на электроде, г; Э - эквивалентная масса вещества, г/моль; I - сила тока, A; t - продолжительность электролиза, с. Эквивалентная масса меди в CuSО4 равна 63,54:2 = 31,77 г/моль. Подставив в формулу (1) значения Э = 31,77; I =4 A, t = 60 · 60 =3600 с, получим

Пример 2. Вычислите эквивалентную массу металла, зная, что при электролизе раствора хлорида этого металла затрачено 3880 Кл электричества и на катоде выделяется 11,742 г металла.
Решение. Из формулы (1)
Э = 11,742 · 96500/3880 = 29,35 г/моль,
Где m =11,742 г; It = Q =3880 Кл.
Пример 3. Чему равна сила тока при электролизе раствора в течение 1 ч 40 мин 25 с, если на катоде выделилось 1,4 л водорода (н.у.)?
Решение. Из формулы (1)
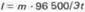
Так как дан объем водорода, то отношение m/Э заменяем отношением Vн2 /Vэ(н2), где Vн2 - объем водорода, л; Vэ(н2) - эквивалентный объем водорода, л. Тогда
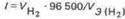
Эквивалентный объем водорода при н.у. равен половине молярного объема 22,4/2 = 11,2 л. Подставив в приведенную формулу значения Vн2 = 1,4 л, Vэ(н2) = 11,2 л, t = 6025 (1ч 40 мин 25 с = 6025 с), находим
I = 1,4 · 96500/11,2 · 6025 = 2 А.
Пример 4. Какая масса гидроксида калия образовалась у катода при электролизе раствора K2SО4, если на аноде выделилось 11,2 л кислорода (н.у.)?
Решение. Эквивалентный объем кислорода (н.у.) 22,4/4 = 5,6 л. Следовательно, 11,2 л содержат две эквивалентные массы кислорода. Столько же эквивалентных масс КОН образовалось у катода, или 56,11 · 2 = 112,22 г (56,11 г/моль - мольная и эквивалентная масса КОН).
Контрольные вопросы
261. Составьте электронные уравнения процессов, происходящих на угольных электродах при электролизе раствора АgNO3. Если электролиз проводить с серебряным анодом, тo его масса уменьшается на 5,4 г. Определите расход электричества при этом. Ответ: 4830 Кл.
262. Электролиз раствора CuSО4 проводили в течение 15 мин при силе тока 2,5 А. Выделилось 0,72 г меди. Составьте электронные уравнения процессов, происходящих на электродах в случае медного и угольного анода. Вычислите выход по току (отношение массы выделившегося вещества к теоретически возможной). Ответ: 97,3 %
263. Составьте электронные уравнения процессов, происходящих на графитовых электродах при электролизе расплавов и водных растворов NaCI и КОН. Сколько литров (н.у.) газа выделится на аноде при электролизе гидроксида калия, если электролиз проводить в течение 30 мин при силе тока 0,5 А? Ответ: 0,052 л.
264. Составьте электронные уравнения процессов, происходящих на графитовых электродах при электролизе раствора КВr. Какая масса вещества выделяется на катоде и аноде, если электролиз проводить в течение 1 ч 35 мин при силе тока 15 А? Ответ: 0,886 г; 70,79 г.
265. Составьте электронные уравнения процессов, происходящих на угольных электродах при электролизе раствора CuCI2. Вычислите массу меди, выделившейся на катоде, если на аноде выделилось 560 мл газа (н.у.). Ответ: 1,588 г.
266. При электролизе соли трехвалентного металла при силе тока 1,5 А в течение 30 мин на катоде выделилось 1,071 г металла. Вычислите атомную массу металла. Ответ; 114,82.
267. При электролизе растворов MgSО4 и ZnCI2, соединенных последовательно с источником тока, на одном из катодов выделилось 0,25 г водорода. Какая масса вещества выделится на другом катоде; на анодах? Ответ: 8,17 г; 2,0 г; 8,86 г.
268. Составьте электронные уравнения процессов, происходящих на угольных электродах при электролизе раствора Na2SО4. Вычислите массу вещества, выделяющегося на катоде, если на аноде выделяется 1,12 л газа (н.у.). Какая масса H2SO4 образуется при этом возле анода? Ответ: 0,2 г; 9,8 г.
269. При электролизе раствора соли кадмия израсходовано 3434 Кл электричества. Выделилось 2 г кадмия. Чему равна эквивалентная масса кадмия? Ответ: 56,26 г/моль.
270. Составьте электронные уравнения процессов, происходящих на электродах при электролизе раствора КОН. Чему равна сила тока, если в течение 1 ч 15 мин 20 с на аноде выделилось 6,4 г газа? Сколько литров газа (н.у.) выделилось при этом на катоде? Ответ: 17,08 А; 8,96 л.
271. Электролиз раствора K2SO4 проводили при силе тока 5 А в течение 3 ч. Составьте электронные уравнения процессов, происходящих на электродах. Какая масса воды при этом разложилась и чему равен объем газов (н.у.), выделившихся на катоде и аноде? Ответ: 5,03 г; 6,266 л; 3,133 л
272. При электролизе соли некоторого металла в течение 1,5 ч при силе тока 1,8 А на катоде выделилось 1,75 г этого металла. Вычислите эквивалентную массу металла. Ответ: 17,37 г/моль.
273. При электролизе раствора CuSО4 на аноде выделилось 168 см3 газа (н.у.). Составьте электронные уравнения процессов, происходящих на электродах, и вычислите, какая масса меди выделилась на катоде.
Ответ: 0,953 г.
274 Электролиз раствора Nа2SO4 проводили в течение 5 ч при силе тока 7 А. Составьте электронные уравнения процессов, происходящих на электродах. Какая масса воды при этом разложилась и чему равен объем газов (н.у.), выделившихся на катоде и аноде? Ответ: 11,75 г; 14,62л; 7,31л.
275. Электролиз раствора нитрата серебра проводили при силе тока 2 А в течение 4 ч. Составьте электронные уравнения процессов, происходящих на электродах. Какая масса серебра выделилась на катоде и каков объем газа (н.у.), выделившегося на аноде? Ответ: 32,20 г; 1,67 л.
276 Электролиз раствора сульфата некоторого металла проводили при силе тока 6 А в течение 45 мин, в результате чего на катоде выделилось 5,49 г металла. Вычислите эквивалентную массу металла. Ответ: 32,7 г/моль.
277. Насколько уменьшится масса серебряного анода, если электролиз раствора AgNO3 проводить при силе тока 2 А в течение 38 мин 20 с? Составьте электронные уравнения процессов, происходящих на графитовых электродах. Ответ: 4,47 г.
278. Электролиз раствора сульфата цинка проводили в течение 5 ч, в результате чего выделилось 6 л кислорода (н.у.). Составьте уравнения электродных процессов и вычислите силу тока. Ответ: 5,74 А.
279. Электролиз раствора CuSО4 проводили с медным анодом в течение 4 ч при силе тока 50 А. При этом выделилось 224 г меди. Вычислите выход по току (отношение массы выделившегося вещества к теоретически возможной). Составьте электронные уравнения процессов, происходящих на электродах в случае медного и угольного анода. Ответ: 94,48 %.
280. Электролиз раствора NaI проводили при силе тока 6 А в течение 2,5 ч. Составьте электронные уравнения процессов, происходящих на угольных электродах, и вычислите массу вещества, выделившегося на катоде и аноде? Ответ: 0,56 г; 71,0 г.
ТЕМА: Коррозия металлов
При решении задач этого раздела см. табл. 7.
Коррозия — это самопроизвольно протекающий процесс разрушения металлов, в результате химического или электрохимического взаимодействия их с окружающей средой.
При электрохимической коррозии на поверхности металла одновременно протекают два процесса:
анодный - окисление металла
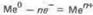
и катодный — восстановление ионов водорода

или молекул кислорода, растворенного в воде,
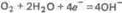
Ионы или молекулы, которые восстанавливаются на катоде, называются деполяризаторами. При атмосферной коррозии — коррозии во влажном воздухе при комнатной температуре — деполяризатором является кислород.
Пример 1. Как происходит коррозии цинка, находящегося в контакте с кадмием в нейтральном и кислом растворах. Составьте электронные уравнения анодного и катодного процессов. Каков состав продуктов коррозии?
Решение. Цинк имеет более отрицательный потенциал (—0,763 В), чем кадмий (—0,403 В), поэтому он является анодом, а кадмий катодом.
Анодный процесс:

катодный процесс:
в кислой среде

в нейтральной среде

Так как ионы Zn2+ с гидроксильной группой образуют нерастворимый гидроксид, то продуктом коррозии будет Zn(OH)2.
Контрольные вопросы
281. Железное изделие покрыли кадмием. Какое это покрытие — анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении покрытия во влажном воздухе и в хлороводородной (соляной) кислоте. Какие продукты коррозии образуются в первом и во втором случаях?
282. Железное изделие покрыли свинцом. Какое это покрытие — анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении покрытия во влажном воздухе и в хлороводородной (соляной) кислоте. Какие продукты коррозии образуются в первом и во втором случаях?
283. Две железные пластинки, частично покрытые одна оловом, другая медью, находятся во влажном воздухе. На какой из этих пластинок быстрее образуется ржавчина? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этих пластинок. Каков состав продуктов коррозии железа?
284. Какой металл целесообразней выбрать для протекторной защиты от коррозии свинцовой оболочки кабеля: цинк, магний или хром? Почему? Составьте электронные уравнения анодного и катодного процессов атмосферной коррозии. Какой состав продуктов коррозии?
285. Если опустить в разбавленную серную кислоту пластинку из чистого железа, то выделение на ней водорода идет медленно и со временем почти прекращается. Однако если цинковой палочной прикоснуться к железной пластинке, то на последней начинается бурное выделение водорода. Почему? Какой металл при этом растворяется? Составьте электронные уравнения анодного и катодного процессов.
286. Цинковую и железную пластинки опустили в раствор сульфата меди. Составьте электронные и ионно-молекулярные уравнения реакций, происходящих на каждой из этих пластинок. Какие процессы будут проходить на пластинках, если наружные концы их соединить проводником?
287. Как влияет рН среды на скорость коррозии железа и цинка? Почему? Составьте электронные уравнения анодного и катодного процессов атмосферной коррозии этих металлов.
288. В раствор электролита, содержащего растворенный кислород, опустили цинковую пластинку и цинковую пластинку, частично покрытую медью. В каком случае процесс коррозии цинка проходит интенсивнее? Составьте электронные уравнения анодного и катодного процессов.
289. Составьте электронные уравнения анодного и катодного процессов с кислородной и водородной деполяризацией при коррозии пары алюминий — железо. Какие продукты коррозии образуются в первом и во втором случаях?
290. Как протекает атмосферная коррозия железа, покрытого слоем никеля, если покрытие нарушено? Составьте электронные уравнения анодного и катодного процессов. Каков состав продуктов коррозии?
291. Как происходит атмосферная коррозия луженого и оцинкованного железа при нарушении покрытия? Составьте электронные уравнения анодного и катодного процессов.
292. Медь не вытесняет водород из разбавленных кислот. Почему? Однако если к медной пластинке, опущенной в кислоту, прикоснуться цинковой, то на меди начинается бурное выделение водорода. Дайте этому объяснение, составив электронные уравнения анодного и катодного процессов. Напишите уравнение протекающей химической реакции.
293. Как происходит атмосферная коррозия луженого железа и луженой меди при нарушении покрытия? Составьте электронные уравнения анодного и катодного процессов.
294. Если пластинку из чистого цинка опустить в разбавленную кислоту, то начинающееся выделение водорода вскоре почти прекращается. Однако при прикосновении к цинку медной палочкой на последней начинается бурное выделение водорода. Дайте этому объяснение, составив электронные уравнения анодного и катодного процессов. Напишите уравнение протекающей химической реакции.
295. В чем сущность протекторной защиты металлов от коррозии? Приведите пример протекторной защиты железа в электролите, содержащем растворенный кислород. Составьте электронные уравнения анодного и катодного процессов.
296. Железное изделие покрыли никелем. Какое это покрытие — анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении покрытия во влажном воздухе и в хлороводородной (соляной) кислоте. Какие продукты коррозии образуются в первом и во втором случаях?
297. Составьте электронные уравнения анодного и катодного процессов с кислородной и водородной деполяризацией при коррозии пары магний — никель. Какие продукты коррозии образуются в первом и во втором случаях?
298. В раствор хлороводородной (соляной) кислоты поместили цинковую пластинку и цинковую пластинку, частично покрытую медью. В каком случае процесс коррозии цинка происходит интенсивнее? Ответ мотивируйте, составив электронные уравнения соответствующих процессов.
299. Почему химически чистое железо более стойко против коррозии, чем техническое железо? Составьте электронные уравнения анодного и катодного процессов, происходящих при коррозии технического железа во влажном воздухе и в кислой среде.
300. Какое покрытие металла называется анодным, и какое — катодным? Назовите несколько металлов, которые могут служить для анодного и катодного покрытия железа. Составьте электронные уравнения анодного и катодного процессов, происходящих при коррозии железа, покрытого медью, во влажном воздухе и в кислой среде.
ТЕМА: Коллоидные растворы
Коллоиды относятся к микрогетерогенным системам. В зависимости от отсутствия или наличия взаимодействия между частицами дисперсной фазы и дисперсной среды различают свободнодисперсные коллоиды - золи и связнодисперсные – гели.
В золях дисперсная фаза образована частицами, называемыми мицеллами, которые практически нерастворимы в дисперсной среде.
Строение мицеллы можно рассмотреть на примере обменной реакции, которая наблюдается в разбавленных растворах при небольшом избытке одного из реагентов:
Пример 1. Как представить условной химической формулой строение мицеллы золя, полученного в результате взаимодействия КI с избытком AgNO3?
Решение. Запишем уравнение взаимодействия указанных веществ в молекулярном и ионно-молекулярном виде:
AgNO3 + KI ® AgI¯ + KNO3
избыток
Ag+ + NO3- + K+ + I- ® AgI¯ + K+ + NO3-
Мицелла состоит из ядра, имеющего кристаллическую или аморфную структуру:
m[AgI]
Образовавшееся ядро коллоидной степени дисперсности является носителем свободной поверхностной энергии, поэтому на его поверхности идет адсорбционный процесс. Обычно адсорбируется ион, входящий в состав ядра и находящийся в избытке. В данном примере ионы серебра – Ag+ достраивают структуру ядра, образуя адсорбционный слой, и придают ядру соответственно положительный заряд m[AgI]×nAg+, поэтому их называют потенциалопределяющими ионами.
В растворе остаются ионы, заряд которых противоположный заряду потенциалопределяющих ионов – противоионы. В данном примере противоионами являются анионы NO3-, которые электростатически притягиваются потенциалопределяющими ионами адсорбционного слоя. Часть противоионов (n – x)NO3- прочно связывается электрическими и адсорбционными силами и входит в адсорбционный слой. Ядро с адсорбционным слоем называется гранулой:
{m[AgI]×nAg+× (n-x)NO3- }x+
Гранула имеет заряд потенциалопределяющих ионов, величина которого зависит от числа ионов, вошедших в адсорбционный слой. Оставшаяся часть противоионов образует диффузионный слой. Ядро с адсорбционным и диффузионным слоями называется мицеллой:
{m[AgI]×nAg+ ×(n-x)NO3- }x+ × xNO3-
Если получать золь йодистого серебра при избытке йодида калия, т.е. при избытке I-, то коллоидная частица, благодаря адсорбции ионов nI- на поверхности ядра, получит отрицательный заряд: m[AgI]×nI-
гранула
 |
{m[AgI]×nI-×(n-x)K+ }х-×xK+
 |
мицелла
Числа m, n, x в зависимости от условий приготовления золей могут изменяться в широких пределах, т.е. мицелла не имеет строго определенного состава.
Наличие одноименного заряда у всех гранул является важным фактором его устойчивости. Заряд препятствует слипанию и укрупнению коллоидных частиц. Если такой процесс наблюдается, то это происходит, в основном, вследствие уменьшения свободной поверхностной энергии, и называется он коагуляцией. Достигнув определенных размеров за счет укрупнения, частицы под действием силы тяжести оседают, наблюдается явление седиментации.
Реагент, который находится в избытке, выполняет функции стабилизатора коллоидной системы, а ядро – дисперсной фазы.
Установлено, что коагуляцию можно вызвать повышением температуры, механическим воздействием, высокочастотными колебаниями и т.д., а также введением специальных растворов электролитов. В последнем случае введенные ионы десольватируют ионы диффузионного слоя, способствуют переходу их в адсорбционный слой, при этом достигается полная электрическая нейтрализация гранул – изоэлектрическое состояние системы, и происходит сжатие диффузионного слоя и уменьшение сил электрического отталкивания, а силы межмолекулярного сцепления растут, что способствует слипанию и укрупнению частиц.
Кроме перечисленного выше, коагуляцию можно вызвать добавлением к одному золю другого с противоположным зарядом гранулы: происходит взаимная коагуляция и выпадают в осадок оба золя.
Начальная стадия коагуляции протекает незаметно и называется скрытой коагуляцией. Наименьшее количество электролита, которое вызывает начало явной (заметной) коагуляции, определяет порог коагуляции золя.
Коагулирующая способность электролитов (ионов) неодинакова и может быть определена как величина, обратная порогу коагуляции:
| КС = 1/ ПК, | (5.1) |
где КС – коагулирующая способность электролитов;
ПК – порог коагуляции, ммоль/л.
Согласно правилу Шульца-Гарди: чем выше заряд коагулирующего иона, тем больше выражена его коагулирующая способность, тем ниже порог коагуляции.
Коагулирующим действием обладает лишь тот ион электролита, который несет заряд, противоположный заряду гранулы.
Часто наблюдается процесс, обратный коагуляции – переход коагулята в золь, называемый пептизацией или дезагрегацией.
Связнодисперсные системы – гели – твердообразны. Они возникают при контакте частиц дисперсной фазы, приводящем к образованию структуры в виде каркаса или сетки. Такую систему можно рассматривать как дисперсную среду в дисперсной фазе. Подобные структуры ограничивают текучесть дисперсной системы и придают ей способность сохранять форму.
Переход золя в гель, происходящий в результате понижения устойчивости золя, называется гелеобразованием.
Пример 2. Мицелла золя гидроксида меди (II) имеет вид:
{m[Cu(OH)2]·nOH-·(n-x)Na+}x-·xNa+. Из приведенных ниже ионов составьте ряд ионов-коагуляторов для этой коллоидной системы: Fe3+; SiO32‾; РО43-; Сl-; К+; Сa2+; NО3-. Для какого из ионов порог коагуляции наименьший?
Решение. Согласно правилу Шульца-Гарди коагулирующей способностью для данной коллоидной системы обладают ионы Fe3+; К+; Сa2+, так как их заряды противоположны заряду гранулы. Если расположить данные ионы в порядке снижения коагулирующей способности, то этот ряд будет выглядеть следующим образом: Fe3+; Сa2+; К+. Соответственно, наименьший порог коагуляции имеет ион Fe3+.
Контрольные вопросы
301. Как представить условной химической формулой строение мицеллы, если: коллоидно-дисперсная фаза [FeS]m, ионный стабилизатор K2S → 2K+ + S2‾. Указать какой из приведенных ниже ионов наиболее эффективный коагулятор для этой коллоидной системы: Al3+, РО43-; Са2+, SiO32‾, ОН‾, Na+. Ответ обоснуйте.
302. Как представить условной химической формулой строение мицеллы золя, полученного в результате взаимодействия К2S c избытком ZnSO4? Какой из приведенных ионов будет наиболее подходящим коагулятором для этой коллоидной системы: Al3+, РО43-; Са2+, SiO32‾, ОН‾, Na+. Почему?
303. Как представить условной химической формулой строение мицеллы золя, полученного в результате взаимодействия AgNO3 c избытком КBr? Какой из приведенных ионов будет наиболее подходящим коагулятором для этой коллоидной системы: Al3+, РО43-; Са2+, SiO32‾, ОН‾, Na+. Почему?
304. Как представить условной химической формулой строение мицеллы золя, полученного в результате взаимодействия NaBr c избытком AgNO3? Какой из приведенных ионов будет наиболее подходящим коагулятором для этой коллоидной системы: Al3+, РО43-; Са2+, SiO32‾, ОН‾, Na+. Почему?
305. Как представить условной химической формулой строение мицеллы золя, полученного в результате взаимодействия FeCl3 c избытком KОН? Какой из приведенных ионов будет наиболее подходящим коагулятором для этой коллоидной системы: Al3+, РО43-; Са2+, SiO32‾, ОН‾, Na+. Почему?
306. Условная формула мицеллы золя кремниевой кислоты имеет вид:
{m[H2SiO3]·nSiO32-·2(n-x)K+}2x-·2xK+. Из приведенных ниже ионов составьте ряд ионов-коагуляторов для этой коллоидной системы: Fe3+; SiO32‾; РО43-; Сl-; К+; Сa2+; NО3-. Для какого из ионов порог коагуляции наименьший? Ответ обоснуйте.
307. Как представить условной химической формулой строение мицеллы золя, полученного в результате взаимодействия FeCl3 c избытком К2S? Какой из приведенных ионов будет наиболее подходящим коагулятором для этой коллоидной системы: Al3+, РО43-; Са2+, SiO32‾, ОН‾, Na+. Почему?
308. Условная формула мицеллы золя сульфата бария имеет вид:
{m[BaSO4]·nBa2+·2(n-x)Cl-}2x+·2xCl-. Какой золь из тех, чьи условные формулы приведены ниже, нужно добавить к данному золю, чтобы вызвать взаимную коагуляцию: {m[H2SiO3]·nSiO32-·2(n-x)K+}2x-·2xK+;
{m[Fe(OH)3]·nFeO+·(n-x)Cl-}x+·xCl-.
Ответ обоснуйте. Какой из приведенных ионов будет наиболее подходящим коагулятором для золя сульфата бария: Al3+, РО43-; Са2+, SiO32‾, ОН‾, Na+. Почему?
309. Условная формула мицеллы золя кремниевой кислоты имеет вид:
{m[H2SiO3]·nSiO32-·2(n-x)K+}2x-·2xK+. Какой золь из тех, чьи условные формулы приведены ниже, нужно добавить к данному золю, чтобы вызвать взаимную коагуляцию: {m[Cu(OH)2]·nOH-·(n-x)Na+}x-·xNa+;
{m[Fe(OH)3]·nFeO+·(n-x)Cl-}x+·xCl-.
Ответ обоснуйте. Какой из приведенных ионов будет наиболее подходящим коагулятором для золя кремниевой кислоты: Al3+, РО43-; Са2+, SiO32‾, ОН‾, Na+. Почему?
310. Условная формула мицеллы золя гидроксида меди (II) имеет вид:
{m[Cu(OH)2]·nOH-·(n-x)Na+}x-·xNa+. Какой золь из тех, чьи условные формулы приведены ниже, нужно добавить к данному золю, чтобы вызвать взаимную коагуляцию: {m[BaSO4]·nBa2+·2(n-x)Cl-}2x+·2xCl-;
{m[Fe(OH)3]·nFeO+·(n-x)Cl-}x+·xCl-.
Ответ обоснуйте. Какой из приведенных ионов будет наиболее подходящим коагулятором для золя гидроксида меди (II): Al3+, РО43-; Са2+, SiO32‾, ОН‾, Na+. Почему?
311. Какое строение будет иметь мицелла золя полученного в результате взаимодействия Na2SiO3 с избытком НС1? Какой из указанных ионов: C1-, Na+, А13+, Н+, SiO32- будет наиболее эффективным коагулятором для этой коллоидной системы? Почему?
312. Как представить условной химической формулой строение мицеллы золя, если коллоидно-дисперсная фаза [Fe(OH)3]m, а ионный стабилизатор FeOCl → FeO+ + Cl-?
Какой из приведенных ионов будет наиболее подходящим коагулятором для этой коллоидной системы: Cl‾, SO42‾, Na+, Fe2+, Fe3+? Ответ обоснуйте.
313. Как представить условной химической формулой строение мицеллы, если: коллоидно-дисперсная фаза [H2SiO3]m, ионный стабилизатор K2SiO3 → 2K+ + SiO32‾. Указать какой из приведенных ниже ионов наиболее эффективный коагулятор для этой коллоидной системы: Al3+, Са2+, SiO32‾, ОН‾, Na+. Ответ обоснуйте.
314. Как представить условной химической формулой строение мицеллы золя, полученного в результате взаимодействия Na2SiO3 c избытком Са(ОН)2?
Какой из этих ионов будет наиболее эффективным коагулятором для этой коллоидной системы: Al3+, Са2+, SiO32‾, ОН‾, Na+. Почему?
315. Мицелла золя гидроксида железа (III) имеет вид:
{m[Fe(OH)3]·nFeO+·(n-x)Cl-}x+·xCl-. Из приведенных ниже ионов составьте ряд ионов-коагуляторов для этой коллоидной системы: Fe3+; SiO32‾; РО43-; Сl-; К+; Сa2+; Cu2+. Для какого из ионов порог коагуляции наименьший? Ответ обоснуйте.
316. Как представить условной химической формулой строение мицеллы золя, полученного в результате взаимодействия Li2SiO3 c избытком HCl? Какой из приведенных ионов будет наиболее эффективным коагулятором для этой коллоидной системы: Al3+, РО43-; Са2+, SiO32‾, ОН‾, Na+. Почему?
317. Как представить условной химической формулой строение мицеллы золя, полученного в результате взаимодействия HCl c избытком AgNO3? Какой из приведенных ионов будет наиболее эффективным коагулятором для этой коллоидной системы: Al3+, РО43-; Са2+, SiO32‾, ОН‾, Na+. Почему?
318. Как представить условной химической формулой строение мицеллы золя, полученного в результате взаимодействия KОН c избытком Cu(NO3)2? Какой из приведенных ионов будет наиболее эффективным коагулятором для этой коллоидной системы: Al3+, РО43-; Са2+, SiO32‾, ОН‾, Na+. Почему?
319. Как представить условной химической формулой строение мицеллы золя, полученного в результате взаимодействия Na2S c избытком СuCl2? Какой из приведенных ионов будет наиболее эффективным коагулятором для этой коллоидной системы: Al3+, РО43-; Са2+, SiO32‾, ОН‾, Na+. Почему?
320. Как представить условной химической формулой строение мицеллы золя, полученного в результате взаимодействия Bа(ОН)2 c избытком К2SO4? Какой из этих ионов будет наиболее эффективным коагулятором для этой коллоидной системы: Al3+, РО43-; Са2+, SiO32‾, ОН‾, Na+. Почему?
Тема: s-Элементы (… ns 1-2)
Контрольные вопросы
321. Составьте электронные и молекулярные уравнения реакций: а) бериллия с раствором щелочи; б) магния с концентрированной серной кислотой, учитывая, что окислитель приобретает низшую степень окисления.
322. При сплавлении оксид бериллия взаимодействует с диоксидом кремния и с оксидом натрия. Напишите уравнения соответствующих реакций. О каких свойствах ВеО говорят эти реакции?
323. Какие соединения магния и кальция применяются в качестве вяжущих строительных материалов? Чем обусловлены их вяжущие свойства?
324. Как можно получить карбид кальция? Что образуется при его взаимодействии с водой? Напишите уравнения соответствующих реакций.
325. Как можно получить гидроксиды щелочных металлов? Почему едкие щелочи необходимо хранить в хорошо закрытой посуде? Составьте уравнения реакций, происходящих при насыщении гидроксида натрия а) хлором; б) оксидом серы SO3, в) сероводородом.
326. Чем можно объяснить большую восстановительную способность щелочных металлов. При сплавлении гидроксида натрия с металлическим натрием последний восстанавливает водород щелочи в гидрид-ион. Составьте электронные и молекулярное уравнения этой реакции.
327. Какое свойство кальция позволяет применять его в металлотермии для получения некоторых металлов из их соединений? Составьте электронные и молекулярные уравнения реакций кальция: а) с V205; б) с CaSO4,. В каждой из этих реакций окислитель восстанавливается максимально, приобретая низшую степень окисления.
328. Какие соединения называют негашеной и гашеной известью? Составьте уравнения реакций их получения. Какое соединение образуется при прокаливании негашеной извести с углем? Что является окислителем и восстановителем в последней реакции? Составьте электронные и молекулярные уравнения.
329. Составьте электронные и молекулярные уравнения реакций: а) кальция с водой; б) магния с азотной кислотой, учитывая, что окислитель приобретает низшую степень окисления.
330. Составьте уравнения реакций, которые нужно провести для осуществления следующих превращений:
Ca → CaH2 → Ca(OH)2 → CaCO3 → Ca(HCO3)2
331. Какую степень окисления может проявлять водород в своих соединениях? Приведите примеры реакций, в которых газообразный водород играет роль окислителя и в которых — восстановителя.
332. Напишите уравнения реакций натрия с водородом, кислородом, азотом и серой. Какую степень окисления приобретают атомы окислителя в каждой из этих реакций?
333. Напишите уравнения реакций с водой следующих соединений натрия: Na2О2, Na2S, NaH, Na3N.
334. Как получают металлический натрий? Составьте электронные уравнения процессов, проходящих на электродах при электролизе расплава NaOH.
335. Какие свойства может проявлять пероксид водорода в окислительно-восстановительных реакциях? Почему? На основании электронных уравнений напишите уравнения реакций Н2О2: а) с Аg2О; б) с К1.
336. Почему пероксид
 2015-10-22
2015-10-22 2204
2204
