4. Клиническая патофизиология под ред.В.А. Черешнева, П.Ф. Литвицкого, В.Н. Цыгана. – СПб: «СпецЛит», 2015. – 467с.
5. Литвицкий П. Ф. Патофизиология. В 2 т. Т. 1. — М.: ГЭОТАР-Медиа, 2015. — С. 35—58.
6. Литвицкий П. Ф. Клиническая патофизиология. — М.: Практическая медицина, 2015. — С. 60—68.
7. Патология / под ред. В. А. Черешнева, В. В. Давыдова. — М.: ГЭОТАР-Медиа, 2009. — Т. 1. — С. 48—52.
8. Зилбернагль С., Ланг Ф. Клиническая патофизиология. Атлас: пер. с англ. под ред. П. Ф. Литвицкого. — М.: Практическая медицина, 2015. — 437 с.
9. Практикум по патологической физиологии / под ред. В. Н. Цыгана, А. В. Дергунова, О. В. Леонтьева. — СПб.: Изд-во ВМА им. С. М. Кирова, 2015. — 240 с.
10. Леонтьев О. В., Дергунов А. В., Цыган В. Н. Курс лекций по патологической физиологии. — СПб.: ИнформМед. — 2014. — С. 97—111.
Глава 8. Воспаление
8.1. Введение[INN1]
8.2. Классификация и этиология воспаления слизистой оболочки полости рта (СОПР), тканей зубов и ЧЛО и шеи.
8.3. Патогенез воспаления СОПР, тканей зубов и ЧЛО и шеи.
8.3.1. Альтерация
8.3.2. Изменения обмена веществ
8.3.3. Расстройства периферического крово- и лимфообращения
8.3.3.1. Экссудация в очаге воспаления
8.3.3.2. Эмиграция в очаге воспаления
8.3.3.3. Фагоцитоз
8.3.4. Пролиферативные процессы в очаге воспаления
8.4. Медиаторы воспаления
8.4.1. Биологические эффекты медиаторов воспаления. Локальные (клеточные) медиаторы воспаления
8.4.2. Плазменные медиаторы воспаления
8.4.3. Промежуточные медиаторы воспаления
8.5. Влияние воспаления СОПР, тканей зубов и ЧЛО и шеи на организм[INN2]
8.6. Влияние реактивности организма на развитие воспаления СОПР, тканей зубов и ЧЛО и шеи
8.7. Роль нервной и эндокринной систем в развитии воспаления
8.8. Биологическое значение воспаления
8.9. Принципы профилактики и терапии воспаления СОПР, тканей зубов и ЧЛО и шеи
8.1. Введение
Термин «воспаление» происходит от лат. inflammatio и гр. phlogosis, что условно означает «воспламенение», «жар».
Известный русский патофизиолог В. В. Воронин, глубоко и всесторонне изучавший воспаление, писал: «Изучать литературу о воспалении — значило бы писать историю всей медицины».
Воспаление — одна из наиболее частых типовых форм реакций организма на действие разнообразных патогенных факторов.
Аналоги воспаления встречают на различных ступенях развития животного мира, но особой сложности и совершенства воспаление достигло у высших животных и человека.
Воспаление — основное проявление многих заболеваний, а локализация и характер воспалительного процесса в том или ином органе нередко определяет нозологическую форму и специфику болезни.
Для обозначения воспаления ткани или органа принято добавлять окончание «-ит» (-itis) к греко-латинскому названию ткани или конкретного органа (например, периодонтит, стоматит, гингивит, гепатит, миокардит, нефрит, колит, энцефалит, менингит, ринит, конъюнктивит, дерматит и т. д.). Реже воспалению дают специальное название (например, пневмония, абсцесс, флегмона и т. д.).
Важно отметить, что при воспалении организм жертвует местным (частью своих поврежденных клеточно-тканевых структур в очаге воспаления) ради сохранения целого (всего организма).
Согласно современной Международной анатомической и гистологической номенклатуре ВОЗ, структуры, которые окружают зуб и обеспечивают его соединение с челюстными костями, а именно:
• периодонтальная связка,
• цемент,
• костная ткань альвеолы,
• десна
В совокупности они именуются периодонтом.
В связи с этим воспалительное заболевание, поражающее эти структуры, согласно номенклатуре ВОЗ, называется периодонтитом. Между тем среди стоматологов России принято вышеперечисленную совокупность структур называть “пародонтом” и, соответственно, процесс, связанный с его воспалением, - пародонтитом.
В отечественной традиции термин периодонт применяют только к периодонтальной связке, а периапикальное воспаление называют периодонтитом.
Теории воспаления. В процессе развития человечества были предложены следующие различные теории происхождения, сущности и значения воспаления.
Согласно защитной теории Гиппократа (IV в. до н. э.), воспаление обеспечивает уменьшение распространения вредного агента по организму.
Теория Джона Гунтера (XVIII в.) рассматривала воспаление как обязательную реакцию организма на повреждение, при помощи которой поврежденная часть тела восстанавливает свои функции.
Согласно нутритивной теории Рудольфа Вирхова (1858) при воспалении отмечают избыточное питание поврежденных тканей — не только клеток, но и межклеточных структур, — приводящее к их гипертрофии и пролиферации.
Сосудистые теории Генле (1846), Брокса (1849) и более известная теория Юлиуса Конгейма (1867) демонстративно показали динамически развивающиеся при воспалении расстройства местного кровообращения, реакций сосудов, экссудации и эмиграции лейкоцитов.
Биологическая (эволюционная, фагоцитарная) теория И. И. Мечникова (1892), свидетельствующая о том, что в ответ на то или иное повреждение тканей, у организмов, находящихся на различных уровнях эволюционного развития обязательно, хотя и в разной степени, формируется реакция как кровяных, так и тканевых микро- и макрофагов.
Нервно-трофическая теория Самуэля (1873) и более известная нервно-сосудистая (вазомоторная) теория Г. Риккера (1924), согласно которой первичным в развитии воспаления считается нарушение функций сосудисто-двигательных нервов.
Физико-химическая (молекулярная) теория Г. Шаде (1923), согласно которой в очаге воспаления всегда развиваются ацидоз, осмотическая гипертензия, повышение онкотического давления и т.д.
Биохимическая (медиаторная) теория В. Менкина (1948), установившая наличие и разную роль в развитии воспаления флогогенных ФАВ (лейкотаксина, экссудина, фактора лейкоцитоза, пирексина и др.).
Иммунологическая теория XX века, рассматривающая воспаление как обязательную реакцию иммунной системы.
Динамическая теория А. Поликара (первая половина XX в.), вскрывшая динамику первичных, вторичных, васкулярных, плазматических, клеточных, нагноительных и восстановительных изменений в воспалительном очаге.
Существуют и другие теории, каждая из которых становилась для своего времени шагом вперед, поэтому критиковать их с позиций современного уровня знаний не следует. Можно лишь отметить, приемлема или нет та или иная теория воспаления сегодня.
Ниже будут рассмотрены современные взгляды на понятие, проявления, сущность, механизмы развития и значение воспаления для организма.
Местные признаки воспаления воспаления СОПР, тканей зубов и ЧЛО и шеи.
К ним относят пять основных признаков воспаления:
— краснота (rubor), развивающаяся в результате увеличения количества функционирующих сосудов (артериол и преимущественно капилляров), артериализации венозной крови, повышения содержания HbO2, имеющего ярко-алый цвет;
— припухлость (tumor), возникающая вследствие увеличения кровенаполнения тканей и формирования отека;
— жар (calor) — повышение температуры тканей, возникающее в результате увеличенного притока более горячей артериальной крови, а также вследствие активизации окислительных процессов;
— боль (dolor), появляющаяся вследствие раздражения болевых рецепторов (ноцицепторов) поврежденных тканей из-за сдавления их отеком, действия гипоксии, токсинов, различных физиологически активных гуморальных веществ;
— нарушение функции (functio laesa), всегда сопровождающее вовлечение в воспалительный процесс клеточно-тканевых структур организма.
Первые четыре признака (знаменитая тетрада) были описаны в I в. н. э. Цельсом в труде «О делах медицины». Пятый (ведущий) признак воспаления добавил во II в. н. э. врач римских гладиаторов Клавдий Гален. Он же впервые дал понятие о воспалении как о местной лихорадке.
Определение понятия «воспаление». Воспаление — сложный типовой патологический процесс, который:
— выработан в процессе эволюции (фило- и онтогенеза);
— генетически запрограммирован;
— имеет преимущественно защитно-адаптивное значение;
— возникает в ответ на действие различных повреждающих (флогогенных) факторов;
— включает комплекс преимущественно местных (а также общих) структурных, метаболических и функциональных, специфических и неспецифических, приспособительных и разрушительных изменений;
— характеризуется динамическими изменениями альтерации, обмена веществ, микроциркуляции с экссудацией, эмиграцией и фагоцитозом лейкоцитов и пролиферации;
— направлен на локализацию, уничтожение и удаление из организма флогогенного фактора, а также на ликвидацию неблагоприятных последствий его действия и восстановление поврежденных тканей.
8.2. Классификация и этиология воспаления
Воспаление, развивающееся в ответ на действие различных патогенных факторов и широко встречающееся при многообразных патологических процессах, патологических состояниях и заболеваниях СОПР, тканей зубов и ЧЛО и шеи, именуют патологическим.
Физиологическое воспаление возникает при некоторых физиологических процессах (менструациях, незначительных повреждениях как слизистых оболочек воспаления СОПР, тканей зубов и ЧЛО и шеи, так и пищеварительного тракта при приеме пищи, кожи при механической работе, мытье в бане, сауне).
Классификация патологического воспаления.
В зависимости от реактивности организма воспаление делят на адекватное (нормергическое) и неадекватное (гиперергическое) воспаление.
Гиперергическое воспаление возникает при различных видах сенсибилизации, аллергизации организма. В его основе лежит повышение возбудимости таких структур: нервной, мышечной, железистой тканей), а также усиление процессов возбуждения и ослабление процессов торможения различных нейронов центральной и периферической нервной системы. Гипергическое воспаление возникает при наркозе, сне, депрессиях, лучевой болезни, старении организма, развитии дистрофических и опухолевых процессов, кахексии. В его основе лежит снижение чувствительности возбудимых тканей, ослабление процессов возбуждения и усиление процессов торможения в нервной системе, угнетение активности эндокринной, иммунной, мышечной, сердечно-сосудистой и других систем.
По биологическому значению для организма воспаление бывает положительным (защитно-приспособительным) и отрицательным (патологическим).
По характеру и степени изменений воспаление делят на специфическое (при туберкулезе, брюшном тифе, дизентерии) и неспецифическое (при банальной инфекции).
В зависимости от превалирования того или иного компонента (основного процесса) различают следующие виды воспаления:
— альтеративное — превалируют явления повреждения СОПР, тканей зубов и ЧЛО и шеи;
— экссудативное — превалируют нарушения микроциркуляции и экссудация в СОПР, тканях зубов и ЧЛО и шеи;
— пролиферативное — превалируют процессы размножения клеток, особенно соединительной ткани; образуется новая ткань в СОПР, тканях зубов, ЧЛО и шеи.
В зависимости от вида экссудата воспаление бывает:
— серозное;
— фибринозное;
— геморрагическое;
— гнилостное;
— гнойное;
— смешанное.
По клиническому течению (скорости развития и длительности течения) воспаление делят на острое (до 1 мес), подострое (до 3—6 мес), хроническое (более 6 мес).
Исходы воспаления могут быть самыми различными:
— выздоровление (возврат к норме) с полным или неполным восстановлением поврежденных структур, метаболизма и функций СОПР, тканей зубов, органов, тканей ЧЛО и шеи (например, частичная или полная замена поврежденного эпителия образовавшимся соединительно-тканевым рубцом);
— переход острого воспаления в хроническое;
— переход одного воспалительного заболевания в другое;
— обратимая гибель клеток (некоторые виды углеводной, жировой, белковой дистрофии, паранекроз СОПР, тканей зубов и ЧЛО, шеи);
— необратимая гибель клеток (гидропическая дистрофия, некробиоз, некроз) этих областей;
— гибель всего организма.
Повреждение тканей и последствия при воспалении показаны на рис. 8.1.
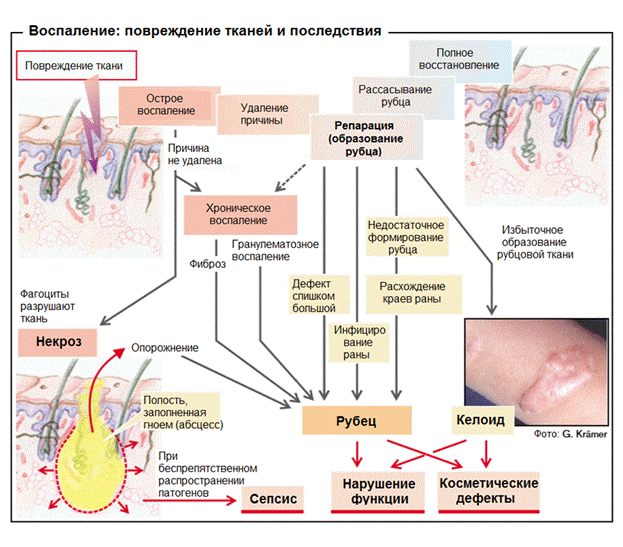
(верстальщику - убрать надпись Воспаление: повреждение тканей и последствия с самого рисунка)
Рис. 8.1. Воспаление: повреждение тканей и последствия
(Зильбергналь С., Ланг Ф. Клиническая патофизиология. Атлас. М., 2015. С. 55)
Этиология воспаления. Воспаление формируется преимущественно как местная, реже как общая реакция организма на патогенный (флогогенный) раздражитель и вызываемые им повреждения.
По происхождению флогогенные раздражители делят на две группы: экзогенные и эндогенные.
Экзогенные факторы могут быть инфекционной и неинфекционной природы. Инфекционные факторы — вирусы, микоплазмы, риккетсии, бактерии, простейшие, паразиты. Неинфекционные факторы — физические (механические, термические, электрические, радиационные), химические (неорганические и органические кислоты, щелочи и др.), биологические (яды насекомых, змей, растений, чужеродные белки), психогенные (характерные преимущественно для человека).
Эндогенные факторы представлены продуктами распада и нарушенного метаболизма тканей, а также отложениями солей, кровоизлияниями, тромбами, эмболами, доброкачественными и злокачественными опухолями, сапрофитной микрофлорой СОПР, тканей зубов и ЧЛО, шеи.
8.3. Патогенез воспаления СОПР, тканей зубов и ЧЛО, шеи
Виды, характеристика и биологическое значение основных процессов (компонентов) воспаления. Независимо от вида флогогенного раздражителя в развитии воспалительной реакции роль играет совокупность процессов (развивающихся одновременно и тесно взаимосвязанных между собой), называемых компонентами воспаления (см. рис. 8.2.). К таким процессам относят:
— альтерацию (от лат. alteratio — изменение) — раздражение, разрушение;
— изменение обмена веществ в очаге воспаления;
— нарушение периферического кровообращения, микроциркуляции и лимфообращения, которое сопровождается:
• экссудацией (от лат. exudatio) — выпотеванием воспалительной жидкости;
• эмиграцией (от лат. emigrare — выселением) — выходом клеток крови из просвета сосудов в очаг повреждения;
• фагоцитозом (phagocytosis от гр. phagein + kytos + os), т. е. захватыванием, поглощением и перевариванием инородных образований макрофагами и микрофагами (в основном моноцитами и нейтрофилами);
— пролиферацию (proliferatio, от лат. proles — потомство + fero — приношу) — размножение клеток, главным образом соединительной и эпителиальной тканей.

Рис. 8.2. Патогенез острого воспаления
(Зильбергналь С., Ланг Ф. Клиническая патофизиология. Атлас. М., 2015. С. 53)
8.3.1. Альтерация СОПР, тканей зубов, ЧЛО и шеи.
Термин «альтерация» означает раздражение и повреждение рецепторов, мембран, внутриклеточных органелл (особенно ядер, лизосом, митохондрий), целых клеток, межклеточного вещества, периферических (особенно терминальных), кровеносных и лимфатических сосудов.
Альтерация — первое и непосредственное следствие действия флогогенного и патогенетических факторов на СОПР, ткани зубов,ЧЛО и шеи.
Она включает комплекс обменных, физико-химических, структурных и функциональных изменений в поврежденных и близлежащих тканях СОПР, тканей зубов, ЧЛО и шеи.
Морфологически она проявляется различными формами и степенями дистрофии, паранекроза, некробиоза, некроза.
Альтерация, как правило, становится пусковым звеном патогенеза развития различных патологических процессов, состояний и болезней СОПР, тканей зубов, ЧЛО и шеи.
Различают два вида альтерации: первичную и вторичную.
Первичная альтерация возникает в ответ на прямое действие воспалительного (флогогенного) фактора и пролонгирует его патогенное действие. Степень и характер альтерации зависит от интенсивности и качества флогогенного фактора, а также от локализации и площади повреждения, реактивности и резистентности поврежденных структур СОПР, тканей зубов, ЧЛО, шеи и организма в целом.
Вторичная альтерация возникает под влиянием различных патогенетических факторов: как местных изменений СОПР, тканей зубов, ЧЛО и шеи (физико-химических факторов, количества и активности медиаторов воспаления, сосудистых реакций и др.), так и системных (нервной и гуморальной, в том числе эндокринной и иммунной) реакций.
Соотношение выраженности первичной и вторичной альтерации может быть различным. Это соотношение обусловлено объемом и характером ткани, главным образом количеством вовлеченных в патологический процесс сосудов (кровеносных и лимфатических) и нервных структур. Обычно чем больше первичная альтерация, тем больше и вторичная. Но при чрезмерно выраженной первичной альтерации (глубокий некроз, обугливание, промерзание) вторичная альтерация может быть выражена не в большей, а в такой же или даже значительно меньшей степени.
Наиболее выражены процессы альтерации в паренхиматозных органах, а также в коже и слизистых (при вовлечении их в аллергические реакции). По мере развития воспаления в очаге первичного повреждения и прилегающих к нему участках ткани развиваются нарушения кровообращения, нервной трофики, гипоксия, ацидоз, появляются токсины. Эти изменения — важные патогенетические факторы, вызывающие новую волну альтерации (т. е. вторичную).
Особое значение в развитии альтерации придают соединительной ткани, состоящей из основного вещества и клеток. Воспаление характеризуется качественным изменением основного вещества, проявляющимся в повышении дисперсности коллоидов и их способности к набуханию. Краситель (например, тушь), в норме проникающий в соединительную ткань только под давлением, при воспалении легко распространяется по поврежденной ткани. Это связано с действием гидролитических ферментов и гиалуронидазы, которые значительно повышают проницаемость соединительной ткани.
Ацидоз и активизация протеаз, липаз, гликозидаз и др. гидролаз способствуют диссоциации органических кислот и слабых оснований (это приводит к увеличению в очаге воспаления осмотического давления). Одновременно наблюдают распад крупных белковых молекул на мелкие, выход белков из крови (в результате увеличения проницаемости стенок сосудов), изменение физико-химических свойств соединительной ткани и т. д. Все это увеличивает не только осмотическое, но и онкотическое давление, гидрофильность тканевых структур. Следует отметить, что центр воспаления — это не центр повреждения (не участок некроза), а периферия поврежденного участка ткани.
Воспаление развивается не в мертвой, а в поврежденной, еще живущей и кровоснабжаемой ткани.
8.3.2. Изменения обмена веществ
Первичная и особенно вторичная альтерации сопровождаются возникновением комплекса разнообразных структурных, физико-химических, обменных и функциональных изменений как в поврежденных структурах СОПР, тканей зубов, ЧЛО, шеи, так и вокруг них.
Альтерация — пусковой механизм развития ниже перечисленных изменений, развивающихся по типу цепной реакции.
Комплекс структурных изменений разнообразен, он проявляется на различном уровне организации организма и обычно включает деструкцию следующих структур СОПР, тканей зубов, ЧЛО, шеи:
— микрососудов (капилляров, пре- и посткапилляров, сфинктеров, артериол, венул, артериоло-венулярных шунтов);
— соединительной ткани (волокон, межклеточного вещества, клеток), эндотелиоцитов, нервных, эпителиальных, тучных клеток и клеток крови;
— протоплазмы, ядер, различных органелл клеток (особенно лизосом, митохондрий, рибосом, эндоплазматического ретикулума);
— клеточных мембран и мембран органелл;
— транспортных каналов для ионов Na+, Ka+, Ca+2, Cl– и других; углеводов, липидов, белков, ФАВ и т.д.;
— пиноцитозных пузырьков (везикул), ответственных за транспорт разных веществ.
Комплекс физико-химических изменений включает следующие изменения СОПР, тканей зубов, ЧЛО, шеи, как правило, нарастающие в динамике воспалительного процесса:
— ацидоз (снижение рН);
— гиперионию (увеличение количества Na+, K+, Ca+2, Cl–, HPO4– и др.);
— дисионию (увеличение внеклеточного K+ и внутриклеточного Na+);
— гиперосмию (увеличение осмотического давления);
— гиперонкию (увеличение онкотического давления);
— увеличение дисперсности и гидрофильности белков паренхиматозных, нервных и, особенно, соединительнотканных структур и т. д.
Физико-химические изменения в очаге воспаления играют большую роль в увеличении образования и изменения активности медиаторов воспаления.
Комплекс метаболических изменений возникает вследствие как структурных, так и физико-химических изменений, главным образом митохондрий и лизосом клеток.
Он включает следующие процессы:
— активацию катаболизма белков, липидов, углеводов и их соединений;
— торможение анаболических процессов;
— усиление аэробного и особенно анаэробного гликолиза;
— усиление тканевого дыхания, сменяющегося его снижением;
— активацию процесса окислительного фосфорилирования (сопровождающегося увеличением синтеза макроэргов), сменяющегося его снижением и разобщением (при этом нарастает дефицит АТФ);
— усиление процесса теплопродукции, сменяющегося его ослаблением;
— накопление разнообразных недоокисленных продуктов метаболизма (вследствие повышения содержания лактата, пирувата, кетоновых тел и др.).
Большинство из перечисленных выше метаболических изменений способствует активизации образования медиаторов воспаления.
Комплекс функциональных изменений прямо зависит от степени и характера структурных, физико-химических и метаболических расстройств. Он включает разнообразные защитно-компенсаторно-приспособительные и патологические изменения функций как поврежденных, так и неповрежденных структур (клеток и межклеточного вещества) практически всех (соединительной, эпителиальной, мышечной и нервной) тканей, особенно клеток крови, эндотелиоцитов, тучных и других клеток.
8.3.3. Расстройства периферического крово-и лимфообращения СОПР, тканей зубов, ЧЛО, шеи
Наиболее часто в очаге воспаления встречают следующую динамическую последовательность реакций кровеносных сосудов.
1. Спазм артериол, приводящий чаще к временной, иногда — к длительной ишемии (вплоть до прекращения кровотока, т. е. может завершиться ишемическим стазом). Спазм обусловлен увеличением тонуса вазоконстрикторов, имеющего рефлекторный генез. Он приводит к невозможности проникновения повреждающих факторов (микробов, токсинов и др.) в кровоток и распространения с ним по организму.
2. Артериальная гиперемия в динамике воспаления может иметь различный механизм развития:
— рефлекторный;
— нейротонический (в основе и того, и другого механизма лежит преобладание тонуса вазодилататоров над вазоконстрикторами);
— гуморально-метаболический (увеличение образования недоокисленных продуктов и вазодилататорных ФАВ);
— нейропаралитический (паралич сосудосуживающих либо и сосудосуживающих, и сосудорасширяющих нервных волокон);
— миопаралитический (паралич гладких мышц сосудов).
3. Венозная гиперемия в динамике воспаления возникает вследствие несоответствия между притоком и сниженным оттоком крови под влиянием следующих различных механизмов:
— нарушение структуры вен;
— паралич нервно-мышечного аппарата вен;
— сдавление вен образующимся и нарастающим экссудатом;
— увеличение общей площади сосудистого русла;
— активация процессов адгезии, агрегации и агглютинации тромбоцитов, лейкоцитов и эритроцитов, особенно в венозных микрососудах;
— микротромбообразование (на внутренних стенках вен);
— увеличение проницаемости сосудистой стенки микрососудов (для воды, солей, макро- и микроэлементов, ФАВ, витаминов, углеводов, липидов, белков);
— сгущение и увеличение вязкости крови и т. д.
На фоне венозного застоя формируется престатическое состояние (сначала толчкообразное, потом маятникообразное движение крови), а затем — стаз.
4. Венозный стаз завершает венозную гиперемию и характеризуется полной остановкой кровотока в венах.
5. Истинный стаз может развиваться на различных стадиях воспаления.
6. Лимфообразование и лимфоотток в динамике воспаления сначала (при артериальной гиперемии) временно активизируются, а при венозной гиперемии — снижаются. Эти расстройства становятся максимальными при стазе (как венозном, так и истинном). Давление лимфы может увеличиваться до 120 мм вод. ст. Большое количество лимфатических сосудов закупоривается белками, хиломикронами, клетками и различными обломками тканей.
8.3.3.1. Экссудация в очаге воспаления в СОПР, тканях зубов, ЧЛО и шеи
Экссудация — процесс выхода воспалительной жидкости (экссудата) из крови в ткани.
Если в норме капиллярная стенка удерживает в крови 95 % белков, то при воспалении проницаемость для белков сосудистых стенок (капилляров, прекапиллярных артериол и посткапиллярных венул) возрастает в 3—7 раз и более.
В динамике экссудации сначала увеличивается выход воды, потом солей, затем углеводов и, наконец, липидов и белков (альбуминов,: альфа-, Р-, гама-[INN3] глобулинов) и их комплексных соединений.
Экссудат — воспалительная жидкость (основа воспалительного отека), содержащая 2—3 % белков (главным образом высокомолекулярных), форменные элементы крови (в основном лейкоциты, а также тромбоциты и эритроциты), ферменты и соли.
Транссудат отличается от экссудата меньшим количеством (менее 2 %) и меньшей молекулярной массой белков, а также меньшим содержанием лейкоцитов, тромбоцитов, эритроцитов, ферментов и солей.
Виды экссудата определяются его составом. Различают серозный, фибринозный, геморрагический, гнойный, гнилостный и смешанный экссудаты.
Серозный экссудат содержит более 2—3 % белков, значительное количество различных клеток, рН составляет 6—7 и более, удельный вес — 1,108 и выше.
Фибринозный экссудат содержит большое количество белков, особенно фибриногена и фибрина.
Геморрагический экссудат содержит белки и различные клетки крови, особенно эритроциты.
Гнойный — огромное количество белков (до 6—8 %), погибших лейкоцитов (главным образом нейтрофилов) и клеток поврежденных тканей, а также микроорганизмы.
Гнилостный — большое количество белков, погибших клеток тканей и очень много анаэробных гнилостных микроорганизмов.
Смешанный экссудат предоставлен разным сочетанием перечисленных выше видов экссудатов.
В зависимости от вида экссудата различают соответствующие виды экссудативного воспаления.
Основные патогенетические факторы экссудации
В образовании воспалительной жидкости (экссудата) участвуют следующие основные патогенетические факторы.
Тканевой фактор — повышение коллоидно-осмотического давления тканей (т. е. увеличение онкотического и осмотического давления тканей, возникающее в результате распада крупных молекул белков на мелкие, диссоциации органических кислот и слабых оснований, увеличения дисперсности клеточно-тканевых структур, ацидоза, повышения количества и активности протеаз и других гидролитических ферментов).
Мембранный (сосудистый) фактор — повышение проницаемости мембран микрососудов (обусловленное истончением и повреждением базальной мембраны и клеток эндотелия, увеличением межэндотелиальных щелей и каналов эндотелиоцитов) за счет увеличения количества вазоактивных ФАВ (гистамина, серотонина, кининов, глобулинов проницаемости и др.). Проницаемость стенок микрососудов повышается в результате как пассивного, так и активного транспортирования различных веществ.
Гемодинамический фактор — повышение гидростатического давления сначала в артериальной, а затем в венозной части капилляров. Увеличение фильтрации начинается при артериальной гиперемии и нарастает при венозной.
Следует отметить, что снижение онкотического давления крови в генезе экссудации практического значения не имеет.
Основные пути экссудации. Выделяют следующие основные виды транспорта экссудата:
— межэндотелиальный пассивный (в связи с изменением формы и размеров эндотелиоцитов и увеличением межэндотелиальной щели);
— трансцеллюлярный пассивный (в связи с расширением клеточных пор);
— трансцеллюлярный активный (с участием как переносчиков без затраты энергии, так и насосов, работающих с затратой энергии АТФ, АДФ, КРФ).
Значение экссудации. Значение экссудации может быть адаптивным и патологическим.
Адаптивное значение экссудации заключается:
— в разбавлении (уменьшении концентрации) и ослаблении действия флогогенного агента на организм;
— удалении из крови метаболитов и токсинов (а значит, в снижении их повреждающего действия на организм) в результате исключения их из крово- и лимфообращения;
— ферментативной и неферментативной нейтрализации микробов, детритов, токсинов вследствие увеличения их адсорбции поврежденными структурами;
— бактерицидном и бактериостатическом действии ацидоза (кислых продуктов), а также ФАВ экссудата (например, лизоцим, β-лизины, факторы системы комплемента);
 2017-11-30
2017-11-30 595
595








