Два элемента Х и Y, принадлежащие одной группе периодической системы элементов, образуют гидриды, имеющие одинаковую массовую долю водорода – 5.9%. При взаимодействии этих гидридов образуются два вещества – простое вещество желтого цвета, образованное элементом Х, и гидрид элемента Y, содержащий 11.1% водорода по массе.
Определите элементы и формулы упомянутых гидридов. Подтвердите ответ расчетом.
Травление металла
В раствор соляной кислоты погрузили металлическую пластинку массой 50 г. В результате реакции выделилось 1 л газа (н.у.), а масса пластинки уменьшилась на 4,99 %. Из какого металла была сделана пластинка?
Анализ смеси углеводородов
На сжигание 25 мл смеси метана и этана взяли 90 мл кислорода. После реакции объем смеси углекислого газа и кислорода составил 60 мл. Определите состав исходной смеси в мольных %. Учтите, что объемы всех газов (газовых смесей) измеряли при одних и тех же условиях (не обязательно н.у.!).
Теплота нейтрализации
При взаимодействии водных растворов, содержащих 36,5 г хлороводорода и 40 г гидроксида натрия, выделилось 57 кДж тепла.
1. Напишите полное и сокращенное ионное уравнения реакций.
2. Сколько тепла выделится при взаимодействии 150 г 10%-ного раствора серной кислоты и 50 г 11,2%-ного раствора гидроксида калия?
Теплоту считаем для сокращенного ионного уравнения (нейтрализация сильной кислоты и сильного основания)
Правые части с коэффициентами
Восстановите левую часть уравнений
· … + … = Cr2O3 + KCl
· … + … = N2 + 4H2O
· … + … + … = 4CaCrO4
· … + … + … = N2 + 3CO2 + K2S
· … + … = K4[Fe(CN)6] + 2KCl
Ответы
· Cr + KClO3 = Cr2O3 + KCl
· N2H4 +2 Н2О2= N2 + 4H2O
· 4Ca + 2Cr2O3 + 5O3= 4CaCrO4
· 2KNO3 + 3C + S = N2 + 3CO2 + K2S
· FeCl2 + 6KCN(конц.)= K4[Fe(CN)6] + 2KCl
Завод в пробирке
Юные химики решили в лаборатории воспроизвести промышленный способ получения вещества Z. Для этого они собрали установку, представленную на рисунке.
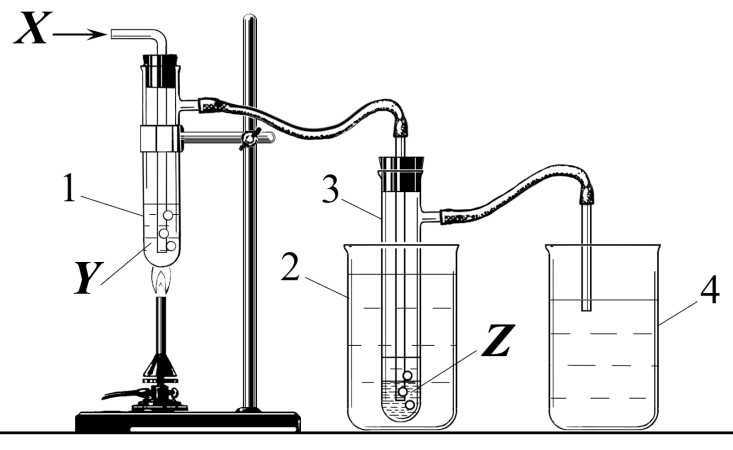
В пробирку (1) они налили насыщенный раствор некоторой соли Y и нагрели. Через горячий раствор пропустили ток газа X желто-зеленого цвета. Летучие вещества, выделяющиеся из реактора, конденсировали в пробирке-приемнике (3), которая была опущена в стакан (2) с холодной водой. Через некоторое время на дне приемника начала конденсироваться тяжелая жидкость Z, имеющая красно-бурую окраску. Известно, что соль Y окрашивает пламя в желтый цвет.
А. Какие вещества зашифрованы буквами X, Y и Z? Ответ поясните и проиллюстрируйте соответствующим уравнением реакции.
Б. Как в промышленности получают вещество Z?
В. Газоотводную трубку от пробирки (3) опустили в стакан (4), заполненный некоторой жидкостью. С какой целью это сделали? Какую жидкость лучше использовать для достижения поставленной цели? Ответ подтвердите соответствующими уравнениями.
11 класс
Элементы-соседи
Два элемента, находящиеся в одном и том же периоде и в одной и той же группе периодической системы (в ее коротком варианте), образуют друг с другом единственное стабильное бинарное соединение с массовой долей одного из элементов 25,6%. Это соединение хорошо растворимо в воде, а при пропускании в его раствор газообразного аммиака выпадает белый осадок, постепенно темнеющий на воздухе. Назовите элементы, определите формулу вещества и напишите уравнения реакций.
2. Газ из парафина
Один из удобных лабораторных способов получения газа Х (плотность по воздуху 1,17) состоит в нагревании смеси парафина с серой до температуры 150-200 оС. Реакция между компонентами смеси протекает спокойно и в любой момент может быть прекращена ее охлаждением. Другим продуктом происходящей реакции является черное вещество Y, нерастворимое в разбавленных кислотах и щелочах, но растворяющееся в концентрированных азотной и серной кислотах.
а) Определите вещества Х и Y и напишите уравнение реакции парафина с серой. Формулу парафина используйте в общем виде – C n H2 n +2.
б) Сделав разумные допущения, оцените, сколько литров Х (при н.у.) можно получить из 1 г стехиометрической смеси парафина с серой.
 2017-11-30
2017-11-30 987
987








