Механизм действия местных анестетиков связывают с влиянием на функциональное состояние чувствительных (афферентных) нервных окончаний и проводников, имеющих в мембране натриевые каналы. Мембранный потенциал покоя поддерживается активным транспортом и пассивной диффузией ионов в нервных клетках. Натрий-калиевый насос обеспечивает выход ионов натрия из клетки и вход в клетку ионов калия. В механизме действия может также иметь значение и антагонизм местных анестетиков с ионами кальция, влияющими на функционирование ионных каналов. Повышение содержания внеклеточного кальция может снижать действие местных анестетиков. При стимуляции нервного волокна происходит деполяризация клеточной мембраны, ионы натрия поступают в клетку, изменяется мембранный потенциал, обуславливающий распространение импульса по аксону. Местные анестетики, проникая через мембрану чувствительных нервных окончаний или волокон, взаимодействуют с рецепторами натриевых каналов, расположенными на внутренней стороне мембраны. Они оказывают влияние на физико-химические свойства и электрохимические процессы в мембране (поверхностное и межфазное натяжение, межфазный потенциал), изменяют ее проницаемость для ионов (особенно натрия), угнетают поток ионов по потенциалзависимым натриевым каналам, препятствуют генерации потенциала действия и его распространению по нервным волокнам, уменьшают возбудимость, снижают скорость и степень деполяризации. Являясь блокаторами натриевых каналов, местные анестетики сохраняют потенциал покоя и пороговый потенциал, но нарушают возникновение и распространение потенциала действия, снижают возбудимость нервных окончаний, стабилизируют потенциал мембраны, нарушая проведение импульсов по периферическому нерву с места болезненных манипуляций в центральную нервную систему и уменьшая центральный ответ на стимуляцию нерва, что приводит к временной утрате чувствительности. При окончании действия местных анестетиков функция чувствительных нервных окончаний и проводников полностью восстанавливается.[14]
Местные анестетики могут оказывать влияние на проведение возбуждения по чувствительным, вегетативным и двигательным волокнам. Последовательность и степень блокады нейронов зависят от гистоморфологической структуры нервных волокон (диаметра, типа и степени их миелинизации). Неодинаковая чувствительность к местным анестетикам основных проводников сенсорной информации (периферических нервных волокон группы А и С) обуславливает дифференцированную блокаду волокон, несущих специфическую функциональную нагрузку.
Наиболее чувствительны к действию анестетиков тонкие немиелинизиро- ванные волокна группы С, стимуляция которых сопровождается нестерпимой, плохо локализованной болью с выраженным эмоциональным переживанием, и тонкие миелинизированные волокна (группы А5), при возбуждении которых возникает кратковременная приступообразная точно локализованная боль без выраженных эмоциональных реакций. Толстые миелинизированные волокна (группа АВ), идущие к скелетным мышцам, тактильным рецепторам и пропри- орецепторам, более устойчивы к действию местных анестетиков.
Угнетая тонкие немиелинизированные и миелинизированные волокна, местные анестетики снимают, прежде всего, болевую, затем - вкусовую, температурную и тактильную чувствительность. Полное обезболивание, т. е. анестезия, достигается при блокаде проведения возбуждения по всем группам сенсорных волокон.
Поскольку волокна, идущие к тактильным рецепторам и проприорецепторам скелетных мышцх, более устойчивы к действию местных анестетиков, иногда ощущение прикосновения и давления на ткани полностью не снимается даже при хорошо проведенной местной анестезии, и пациенты, особенно эмоционально лабильные, воспринимают его как болевое. В этом случае врач должен объяснить пациенту, почему сохраняется тактильная чувствительность (например, при отделении гладилкой корня при операции удаления зуба). Проведение импульсов по двигательным нервам обычными дозами местных анестетиков полностью не блокируется.
Местные анестетики могут вмешиваться в передачу импульсов в любой возбудимой ткани, в связи с чем после их всасывания в кровь возможно развитие системного, в том числе и токсического действия. Наиболее чувствительны к действию местных анестетиков ЦНС и сердечно-сосудистая система.
Проникая через гематоэнцефалический барьер, местные анестетики могут вызывать кратковременное возбуждение ЦНС (беспокойство, тремор), сменяемое ее угнетением, нарушением кровообращения и дыхания. Блокируя натриевые каналы проводящей системы сердца, они оказывают влияние на автоматизм, на проводимость и сократимость миокарда в степени, пропорциональной их анестезирующей активности и дозе. Это позволило использовать системное действие лидокаина при оказании неотложной помощи пациентам с желудочковыми аритмиями. Однако при повышении концентрации местные анестетики могут вызывать развитие сердечных аритмий.
Изучение механизма действия на молекулярном уровне выявило влияние химической структуры и физико-химических свойств (молекулярный вес, рКа - константа диссоциации, жирорастворимость, связывание с белками) местных анестетиков на эффективность и безопасность местного обезболивания.
В молекулярной структуре местных анестетиков имеется 3 основных компонента: ароматическая группа (или тиофеновое кольцо), промежуточная цепочка и аминогруппа (рис.1). Ароматическая группа, обладающая липофильностью, координирует пассивную диффузию анестетика через нейрональную мембрану; аминогруппа, содержащая вторичный или третичный атом азота, обеспечивает гидрофильность анестетика и взаимодействие его с белком-рецептором, расположенным на внутренней поверхности мембраны нервного волокна; промежуточная алифатическая цепочка, построенная по типу сложных эфиров или амидов, соединяет липофильную и гидрофильную части молекулы.
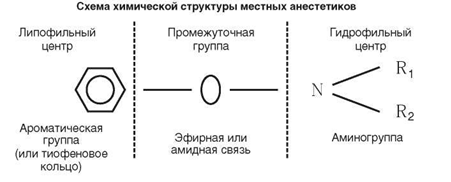
Рис. 1. Схема химической структуры местных анестетиков
Классификация местных анестетиков
По химической структуре (в зависимости от структуры промежуточной цепочки)
• Сложные эфиры: бензокаин (анестезин), прокаин (новокаин), тетракаин (дикаин).
• Амиды: артикаин (альфакаин, артикаин, артикаин ДФ, артикаин ИНИБСА, артикаин Перрель. Артифрин, брилокаин, примакаин, септанест, уби- стезин, ультракаин, цитокартин), бупивакаин (маркаин), лидокаин, (кси- каин, ксилокаин, лигнокаин), мепивакаин (мепивастезин, мепидонт, скандонест), ропивакаин (наропин), тримекаин.
По длительности действия:
1. Короткого действия - до 30-40 минут (прокаин).
2. Средней продолжительности действия - 45-90 минут (артикаин, лидока- ин, мепивакаин, тримекаин).
3. Длительного действия - до 90 минут и более (бупивакаин, ропивакаин)
По способу применения:
1. Для поверхностной (терминальной, аппликационной) анестезии: бензокаин, лидокаин, тетракаин.
2. Для инфильтрационной и проводниковой анестезии: артикаин, бупивакаин, лидокаин, мепивакаин, прокаин, ропивакаин, тримекаин.
3. Для интралигаментарной, внутрипульпарной, интрасептальной, внутри- костной анестезии: артикаин, лидокаин, мепивакаин.
К местным анестетикам предъявляют определенные требования: они должны обладать хорошей диффузионной способностью, высокой местнообезболивающей активностью, иметь короткий латентный период и достаточную продолжительность действия, выраженную избирательность и обратимость действия на нервные окончания и волокна, максимально эффективно устранять болевую чувствительность в области вмешательства, не раздражать и не повреждать ткани в месте введения, не оказывать системного воздействия на организм, быть стабильными при стерилизации и хранении. Идеального местного анестетика, соответствующего все этим требованиям, нет. На сегодняшний день препаратами выбора для инъекционной анестезии в стоматологии являются препараты, создаваемые на основе 3 местных анестетиков - лидокаина, артикаина и мепивакаина. Эти препараты обеспечивают быстрое начало анестезии, достаточную глубину и продолжительность обезболивания. Они превосходят прокаин (новокаин) по анестезирующей активности в 2-4 раза, действуют длительнее, реже дают аллергические реакции.[3]
При выборе местноанестезирующего препарата врач должен внимательно изучить его состав, учитывая не только механизм действия, фармакодинамику, побочные эффекты, показания и противопоказания к применению входящих в его состав компонентов, но и особенности их химической структуры, физикохимических свойств, фармакокинетики и возможность взаимодействия с применяемыми пациентом лекарствами.
От химической структуры зависят скорость наступления и длительность действия местных анестетиков, особенности их метаболизма в организме, выраженность побочных эффектов, аллергогенность. В процессе биотрансформации местных анестетиков могут образовываться метаболиты, обладающие определенной степенью активности и токсичности, что следует учитывать при выборе препарата, особенно при работе с пациентами, имеющими сопутствующие заболевания.
Эфирные связи нестойки, поэтому местные анестетики группы сложных эфиров быстро разрушаются эстеразами в тканях и крови (в том числе бутирилхоли- нэстеразой или псевдохолинэстеразой) и действуют коротко. При наличии в крови атипичной псевдохолинэстеразы нарушение гидролиза местных анестетиков группы сложных эфиров приводит к повышению их концентрации в крови, удлинению анестезии, увеличению потенциальной токсичности, что следует учитывать при выборе препаратов для проведения обезболивания. У новорожденных детей активность ферментов ниже, чем у взрослых, что необходимо учитывать при выборе для них анестетиков. Препараты группы сложных эфиров имеют короткий срок хранения из-за тенденции к спонтанному гидролизу, особенно при нагревании.[12]
Местные анестетики группы амидов (артикаин, лидокаин, мепивакаин, бупивакаин, ропивакаин, тримекаин) метаболизируются в основном микросомальными ферментами печени и действуют более длительно (таб. 1, 2). Сначала происходит N-дезалкилирование их аминоокончаний, образующийся при этом вторичный амин большинства амидов подвергается гидролизу, но может происходить конъюгация, гидроксилирование или дальнейшее их дезалкилирование. При патологии печени метаболизм этих препаратов может нарушаться.
Таблица 1Классификация местных анестетиков по длительности действия
| Длительность действия, мин. | Препараты | |
| Местные анестетики короткого действия | 30-40 | Прокаин |
| Местные анестетики средней продолжительности действия | 45-90 | Артикаин, лидокаин, мепивакаин, тримекаин |
| Местные анестетики длительного действия | Более 90 | Бупивакаин ропивакаин |
В процессе биотрансформации местных анестетиков группы амидов (например, лидокаина) могут образовываться фармакологически активные и/или токсичные метаболиты. Хотя артикаин является анестетиком группы амидов, наличие дополнительной эфирной связи обуславливает биотрансформацию его не только ферментными системами печени, но и эстразами тканей и крови с образованием неактивной артикаиновой кислоты. Этим объясняется более короткий период полувыведения артикаина из плазмы крови по сравнению с другими амидными анестетиками (табл.1) 90% артикаина инактивируется гидроксилированием карбоксильной группы неспецифическими эстеразами тканей и плазмы крови и выводится преимущественно в виде неактивного метаболита - артикаиновой кислоты (64%) и в меньшей степени глюкуронида артикаиновой кислоты (13%) и в неизмененном виде (около 5-10%).
Таблица 2 Фармакокинетические параметры местных анестетиков
| Препарат | рКа | Связывание с белками (%) | Коэффициент разделения (октанольный буфер)* | Т172(мин.) | Выделение с мочой в неизмененном виде (%) |
| Артикаин | 7,8 | 1,5-10 | |||
| Бупивакаин | 8,1 | ||||
| Лидокаин | 7,8 | ||||
| Мепивакаин | 7,7 | 1-16 | |||
| Прокаин | 8,9 | 5,8 | 0,7 |
Проведенный сравнительный анализ эффективности анестетиков разных химических групп выявил, что амиды лучше диффундируют в ткани, более длительно действуют, реже вызывают аллергические реакции, более стойки при хранении и стерилизации.[13]
По химической структуре все применяемые в настоящее время местные анестетики являются слабыми основаниями. Они липофильны и плохо растворяются в воде. Особенности структуры тканей челюстно-лицевой области делают предпочтительным инъекционное обезболивание стоматологических вмешательств, поэтому местные анестетики используются в виде удобных для применения водорастворимых (гидрофильных) солей соляной кислоты. Эти растворы стабильны при рН от 4,5 до 6,0.
После инъекции водорастворимые соли местных анестетиков хорошо диффундируют в тканевой жидкости (физиологическое значение рН экстрацеллюлярной жидкости - 7,4), но для проявления анестезирующего эффекта в тканях должен произойти гидролиз местного анестетика с образованием липофильного неионизированного основания, проникающего через фосфолипидную мембрану нервных окончаний и волокон. Активность гидролиза зависит от константы диссоциации (рКа) местного анестетика, концентрации и рН его раствора, а также рН тканей, в которые вводят препарат. Транспорт липофильного анестетика-основания через нейрональную мембрану осуществляется путем простой диффузии по градиенту концентрации. Чем выше концентрация раствора местного анестетика, ближе рКа и рН его раствора к рН инъецируемых тканей, тем выше концентрация липофильного анестетика-основания на наружной стороне мембраны, активнее происходит его диффузия, препарат действует быстрее и сильнее. В нервном волокне вновь устанавливается равновесие между катионом и основанием анестетика. Активной формой анестетика на внутренней стороне мембраны является водорастворимая катионная форма.
Таким образом, для проявления обезболивающего эффекта важное значение имеет жирорастворимость и гидрофильные свойства местного анестетика. Растворимость в жирах влияет на проникновение препарата через клеточные мембраны, в том числе оболочки нервных волокон, а с рецепторами нейрональной мембраны взаимодействует катионная водорастворимая форма местного анестетика.
Современные местные анестетики (артикаин, лидокаин, мепивакаин), широко используемые в стоматологии, имеют рКа 7,6-7,9, гидролиз их солей активно идет в слабощелочной среде интактных тканей, и обезболивающий эффект развивается через 2-5 минут в зависимости от вида анестезии. Повышение рКа приводит к замедлению гидролиза, поэтому у бупивакаина (маркаина), имеющего рКа 8,1, анестезирующий эффект развивается через 7-10 минут. У прокаина (новокаина), имеющего наиболее высокое значение рКа (8,9), гидролиз даже в интактных тканях идет медленно и эффект развивается через 10-18 минут.
При наличии в месте проведения анестезии инфекции и воспаления рН тканей снижается, в результате гидролиз анестетика идет медленнее, угнетается освобождение анестетика-основания, замедляется скорость развития и уменьшается длительность анестезирующего эффекта. В меньшей степени теряет свою активность при воспалении артикаин, применяемый в более высокой концентрации, что делает его препаратом выбора в этих условиях.
Местные анестетики в растворе находятся в виде солей соляной кислоты, поэтому рН этих растворов 4,5-6,5, а при наличии в местноанестезирующем растворе нестабильного в щелочной среде эпинефрина (адреналина) рН еще больше снижается (до 3,5-5,0), что обуславливает болезненность при введении этих препаратов (табл.3).
При использовании местноанестезирующих растворов, имеющих низкое значение рН, особенно мепивакаина с вазоконстриктором (рН 3-3,5), в месте инъекции рН тканей уменьшается, в связи с чем, при их быстром повторном введении может наблюдаться снижение обезболивающего эффекта препарата, т. е. развитие тахифилаксии.
Таблица 3рН растворов местноанестезирующих препаратов
| Препарат | рН раствора без вазоконстриктора | рН раствора с вазоконстриктором |
| Новокаин | 5,0-6,5 | - |
| Лидокаин | 6,5 | 5,0-5,5 |
| Артикаин | - | 4,4-5,4 |
| Мепивакаин | 4,5 | 3,0-3,5 |
| Бупивакаин | 4,5-6,0 | 3,0-4,5 |
| Ропивакаин | 5,5-6,0 | - |
Поскольку рН местноанестезирующих растворов варьирует от 3,2 до 6,5, а рКа большинства из них составляет 7,7- 9,0, большая часть анестетика в растворе находится в ионизированной катионной форме и менее 3% присутствует в виде неионизированного свободного основания, растворимого в жирах и проникающего через фосфолипидную мембрану нервного волокна. Добавление химических веществ, которые увеличивают рН раствора местного анестетика до нормального рН тканей (7,35-7,5), за минуты до инъекции повышает количество липофильного анестетика-основания, ускоряет, увеличивает и удлиняет анестезирующий эффект, уменьшает боль при введении местного анестетика.
Пассивный транспорт анестетика-основания в клетку осуществляется по градиенту концентрации со скоростью прямо пропорциональной растворимости препарата в жирах. Чем выше липофильность местного анестетика, тем легче он проникает через фосфолипидную мембрану нервного волокна, создавая более высокую концентрацию на рецепторе, что обуславливает его активность. В то же время при высокий липофильности препарат лучше проходит гистогематические барьеры, что увеличивает его токсичность. Лидокаин превосходит по жирорастворимости прокаин (новокаин), поэтому он активнее проходит мембрану нервного волокна, действует быстрее и сильнее, в то же время он в большей степени всасывается в кровь, что увеличивает вероятность развития системного, в том числе токсического действия. Еще более высокой жирорастворимостью обладает бупивакаин, имеющий самую высокую кардио-токсичность.
Внутри клетки, где рН ниже, чем на наружной поверхности нейрональной мембраны, часть молекул местного анестетика вновь переходит в катионную форму, которая взаимодействует с белком-рецептором потенциалзависимых натриевых каналов на внутренней поверхности мембраны нервного волокна, изменяя ее физико-химические свойства и нарушая проницаемость для ионов.
Анестезирующее действие и системная токсичность препарата зависят также от способности связываться с белками-рецепторами ионного канала в мембране нервного волокна и белками плазмы крови. Чем выше показатель связывания анестетика с белками, тем выше степень его фиксации на рецепторе, что увеличивает местноанестезирующую активность и длительность действия препарата, а связывание с белками плазмы крови препятствует прохождению гистогематических барьеров и поступлению его в ткани, снижая системную токсичность. Артикаин, бупивакаин и ропивакаин наиболее активно связываются с белками (94-95%). Местные анестетики группы сложных эфиров, в отличие от анестетиков группы амидов, связываются с белками плазмы крови незначительно (5-10%).
При всасывании местных анестетиков в кровь концентрация препарата на рецепторе снижается и, следовательно, уменьшается его обезболивающая активность, в то же время возможность системного (токсического) действия увеличивается.
Местные анестетики в основном связываются с глобулинами (а1-кислым гликопротеином) плазмы крови, уровень которых при беременности, инфаркте миокарда, опухолях, в послеоперационном периоде, у новорожденных и пожилых пациентов изменяется, что может повлиять на уровень в крови не связанного с белками препарата, способного проходить через гистогематические барьеры. При расчете дозы местного анестетика следует учитывать, что при гиперкапнии, гипопротромбинемии и ацидозе снижается связывание анестетиков белками и их потенциальная системная токсичность повышается.
Таким образом, физико-химические свойства (липофильность, степень ионизации, связывание с белками) местных анестетиков влияют на скорость и степень диффузии, определяют концентрацию препарата на рецепторе, от которой зависит его местноанестезирующая активность (скорость наступления, сила и длительность эффекта), а также способность всасываться в кровь и оказывать системное действие. Высокий показатель связывания анестетика с белками плазмы крови затрудняет поступление анестетика в ткани, а высокая жирорастворимость, наоборот, облегчает. Скорость всасывания в кровь зависит от дозы и концентрации раствора анестетика, его химической структуры и физико-химических свойств, пути и скорости его введения, васкуляризации тканей в области применения, наличия или отсутствия в растворе вазоконстриктора. Выраженность большинства системных эффектов пропорциональна уровню местного анестетика в плазме крови и зависит от наличия у пациента сомати-ческой патологии (заболеваний печени, почек, сердечно-сосудистой системы). Хорошо растворимые в жирах анестетики (бупивакаин, ропивакаин) создают более высокую концентрацию в крови, чем менее липофильные лидокаин и ар- тикаин, которые меньше всасываются в кровь. Артикаин имеет более низкий коэффициент разделения по сравнению с лидокаином и при этом в большей степени связывается с белками плазмы, что обуславливает его более низкую токсичность и дает возможность использовать в более высокой концентрации (4%-ный раствор) для инъекционного обезболивания, чем другие местные анестетики. Препараты, имеющие высокую липофильность, в большей степени проходят через тканевые барьеры, в том числе плаценту, путем пассивной диффузии и поступают в систему кровообращения плода. Риск воздействия на плод ниже у анестетиков, имеющих более низкую липофильность и высокую степень связывания с белками плазмы крови, например, у артикаина.
У местных анестетиков (прокаин, бупивакаин, лидокаин и артикаин) присутствует сосудорасширяющее действие, что приводит к повышению скорости их всасывания в кровь и увеличивает токсичность. Это уменьшает уровень препарата в месте введения, а соответственно снижает активность и длительность анестезии.[5]
Уровень препарата в крови определяется не только способностью всасываться в кровь, но также скоростью метаболизма, клиренсом и периодом по- лувыведения (Т1/2), т. е временем снижения его уровня в плазме крови на 50%. После всасывания в кровь в начальную фазу распределения более высокий уровень местного анестетика наблюдается в тканях и органах, имеющих высокую перфузию (головной мозг, печень, почки, сердце, легкие, селезенка), затем происходит медленное перераспределение местных анестетиков в мышцы и жировую ткань, т. е. в ткани, которые хуже снабжаются кровью. От уровня местного анестетика в крови и органах зависит его потенциальная токсичность. Высокая васкуляризация ЦНС и сердечно-сосудистой системы способствует созданию в этих системах потенциально токсических уровней местных анестетиков, что зависит от жирорастворимости, связывания с белками плазмы крови, биотрансформации и ренальной экскреции препаратов.
Период полувыведения (Т1/2) амидных местных анестетиков (табл.2) колеблется от 22 мин. у артикаина до 163 мин. у бупивакаина. На скорость биотрансформации, клиренс и объем распределения этих препаратов оказывает влияние состояние функции печени и печеночного кровотока, что следует учитывать у пациентов со значительным нарушением функции печени и сердечно-сосудистой системы. Период полувыведения местных анестетиков зависит также от содержания вазоконстриктора и составляет для артикаина от 20 до 30 минут, а лидокаина и мепивакаина от 90 до 120 минут. У новорожденных клиренс местных анестетиков снижен, а значение Т1/2 увеличено.
Почечный клиренс зависит от связи препарата с белками плазмы и рН мочи. Местные анестетики группы сложных эфиров почти полностью гидролизуются в плазме крови и в неизменном виде в моче определяются в незначительном количестве. Процесс биотрансформации амидных анестетиков в печени более сложен и содержание неизмененного препарата в моче может быть выше (до 10% у лидокаина и 16% у бупивакаина). Эти особенности экскреции местных анестетиков следует учитывать у пациентов с нарушением функции почек.
Таким образом, фармакокинетика местных анестетиков зависит от химической структуры, физико-химических свойств, пути введения препарата, возраста пациента и может значительно меняться при нарушении функции печени, почек, под влиянием факторов, изменяющих рН мочи и почечный кровоток.
Учитывая особенности структуры тканей челюстно-лицевой области, в стоматологии в основном используются инъекционные методы местного обезболивания (инфильтрационая, проводниковая, интралигаментарная, внутрипульпарная, интрасептальная, внутрикостная анестезия).
Для инфильтрационной и проводниковой анестезии могут использоваться артикаин, лидокаин, мепивакаин, прокаин (новокаин), тримекаин, бупивакаин (маркаин), ропивакаин (наропин); для интралигаментарной, внутрипульпарной, интрасептальной, внутрикостной анестезии - артикаин, лидокаин, мепивакаин.
Для поверхностной (терминальной, аппликационной) анестезии используются местные анестетики, хорошо проникающие в ткани и воздействующие на чувствительные нервные окончания: бензокаин (анестезин), лидокаин в высокой концентрации (5-10%), тетракаин (дикаин). Но следует помнить, что через неповрежденные кожные покровы анестетики не проходят, поэтому поверхностная анестезия используется только для обезболивания слизистой оболочки рта, тканей пародонта, раневых поверхностей, обезболивания места вкола перед проведением внутриротовой инъекционной анестезии. Поверхностная анестезия считается наиболее безопасным методом обезболивания, но следует помнить, что используемые для этой цели анестетики хорошо всасываются и их нельзя наносить на большие поверхности слизистой оболочки рта из-за риска возможности всасывания в кровь и развития системного токсического действия.[11]
Заключение
Болевой синдром, обусловленный богатой смешанной иннервацией челюстно-лицевой области, является постоянным спутником большинства стоматологических заболеваний, что часто затрудняет работу врача.
Сегодня обезболивание стало неотъемлемой частью стоматологического лечения, защищающее пациента от страха, ожидания боли, психоэмоционального переживания, перенапряжения, а также позволяющее предотвратить развитие дентофобии и способствующее своевременному обращению пациента за врачебной помощью.
Эффективность и безопасность местной анестезии во многом зависит от адекватно выбранного препарата и его дозы с учетом планируемого вмешательства, соматического состояния пациента и его возраста.
 2017-12-14
2017-12-14 7089
7089
