Багатоатомні спирти містять у молекулі кілька гідроксильних груп.
Двохатомні спирти називають д і о л а м и, або гліколями. Назви двохатомних спиртів за міжнародною номенклатурою складають з назви відповідного алкану з додаванням закінчення -діол і цифр, які означають положення гідроксильної групи в ланцюгу.
Трьохатомні спирти називають тріодами, або гліцеринами. їх назви будують аналогічно до назв двохатомних спиртів, але з додаванням закінчення -тріол.
Найпростіші представники двох- і трьохатомних спиртів:
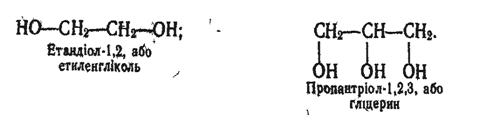
Властивості. Хімічні властивості багатоатомних спиртів багато в чому подібні до властивостей одноатомних спиртів. При цьому в реакціях може брати участь як одна, так і дві і більше гідроксильних груп. Нижче розглядаються властивості багатоатомних спиртів на прикладі етиленгліколю і гліцерину. Це безбарвні в'язкі сиропоподібні рідини, солодкуваті на смак, добре розчиняються у воді.
1. Взаємодія з лужними металами. Лужні метали витісняють водень з гідроксильних груп з утворенням гліколятів або гліцератів:
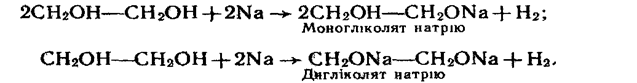
Аналогічно реагує з лужними металами гліцерин, при цьому можуть утворюватись моно-, ди- і тригліцераги.
2. Взаємодія з галогеноводнями. Багатоатомні спирти реагують з галогеноводнями (НС1, НВг, НІ) з утворенням гадогенозаміщених спиртів або галагенопохідних алканів:
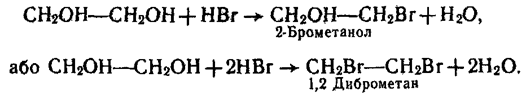
3. Взаємодія з кислотами. З кислотами багатоатомні спирти утворюють складні ефіри, наприклад:
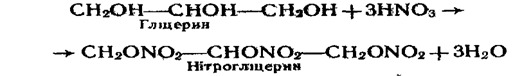
Складні ефіри гліцерину з органічними кислотами називають жирами.
4. Взаємодія з гідроксидом міді (II). Ця реакція характерна тільки для багатоатомних спиртів. Осад гідроксиду міді (II) розчиняється в етиленгліколі та гліцерині з утворенням розчину яскраво-синього кольору:
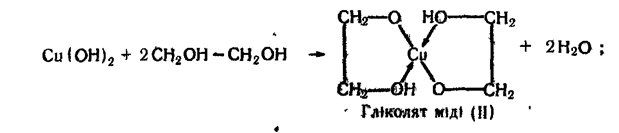
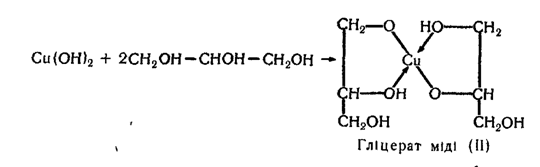
У записаних формулах гліколяту і гліцерату міді (II) стрілками показані донорно-акцепторні зв'язки (мідь — акцептор). Сполуки такого типу належать до комплексних.
Добування і застосування етиленгліколю і гліцерину. Етиленгліколь добувають у промисловості гідратацією (приєднання води) етиленоксиду:
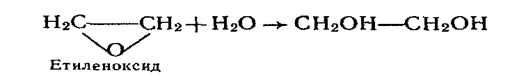
Як і одноатомні спирти, етиленгліколь можна добути гідролізом галагенопохідних алканів водним розчином лугів. Для цієї реакції необхідні 1,2-дигалогенопохідні етану:
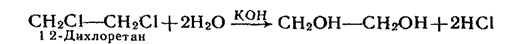
Етиленгліколь утворюється під час пропускання етилену крізь розчин перманганату калію, при цьому відбуваються окислення і гідратація етилену:
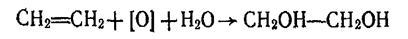
Гліцерин добувають синтетичне з пропілену за такою схемою:
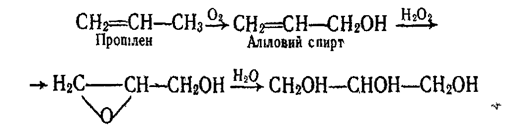
Гліцерин входить до складу природних сполук — жирів рослинного і тваринного походження — і може бути виділений з них.
Етиленгліколь і гліцерин використовуються в промисловому органічному, синтезі.
Гліцерин застосовують для виробництва мастил, як пом'якшувач шкіри і тканин, у парфумерній, фармацевтичній і харчовій промисловості.
Водні розчини етиленгліколю і гліцерину замерзають при низьких температурах, тому їх використовують як антифризи — рідини з низькою температурою замерзання, які застосовуються для охолодження двигунів внутрішнього згоряння.
Гліцерин.
Єдиний практично важливий представник трьохатомного спирту. Сіропоподібна солодка рідина, без кольору, добре розчинна у воді. Водні розчини гліцерину замерзають при низькій температурі.
Гліцерин широко розташований у природі, є основним спиртом, приймає участь у будові молекул різних груп ліпідів. У промисловості гліцерин добувають гідролізом ацилгліцеринів:
О
½½
 СН2-О-С-R
СН2-О-С-R
О СН2ОН
½½½
 СН-О-С-R1 + 3Н2О ® СН-ОН + R-СООН + R1-СООН + R2-СООН
СН-О-С-R1 + 3Н2О ® СН-ОН + R-СООН + R1-СООН + R2-СООН
О ½карбонові кислоти
½½ СН2ОН
СН2-О-С-R2 гліцерин
тригліцерин
Гліцерин широко використовується в багатьох галузях промисловості. Основна його кількість витрачається для добування похідних - гліфталевих смол, нітрогліцерину.
У харчовій промисловості гліцерин використовують для приготування лікерів та безалкогольних напоїв, у паперовій та шкіровеній - для збереження матеріалів від висихання. Він входить у склад багатьох косметичних препаратів і широко використовується як пом'ягчуюча шкіру речовина.
 2017-12-16
2017-12-16 960
960







