Оптимальною величиною загальної твердості води, яка іде на приготування пива вважається 2-4 мг×екв/дм3.
Метод визначення загальної твердості заснований на утворенні комплексної сполуки трилона Б з іонами кальцію та магнію.
Проведення досліду.
В конічну колбу вносять 100см3 досліджуємої води прибавляють 5см3 буферного розчину, 0,1г індикатору хромогенчорного та титрують трилоном Б до змінення забарвлення. Якщо на титрування пішло більш ніж 10см3 розчину трилону Б, то це говогить про те що загальний вміст іонів кальцію та магнію більше 0,5 мг×екв. В таких випадках визначення слід повторити, взявши об¢єм води та розвівши його до 100см3 бідистильованою водою.
Обробка результатів.
Загальну твердість води (Х) в мг×екв/дм3 розраховують по формулою:
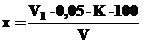 (1)
(1)
де V1- об¢єм розчину трилона Б, витраченого на титрування, см3;
К – коефіцієнт поправки до розчину трилона Б;
V - об¢єм води, взятий для визначення, см3.
ВИЗНАЧЕННЯ КАЛЬЦІЮ І МАГНІЮ.
Оптимальним відношенням іонів кальцію та магнію в воді, яка іде на приготування пива, вважають відношення 1:1, 2:1, 3:1.Метод заснований на визначенні іонів кальцію з трилоном Б в лужному середовищі в присутності індикатора мурексиду, сполуки забарвленої в оранжево-рожевий колір.
Вміст магнію розраховують за різницею між загальною твердістю та вмістом кальцію.
4.1 Проведення досліду.
До визначеного об¢єму досліджуваної води, який доводять до мітки 100 см3 бідистильованою водою, додають 5 см3 розчину гідроксиду натрію та 2-5 крапель розчину мурексиду. Розчин титрують трилоном Б до переходу забарвлення в ліловий колір. Визначення проводять в двох пробах, першу перетитровують та використовують в якості свідка.
Обробка результатів.
Масову концентрацію кальцію (хСа) в мг.екв/дм3 розраховують за формулою:
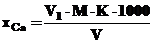 (2)
(2)
де М- молярність розчину трилона Б;
К – коефіцієнт поправки розчину трилона Б;
V1 – об¢єм розчину трилона Б, який пішов на титрування, см3;
V - об¢єм проби, см3.
Масову концентрацію магнію (хМg) в мг.екв/дм3 розраховують за формулою:
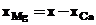 (3)
(3)
де х – загальна твердість в мг.екв/дм3;
хСа – масова концентрація кальцію, мг.екв/дм3.
5 ВИЗНАЧЕННЯ ЛУЖНОСТІ
Під лужністю розуміють властивість бікарбонатів, карбонатів, гідратів, а також інших солей слабких кислот, які вміщуються в воді пов¢язувати еквівалентну кількість сильної кислоти.
5.1 Проведення досліду:
100 см3 проби води наливають в конічну колбу та прибавляють 0,15 см3 змішаного індикатора І або 0,25 см3 змішаного індикатора ІІ і титрують розчином HCl з с=0,1 моль/дм3 до моменту, коли зелене забарвлення змішаного індикатору перейде в брудно-сірий або до порожевіння при використанні індикатора ІІ.
5.2 Обробка результатів
Лужність (х) в мг.екв/дм3 розраховують за формулою:
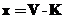 (4)
(4)
де V- об¢єм розчину HCl з с=0,1 моль/дм3, який пішов на титрування, см3;
К – коефіцієнт поправки до розчину соляної кислоти.
 2018-01-08
2018-01-08 291
291








