Эквивалентом вещества называется такое количество его, которое взаимодействует с одним моль атомов водорода или вообще с одним эквивалентом любого другого вещества. Обозначается эквивалент Э (Х), выражается в молях. (определение в методичке)
Или
Эквивалент – это реальная или условная частица, которая в кислотно-основных реакциях присоединяет (или отдает) один ион Н+ или ОН–, в окислительно-восстановительных реакциях принимает (или отдает) один электрон, реагирует с одним атомом водорода или с одним эквивалентом другого вещества.
Например, рассмотрим следующую реакцию:
H3PO4 + 2KOH ® K2HPO4 + 2H2O.
В ходе этой реакции только два атома водорода замещаются на атомы калия, иначе, в реакцию вступают два иона Н+ (кислота проявляет основность 2). Тогда по определению эквивалентом H3PO4 будет являться условная частица 1/2H3PO4, т.к. если одна молекула H3PO4 предоставляет два иона Н+, то один ион Н+ дает половина молекулы H3PO4.
С другой стороны, на реакцию с одной молекулой ортофосфорной кислотой щелочь отдает два иона ОН–, следовательно, один ион ОН– потребуется на взаимодействие с 1/2 молекулы кислоты. Эквивалентом кислоты является условная частица 1/2Н3РО4, а эквивалентом щелочи частица КОН.
Эквивалент одного и того же вещества может меняться в зависимости от того, в какую реакцию оно вступает.Эквивалент элемента также может быть различным в зависимости от вида соединения, в состав которого он входит.Эквивалентом может являться как сама молекула или какая-либо другая формульная единица вещества, так и ее часть.
Закон эквивалентов предложен в 1814г. И.Рихтером: «Вещества взаимодействуют и получаются в массовых количествах прямо пропорционально их эквивалентам». Математическое выражение этого закона:
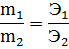
m1, m2- массы веществ, Э1, Э2- эквиваленты веществ. Или m1Э2=m2Э1
Следствие закона: Объемы реагирующих растворов обратно пропорциональны их нормальным и молярным концентрациям:
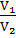 =
= 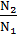 или
или 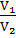 =
= 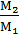
 2018-01-21
2018-01-21 2507
2507








