Электролиты – вещества, которые при растворении подвергаются диссоциации на ионы. В результате раствор приобретает способность проводить электрический ток, т.к. в нем появляются подвижные носители электрического заряда. Электролиты можно разделить на две большие группы: сильные и слабые. Сильные электролиты диссоциируют практически полностью. К сильным электролитам относятся, например, H2SO4, HCl, HNO3, H3PO4, HClO3, HClO4, KOH, а также хорошо растворимые соли: NaCl, KBr, NH4NO3и др. Для слабых электролитов устанавливается равновесие между недиссоциированными молекулами и ионами. К слабым электролитам относятся плохо растворимые соли (см. таблицу растворимости), вода и большинство органических кислот (например, уксусная CH3COOH, муравьинаяHCOOH), а также неорганические соединения: H2CO3, H2S, HCN, H2SiO3, H2SO3, HNO2, HClO, HCNO, NH4OH и др. Константа равновесия для процесса диссоциации называется константой диссоциации (K). В общем случае для электролита,диссоциирующего на два иона:АВ  А+ + В–
А+ + В–
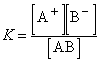
Для приведенного выше процесса диссоциации уксусной кислоты: 
Если обозначить концентрацию электролита, распадающегося на два иона, через C, то
[A+] = [B–] = a C; [AB] = C(1–a);

Это уравнение соответствует закону разбавления Оствальда. Если электролит слабый, и диссоциация очень мала (a<<1), то закон разбавленияОствальда упрощается:
K =a2 C; 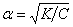 .
.
Таким образом, степень диссоциации возрастает с разбавлением раствора.
Билет 36
Ио́нное произведе́ние воды́ — произведение концентраций ионов водорода Н+ и ионов гидроксида OH− в воде или в водных растворах, константа автопротолиза воды.
Вывод значения ионного произведения воды
Вода, хотя и является слабым электролитом, в небольшой степени диссоциирует:
H2O + H2O ↔ H3O+ + OH−
или
H2O ↔ H+ + OH−
Равновесие этой реакции сильно смещено влево. Константу диссоциации воды можно вычислить по формуле:  [H+] — концентрация ионов гидроксония (протонов); [OH−] — концентрация гидроксид-ионов; [H2O] — концентрация воды (в молекулярной форме) в воде;
[H+] — концентрация ионов гидроксония (протонов); [OH−] — концентрация гидроксид-ионов; [H2O] — концентрация воды (в молекулярной форме) в воде;
Концентрация воды в воде, учитывая её малую степень диссоциации, величина практически постоянная и составляет (1000 г/л)/(18 г/моль) = 55,56 моль/л.
При 25 °C константа диссоциации воды равна 1,8×10−16моль/л. Уравнение (1) можно переписать как:
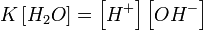 , ,
| (2) |
Обозначим произведение K·[H2O] = Kв = 1,8×10−16 моль/л·55,56 моль/л = 10−14моль²/л² = [H+]·[OH−] (при 25 °C).
Константа Kв, равная произведению концентраций протонов и гидроксид-ионов, называется ионным произведением воды. Она является постоянной не только для чистой воды, но также и для разбавленных водных растворов веществ. C повышением температуры диссоциация воды увеличивается, следовательно, растёт и Kв, при понижении температуры — наоборот.
Билет 37
Водоро́дный показа́тель, pH — мера активности (в очень разбавленных растворах она эквивалентнаконцентрации) ионов водорода в растворе, и количественно выражающая его кислотность, вычисляется как отрицательный (взятый с обратным знаком) десятичный логарифм активностиводородных ионов, выраженной в молях на литр: 
Если в воде пониженное содержание свободных ионов водорода [H+] (рН > 7) по сравнению с ионами гидроксида [ОН-], то вода будет иметь щелочную реакцию, а при повышенном содержании ионов Н+ (рН < 7) - кислую. В идеально чистой дистиллированной воде эти ионы будут уравновешивать друг друга и в нейтральной воде рН=7. При растворении в воде различных химических веществ этот баланс может быть нарушен, что приводит к изменению значения рН.
Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. При добавлении к воде кислоты концентрация ионов водорода увеличивается, а концентрация гидроксид-ионов соответственно уменьшается, при добавлении основания — наоборот, повышается содержание гидроксид-ионов, а концентрация ионов водорода падает. Когда [H+] > [OH-] говорят, что раствор является кислым, а при [OH-] > [H+] — щелочным.
Билет 38
Гидро́лиз (от др.-греч. ὕδωρ — вода и λύσις — разложение) — один из видов химических реакций сольволиза, где при взаимодействии веществ с водой происходит разложение исходного вещества с образованием новых соединений. Механизм гидролиза соединений различных
]Гидролиз солей
Гидролиз солей — разновидность реакций гидролиза, обусловленного протеканием реакций ионного обмена в растворах (преимущественно, водных) растворимых солей-электролитов. Движущей силой процесса является взаимодействие ионов с водой, приводящее к образованию слабого электролита в ионном или (реже) молекулярном виде («связывание ионов»).
Различают обратимый и необратимый гидролиз солей[1]:
§ 1. Гидролиз соли слабой кислоты и сильного основания (гидролиз по аниону):
CO32− + H2O = HCO3− + OH−
Na2CO3 + Н2О = NaHCO3 + NaOH
(раствор имеет слабощелочную среду, реакция протекает обратимо, гидролиз по второй ступени протекает в ничтожной степени)
§ 2. Гидролиз соли сильной кислоты и слабого основания (гидролиз по катиону):
Cu2+ + Н2О = CuOH+ + Н+
CuCl2 + Н2О = CuOHCl + HCl
(раствор имеет слабокислую среду, реакция протекает обратимо, гидролиз по второй ступени протекает в ничтожной степени)
§ 3. Гидролиз соли слабой кислоты и слабого основания:
2Al3+ + 3S2− + 6Н2О = 2Al(OH)3(осадок) + ЗН2S(газ)
Al2S3 + 6H2O = 2Al(OH)3 + 3H2S
(равновесие смещено в сторону продуктов, гидролиз протекает практически полностью, так как оба продукта реакции уходят из зоны реакции в виде осадка или газа).
Соль сильной кислоты и сильного основания не подвергается гидролизу, и раствор нейтрален. См. также Электролитическая диссоциация.
Степень гидролиза
Под степенью гидролиза подразумевается отношение части соли, подвергающейся гидролизу, к общей концентрации её ионов в растворе. Обозначается α (или hгидр);
α = (c гидр/ c общ)·100 %
где c гидр — число молей гидролизованной соли, c общ — общее число молей растворённой соли.
Степень гидролиза соли тем выше, чем слабее кислота или основание, её образующие.
Является количественной характеристикой гидролиза.
Константа гидролиза — константа равновесия гидролитической реакции.
Выведем уравнение константы гидролиза соли, образованной слабой кислотой и сильным основанием:
Билет 39
Окислительно-восстановительные реакции сопровождаются переходом электронов от одних участвующих в реакции частиц (атомов, ионов, молекул) к другим. Процесс потери электронов частицей называется ее окислением, а сама частица, теряющая электроны, - восстановителем. Процесс присоединения электронов частицей называется ее восстановлением, а сама частица, принимающая электроны, - окислителем. Таким образом, в ходе окислительно-восстановительной реакции окислитель восстанавливается, а восстановитель окисляется.
В химических реакциях окисление одного вещества всегда сопровождается восстановлением другого, и наоборот. Количество электронов, принимаемых окислителем, равно количеству электронов, теряемых восстановителем, поэтому химическая система в целом остается электронейтральной. Это означает, что если мы нашли в уравнении реакции вещество, которое в ходе реакции, например, восстанавливается, то следует искать в том же уравнении вещество, которое в ходе реакции окисляется, и наоборот.
Степень окисления – формальная величина, которую вычисляют на основе формулы соединения исходя из условного допущения, что связь между атомами в данном соединении ионная. Несмотря на формальный характер понятия «степень окисления», использование его оказывается весьма продуктивным при рассмотрении окислительно-восстановительных реакций, в частности при нахождении коэффициентов уравнений окислительно-восстановительных реакций.
Так как электрон заряжен отрицательно, при окислении степень окисления атома изменяется в положительную сторону, а при восстановлении – в отрицательную.
 2018-01-21
2018-01-21 703
703








