Вопрос 1 Основн законы
Закон сохранения массы и энергии (Ломоносов М.В., 1748 г.):
а) "масса веществ, вступающих в реакцию, равна массе веществ, образующихся в результате реакции".
б) "в изолированной системе сумма масс и энергий постоянна".
Закон постоянства состава (Пруст Ж., 1801 г.):
"каждое химически чистое соединение всегда имеет один и тот же количественный состав независимо от способа его получения".
Закон эквивалентов (Рихтер И., 1793 г.):
а) "все вещества реагируют в эквивалентных отношениях"
б) "моль эквивалентов одного вещества реагирует с одним моль эквивалентов другого вещества".
Эквивалент - реальная или условная частица вещества, которая может замещать, присоединять, высвобождать или быть каким-либо другим способом эквивалентна одному протону Н+ в кислотно-основных или ионообменных реакциях, или одному электрону в окислительно-восстановительных реакциях.
Эквивалентные массы для химических соединений определяются по следующим формулам:
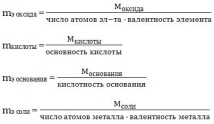
Закон Авогадро (1811 г.):
"в равных объемах любых газов, взятых при одной и той же температуре и одинаковом давлении, содержится одинаковое число молекул". Т.е. 1 моль любого газа занимает один и тот же объем (молярный объем): vm = 22,4 л/моль.
Относительная атомная масса элемента Ar - отношение массы атома элемента к 1/12 части массы атома 12С.
Относительная молекулярная масса вещества Mr - отношение массы молекулы вещества к 1/12 части массы атома 12С.
Mr = ∑Ar
Mr = М, где М - молярная масса вещества.
Моль - количество вещества, содержащее столько молекул, атомов, ионов, электронов или других структурных единиц, сколько содержится атомов в 12 г. изотопа12С.
Число структурных единиц в 1 моль вещества NА = 6,02 · 1023 моль-1 - число Авогадро.
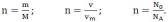
Из закона Авогадро следует, что
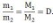
D - относительная плотность одного газа по другому: D = ρ1/ρ2.
Закон кратных отношений (Дальтон, 1803 г.):
"если два элемента образуют друг с другом несколько химических соединений, то массы одного из элементов, приходящиеся в этих соединениях на одну и ту же массу другого, относятся между собой как небольшие целые числа".
 2018-01-21
2018-01-21 348
348







