Квантовые числа. Для характеристики поведения электрона в атоме введены квантовые числа: главное, орбитальное, магнитное и спиновое. Главное квантовое число п определяет энергию и размеры электронных орбиталей. Главное квантовое число принимает значения I, 2, 3, 4, 5,... и характеризует оболочку или энергетический уровень. Чем больше n, тем выше энергия. Оболочки (уровни) имеют буквенные обозначения: К (п = 1), L (п = 2), М(п = 3), N(n = 4), Q (п = = 5), переходы электронов с одной оболочки (уровня) на другую сопровождаются выделением квантов энергии, которые могут проявиться в виде линий спектров Орбитальное квантовое число / определяет форму атомной орбитали. Электронные оболочки расщеплены на подоболочки, поэтому орбитальное квантовое число также характеризует энергетические подуровни в электронной оболочке атома. Орбитальные квантовые числа принимают целочисленные значения от 0 до (п — 1). Подоболочки также обозначаются буквами: Подоболочка (подуровень) s p d f Орбитальное квантовое число,l 0 1 2 3Электроны с орбитальным квантовым числом 0, называются s-электронами. Орбитали и соответственно электронные облака имеют сферическую форму. Электроны с орбитальным квантовым числом 1 называются р-электронами. Обитали и соответственно электронные облака имеют форму, напоминающую гантель. Электроны с орбитальным квантовым числом 2 называют d-электронами. Орбитали имеют более сложную форму, чем р-орбитали Наконец, электроны с орбитальным квантовым числом 3 получили название f-электронов. Форма их орбиталей еще сложнее, чем форма d-орбиталей. В одной и той же оболочке (уровне) энергия подоболочек (подуровней) возрастает в ряду: В первой оболочке (п = 1) может быть одна (s-), во второй (n = 2) — две (s-, р-), в третьей (п = 3) — три (s-, p-, d-),в четвертой (п= 4) — четыре (s-, p-, d-, f-)-подоболочки. Магнитное квантовое число m характеризует ориентацию, обитали в пространстве. В отсутствие внешнего
магнитного поля все обитали одного подуровня (подоболочки) имеют одинаковое значение энергии. Под воздействием внешнего магнитного поля происходит расщепление энергии подоболочек. Магнитное квантовое число принимает целочисленные значения от -l до +l, включая ноль. Например, для l= 3, магнитные квантовые числа имеют значения -3, -2, -1, 0, +1, +2, +3, т. е. в данной подоболочки (f-подоболочки) существует семь орбиталей. Соответственно в подоболочке s (l = 0) имеется одна орбиталь (т, -= 0), в подоболочке p (l = 1) — три обитали (т, = -1,0, +1), в подоболочке d(l = 2) пять орбиталей (m, = -2, -1, 0, +1, +2)
Вопрос 5 Принцип Паули,Гунда
Принцип Паули, который часто называют еще принципом запрета, ограничивает число электронов, которые могут находиться на одной орбитали. Согласно принципу Паули, на любой орбитали может находиться не более двух электронов и то лишь в том случае, если они имеют противоположные спины (неодинаковые спиновые числа). Поэтому в атоме не должно быть двух электронов с одинаковыми четырьмя квантовыми числами (n, l, ml, ms).
Атом лития имеет три электрона. Орбиталь с самой низкой энергией - 1 s -орбиталь - может быть заселена лишь двумя электронами, причем у этих электронов должны быть разные спины. Если обозначать спин +1/2 стрелкой, направленной вверх, а спин −1/2 - стрелкой, направленной вниз, то два электрона с противоположными (антипараллельными) спинами на одной орбитали можно схематически представить так:
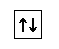
Третий электрон в атоме лития должен занимать орбиталь, следующую по энергии за самой низкой орбиталью, то есть 2 s -орбиталь.
Правило Гунда
Правило Гунда (Хунда) определяет порядок заселения электронами орбиталей, имеющих одинаковую энергию. Оно было выведено немецким физиком-теоретиком Ф. Гундом (Хундом) в 1927 г. на основе анализа атомных спектров.
Согласно правилу Гунда, заселение орбиталей, относящихся к одному и тому же энергетическому подуровню, начинается одиночными электронами с параллельными (одинаковыми по знаку) спинами, и лишь после того, как одиночные электроны займут все орбитали, может происходить окончательное заселение орбиталей парами электронов с противоположными спинами. В результате суммарный спин (и сумма спиновых квантовых чисел) всех электронов в атоме будет максимальным.
Например, атом азота имеет три электрона, находящиеся на 2 р -подуровне. Согласно правилу Гунда, они должны располагаться поодиночке на каждой из трех 2 р -орбиталей. При этом все три электрона должны иметь параллельные спины:
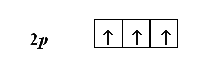
Принцип минимума энергии определяет порядок заселения атомных орбиталей, имеющих различные энергии. Согласно принципу минимума энергии, электроны занимают в первую очередь орбитали, имеющие наименьшую энергию. Энергия подуровней растет в ряду:
1 s < 2 s < 2 p < 3 s < 3 p < 4 s < 3 d < 4 p < 5 s < 4 d < 5 p < 6 s < 4 f  5 d < 6 p < 7 s < 5 f
5 d < 6 p < 7 s < 5 f  6 d...
6 d...
Атом водорода имеет один электрон, который может находиться на любой орбитали. Однако, в основном состоянии он должен занимать 1 s -орбиталь, имеющую самую низкую энергию.
В атоме калия последний девятнадцатый электрон может заселить либо 3 d -, либо 4 s -орбиталь. В соответствии с принципом минимума энергии, электрон занимает 4 s -орбиталь, что подтверждается экспериментом.
Следует обратить внимание на неопределенность записи 4 f 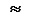 5 d и 5 f
5 d и 5 f 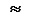 6 d. Оказалось, что у одних элементов более низкую энергию имеет 4 f -подуровень, а у других - 5 d -подуровень. То же самое наблюдается для 5 f - и 6 d -подуровней.
6 d. Оказалось, что у одних элементов более низкую энергию имеет 4 f -подуровень, а у других - 5 d -подуровень. То же самое наблюдается для 5 f - и 6 d -подуровней.
 2018-01-21
2018-01-21 552
552








