Электродный потенциал каждого электрода зависит от природы металла, концентрации его ионов в растворе и температуры.
Для условий отличных от стандартных эдектродный потенциал вычисляется по формуле Нернста:
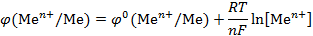
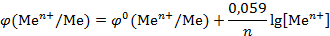
φ – равновесный электродный потенциал, В; φ° - стандартный электродный потенциал, В; R – универсальная газовая постоянная (R=8,31 Дж/мольК); T – температура, К; n – число отданных(принятых) электронов; F – число Фарадея (F=96500 Кл); [Меn+] – концентрация ионов металлов в растворе, моль/л.
Рассчитанный по уравнению Нернста равновесный потенциал зависит прежде всего от соотношения концентраций окисленной и восстановленной форм рассматриваемой полуреакции: увеличение концентрации окисленной формы, также как уменьшение концентрации восстановленной формы, приводит к возрастанию потенциала. Однако эти изменения потенциала сравнительно невелики.
Во многих окислительно-восстановительных реакциях участвуют ионы водорода (гидроксония). Изменение концентрации ионов водорода в процессе химического взаимодействия вносит существенный вклад в изменение потенциала окислительно-восстановительной системы.
В тех случаях, когда в окислительной или восстановительной полуреакции ионы водорода не принимают непосредственного участия, они могут влиять на состояние ионов окисленной и восстановленной форм в растворе, тем самым изменяя потенциал.
На значение потенциала существенное влияние оказывают любые побочные химические процессы, в которых участвуют окисленная и восстановленная формы. Часто такими процессами являются реакции комплексообразования, при которых возможно существование в растворе ряда комплексных соединений.
Как следует из уравнения Нернста, потенциал системы зависит от температуры. Наиболее существенно влияние температуры на потенциал окислительно-восстановительных систем, включающих гетерогенную фазу. Кроме того, значительное влияние температура оказывает на скорость окислительно-восстановительных реакций.
 2018-01-21
2018-01-21 2496
2496








