Гидролиз солей -это реакция обменного взаимодействия соли с водой, в результате которой образуется слабая кислота или слабое основание, кислая или основная соль.
А) соль, образованная слабой кислотой и сильным основанием.
Na2CO3 + H2O = NaHCO3+NaOH
Слабая кислота сильное основание
2Na++CO32-+HOH=Na++HCO3-+Na++OH-
CO32-+HOH=HCO3-+OH-
Гидролиз протекает по аниону, так как образуется избыток OH- ионов и раствора Phбудет больше 7.
Кг= 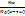
Б) соль, образованная слабым основанием и сильной кислотой.
Гидролиз протекает по катиону, так как образуется избыток H+ ионов и pH раствора будет меньше 7.
CuCl2  Cu2+ + 2Cl-
Cu2+ + 2Cl-
(Cu(OH)2) (HCl)
CuCl2+HOH  CuOHCl + HCl (дописать полное и сокращенное ионное ур-ия);
CuOHCl + HCl (дописать полное и сокращенное ионное ур-ия);
2 ст. не протекает; Кд= 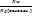
В) соль, образованная слабым основанием и слабой кислотой
В данном случае образуется слабая кислота и слабое основание, гидролиз протекает как по аниону, так и по катиону, pH>7
CH3COONH4  CH3COO- + NH4+
CH3COO- + NH4+
(CH3COOH) (NH4OH)
CH3COONH4 + HOH  NH4OH; (допис. Полнуюионнуюрек-ию)
NH4OH; (допис. Полнуюионнуюрек-ию)
Кд= 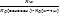
Г) соль, образованная сильной кислотой и сильным основанием.
Гидролизу не подвергается, так как в данном случае слабый электролит не образуется, pH=7
 2018-01-21
2018-01-21 625
625








