1. Сопряжение. Ароматичность. Электронные эффекты заместителей
25. Объясните, в каком соединении – хлорбензоле или бензилхлориде (фенилхлорметане) – галоген является частью сопряженной системы.
Назовите вид сопряжения.
Изобразите графически дополнительное перекрывание электронных орбиталей, приводящее к образованию сопряженной системы.
Решение
. 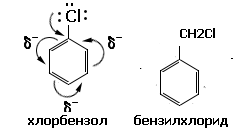
Галоген является частью сопряженной системы в хлорбензоле, поскольку в бензилхлориде его отделяет от бензольного кольца метиленовый мостик СН2. Вид сопряжения – р-π. В сопряжении участвуют 3р- электроны хлора и π-система бензольного кольца.
26. Укажите вид и знак электронных эффектов в этиламине (этанамине) и п-аминобензойной (4-аминобензойной) кислоте.
Обозначьте эффекты графически.
Объясните, почему только в одном случае аминогруппа проявляет мезомерный эффект.
Ответ
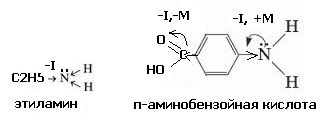
В случае этиламина наблюдается смещение электронной плотности по сигма связи С-N от радикала к аминогруппе, поскольку азот – более электроотрицателен, чем углерод. Вид и знак эффекта – I (отрицательный индукционный эффект).
У п-аминобензойной кислоты имеется лве функциональные группы (аминогруппа и карбоксильная группа), проявляющие разные виды электронных эффектов:
Для аминогруппы характерно сочетание отрицательного индукционного и положительного дмезомерного эффектов (-I,+M); для карбоксильной группы - отрицательного индукционного и отрицательного мезомерного эффектов (-I,-M).
Аминогруппа проявляет мезомерный эффект (р-π сопряжение 2рэлектронов азота с π –электронной плотностью бензольного кольца) только в п-аминобензойной кислоте, поскольку в этиламине нет π-связей.
2. Кислотность и основность органических соединений
27. Расположите в порядке уменьшения кислотности этанол, этиленгликоль (этандиол-1,2), глицерин (пропантриол-1, 2, 3).
Объясните, исходя из стабильности соответствующих анионов.
Решение
1. Уменьшение кислотности происходит в ряду:
глицерин, этиленгликоль, этанол.
2. Данная закономерность объясняется понижением стабильности соответствующих анионов. Наиболее стабилен анион (С3Н5О3)3-. Несколько меньше стабильность аниона(С2Н4О2)2-. Наименее стабилен этилат-ион С2Н50-.
3. Причиной понижения стабильности является увеличение полярности связи О-Н в ряду глицерин, этиленгликоль, этанол. Это, в свою очередь, обусловлено увеличением электронной плотности на кислороде за счет ее смещения от углеводородного радикала.
28. Расположите в порядке уменьшения основности анилин, этанамин (этиламин), 3-аминофенол.
Объясните, исходя из прочности образуемой NH-связи.
1. Уменьшение основности происходит в ряду:
этанамин (этиламин), 3-аминофенол, анилин.
2.Прочность образуемой NH-связи определяется электронной плотностью на атоме азота. Чем больше эта плотность, тем более выражены основные свойства. В этиламине этильный радикал является донором электронной плотности для азота, поэтому этиламин обладает наиболее выраженными основными свойствами. Гидроксогруппа в 3-аминофеноле является электронодонорным заместителем и, таким образом, уменьшает акцепторное влияние бензольного кольца на аминогруппу. Поэтому электронная плотность на атоме азота в 3-аминофеноле выше, чем в анилине, и основные свойства у этого соединения выражены сильнее. В анилине неподелённая электронная пара атома N аминогруппы вступает в сопряжение с 6π-электронной системой ароматического ядра. Электронная плотность на атоме N понижается, поэтому основные свойства у анилина выражены слабее, чем у предельных аминов и 3-аминофенола.
3. Реакции электрофильного характера
29. Напишите схему реакции гидратации пропена (пропилена).
Опишите её механизм.
Назовите продукт реакции по ЗН ИЮПАК.
Объясните отличие этой реакции от гидратации акриловой (пропеновой) кислоты, опираясь на современную трактовку правила Марковникова.
Ответ
1. Схема реакции гидратации пропена:
CH3CH=CH2 + H2O ® CH3CH(OH)CH3
2. Механизм реакции.
Реакция протекает в три стадии. На первой стадии, при взаимодействии с катализатором кислотного характера (Н3РО4) образуется s -комплекс (устойчивый карбокатион). На второй стадии к нему присоединяется молекула воды, на третьей происходит отщепление водородного протона.
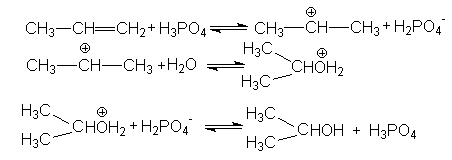
3. В результате реакции получается пропанол-2.
4. Отличие этой реакции от гидратации акриловой (пропеновой) кислоты заключается в том, что атом водорода присоединяется к менее гидрированному атому углерода в составе двойной связи:
СН2=СН-СООН+Н2О = СН2ОН-СН2-СООН
Причиной этого является распределение электронной плотности в молекуле акриловой кислоты:

Вследствие сопряжения электронных плотностей π-связей карбоксильной группы и двойной связи и смещения общей электронной плотности в сторону более электроотрицательного атома кислорода на менее гидрированном атоме С возникает частичный отрицательный заряд, на более гидрированном – частичный положительный заряд. В соответствии с современной трактовкой правила Марковникова присоединение электрофильной частицы Н+ происходит в соответствии с распределением электронной плотности, к частице с повышенной электронной плотностью.
30. Напишите схему реакции бромирования анилина.
Опишите её механизм.
Назовите продукт бромирования по ЗН ИЮПАК.
Укажите ориентирующее действие аминогруппы.
Объясните, что легче бромируется бензол или анилин.
Решение
1. Схема реакции бромирования анилина
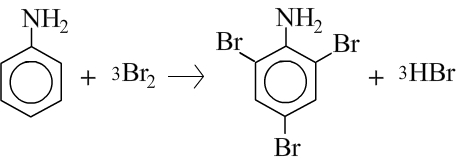
2. Механизм реакции - электрофильное замещение в ароматическом ядре. Специфической особенностью является избыточная электронная плотность в о- и п-положениях, обусловленная +М-эффектом аминогруппы. Реакция проходит в две стадии. На первой стадии (электрофильное присоединение) в о- и п-положениях образутся нестойкий δ-комплекс, лишенный ароматической структуры, с четырьмя π –электронами, делокализованными в сфере воздействия ядер пяти углеродных атомов. Шестой углеродный атом при этом переходит из состояния sp2-гибридизации в состояние sp3, приобретая таким образом тетраэдрическую симметрию. Оба заместителя Br и Н лежат в плоскости, перпендикулярной к плоскости кольца. На второй стадии лабильный δ-комплекс превращается в стабильный 2,4,6 триброманилин с потерей 3 протонов
3. Ориентирующее действие аминогруппы происходит в положения 2,4,6:
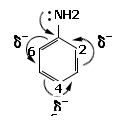
4. Бромирование анилина происходит легче, чем бромирование бензола, вследствие сопряжения неподеленной электронной пары азота с электронами ароматического ядра. Это, в свою очередь, приводит к увеличению электронной плотности в бензольном кольце, что способствует более быстрому протеканию реакции электрофильного замещения.
31. Напишите схему реакции бромирования бензойной кислоты (катализатор FеBr3).
Опишите её механизм.
Назовите продукт бромирования по ЗН ИЮПАК.
Укажите ориентирующее действие заместителя.
Объясните, что легче бромируется – бензол или бензойная кислота.
Ответ
1. Схема реакции бромирования бензойной кислоты (катализатор FеBr3):
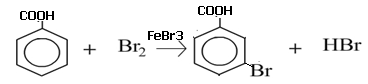
2.Механизм реакции - электрофильное замещение в ароматическом ядре. Специфической особенностью является повышенная по сравнению с другими атомами электронная плотность в м-положении, обусловленная -М-эффектом карбоксильной группы. Реакция проходит в две стадии. На первой стадии (электрофильное присоединение) в м-положении образуется нестойкий δ-комплекс, лишенный ароматической структуры, с четырьмя π –электронами, делокализованными в сфере воздействия ядер пяти углеродных атомов. Шестой углеродный атом при этом переходит из состояния sp2-гибридизации в состояние sp3, приобретая таким образом тетраэдрическую симметрию. Оба заместителя Br и Н лежат в плоскости, перпендикулярной к плоскости кольца. На второй стадии лабильный δ-комплекс превращается в стабильную 3-бромбензойную кислоту с потерей 1 протона
3.Название продукта бромирования по ЗН ИЮПАК -3-бромбензойная кислота
4. Ориентирующее действие заместителя обусловлено отрицательным мезомерным эффектом карбоксильной группы, усиливающим электронную плотность в м-положении(3 и 5- положение):
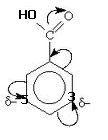
5. Легче бромируется бензол, так как вследствие отрицательного мезомерного эффекта карбоксильной группы происходит уменьшение электронной плотности на бензольном кольце.
32. Напишите схемы реакций алкилирования бензола третичным изобутанолом и пропеном в кислой среде.
Опишите механизм этих реакций.
Назовите продукты алкилирования по ЗН ИЮПАК.
Ответ
1. Схемы реакций алкилирования бензола пропеном (реакция (а) и третичным изобутанолом (реакция (b) в кислой среде:
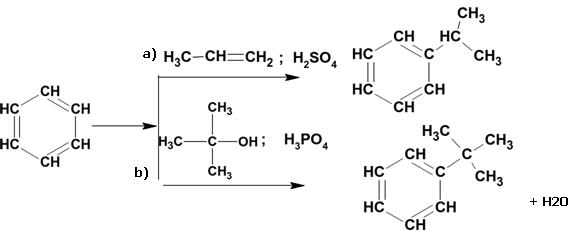
2.М еханизм этих реакций –электрофильное замещение, катализируемое минеральными кислотами. В качестве электрофильной частицы выступает карбкатион, который образуется либо при присоединении протона к олефину, либо при отщеплении воды от молекулы спирта под действием протона.
3. В обеих рассматриваемых реакциях (а и b) образуется один продукт алкилирования – изопропилбензол (кумол). В реакции b) также выделяется вода.
4. Реакции нуклеофильного характера
33. Напишите схему реакции взаимодействия 1-бромпропана с этилатом натрия.
Опишите ее механизм.
Укажите нуклеофил, субстрат, уходящую группу.
Ответ
1. Схема реакции взаимодействия 1-бромпропана с этилатом натрия:

2. Механизм реакции: замещение нуклеофильное, бимолекулярное, SN2
Реакция происходит в одну стадию. При этом атака нуклеофила и отщепление уходящей группы происходит одновременно:
C3H7Br + C2H5O- → [C2H5O-⋯ C3H7⋯ Br]− → C2H5-O-C3H7+ Br –
3. Нуклеофил - этилат-анион C2H5O-,
субстрат - 1-бромпропан, СН3СН2СН2Br,
уходящая группа - Br –
 2018-01-21
2018-01-21 10809
10809







