

График зависимости концентрации реагента A для первого порядка реакции
Кинетическое уравнение реакции первого порядка:

Реакция второго порядка


График зависимости концентрации реагента A для второго порядка реакции
Для реакций второго порядка кинетическое уравнение имеет следующий вид:
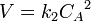
или
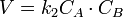
Реакция нулевого порядка


График зависимости концентрации реагента A в реакции A → B от времени для нулевого порядка реакции
Кинетическое уравнение имеет следующий вид:
V 0 = k 0
Скорость реакции нулевого порядка постоянна во времени и не зависит от концентраций реагирующих веществ. Нулевой порядок характерен, например, для гетерогенных реакций в том случае, если скорость диффузии реагентов к поверхности раздела фаз меньше скорости их химического превращения.
Вопрос
1 Большинство практически важных реакций ускоряются при нагревании.
Более точно и более универсально зависимость константы скорости реакции от температуры выражена уравнением Аррениуса [  ] (1889):
] (1889):

Множитель A связан с частотой столкновений частиц и их ориентацией при столкновениях; Ea – энергия активации данной химической реакции.
Для определения энергии активации данной реакции достаточно измерить ее скорость при двух температурах.
2 Возрастание скорости реакции с ростом температуры принято характеризовать температурным коэффициентом скорости реакции, числом, показывающим, во сколько раз возрастает скорость данной реакции при повышении температуры системы на 10°С. Температурный коэффициент различных реакций различен. При обычных температурах его значение для большинства реакций находится в пределах от 2... 4.
Температурный коэффициент определяют в соответствии с так называемым «правилом Вант-Гоффа», которое математически выражается уравнением
v 2/ v 1 = g (T 2 – T 1)/10,
где v 1 и v 2 – скорости реакции при температурах Т 1 и Т 2; g - температурный коэффициент реакции.
Так, например, если g = 2, то при Т 2 – Т 1 = 50°С v 2/ v 1 = 25 = 32, т.е. реакция ускорилась в 32 раза, причем это ускорение никак не зависит от абсолютных величин Т 1 и Т 2, а только от их разности.
Коэффициент температурного ускорения Q10, для большинства химических реакций абиотического характера равный 2, в реакциях живых систем колеблется в довольно широких пределах даже для одних и тех же процессов, протекающих в разных диапазонах температур.
3 В химической модели, известной как Теория активных соударений (ТАС), есть три условия, необходимых для того, чтобы произошла реакция:
- Молекулы должны столкнуться. Это важное условие, однако его не достаточно, так как при столкновении не обязательно произойдёт реакция.
- Молекулы должны обладать необходимой энергией (энергией активации). В процессе химической реакции взаимодействующие молекулы должны пройти через промежуточное состояние, которое может обладать большей энергией. То есть молекулы должны преодолеть энергетический барьер; если этого не произойдёт, реакция не начнётся.
- Молекулы должны быть правильно ориентированы относительно друг друга.
4 Уравне́ние Арре́ниуса устанавливает зависимость константы скорости химической реакции  от температуры
от температуры  .
.
Согласно простой модели столкновений химическая реакция между двумя исходными веществами может происходить только в результате столкновения молекул этих веществ. Но не каждое столкновение ведёт к химической реакции. Необходимо преодолеть определённый энергетический барьер, чтобы молекулы начали друг с другом реагировать. То есть молекулы должны обладать некой минимальной энергией (энергия активации  ), чтобы этот барьер преодолеть. Из распределения Больцмана для кинетической энергии молекул известно, что число молекул, обладающих энергией
), чтобы этот барьер преодолеть. Из распределения Больцмана для кинетической энергии молекул известно, что число молекул, обладающих энергией  , пропорционально
, пропорционально  . В результате скорость химической реакции представляется уравнением, которое было получено шведским химиком Сванте Аррениусом из термодинамических соображений:
. В результате скорость химической реакции представляется уравнением, которое было получено шведским химиком Сванте Аррениусом из термодинамических соображений:
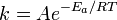
Здесь  характеризует частоту столкновений реагирующих молекул,
характеризует частоту столкновений реагирующих молекул,  — универсальная газовая постоянная.
— универсальная газовая постоянная.
ЭНЕРГИЯ АКТИВАЦИИ в элементарных р-циях, миним. энергия реагентов (атомов, молекул и др. частиц), достаточная для того, чтобы они вступили в хим. р-цию, т. е. для преодоления барьера на пов-сти потенциальной энергии, отделяющего реагенты от продуктов р-ции.
Стерический фактор – один из важнейших параметров кинетики химической реакции, определяется вероятностью вступления в реакцию двух столкнувшихся частиц, обладающих достаточной энергией. Название связано с зависимостью результата столкновения частиц от их взаимной ориентации при ударе. Для реакций атомов и одноатомных молекул с молекулами – стерический фактор близок к 1. Для реакций крупных молекул и радикалов с молекулами он изменяется от 10–3 до 10–6 и даже до 10–10
Суть теории переходного состояния (активированного комплекса):
1) частицы реагентов при взаимодействии теряют свою кинетическую энергию, которая превращается в потенциальную, и для того чтобы реакция свершилась, необходимо преодолеть некий барьер потенциальной энергии;
2) разница между потенциальной энергией частиц и упомянутым энергетическим барьером и есть энергия активации;
3) переходное состояние находится в равновесии с реагентами;
4) в тех реакциях, где энергия активации существенно ниже энергии разрыва химических связей, процессы образования новых связей и разрушения старых связей могут полностью или частично совпадать по времени.
 2018-01-21
2018-01-21 1100
1100
