ЭНЕРГИЯ АКТИВАЦИИ в элементарных р-циях, миним. энергия реагентов (атомов, молекул и др. частиц), достаточная для того, чтобы они вступили в хим. р-цию, т. е. для преодоления барьера на пов-сти потенциальной энергии, отделяющего реагенты от продуктов р-ции. Потенциальный барьер - максимум потенциальной энергии, через к-рый должна пройти система в ходе элементарного акта хим. превращения. Высота потенциального барьера для любого пути, проходящего через переходное состояние, равна потенциальной энергии в переходном состоянии. Если в сложной р-ции, состоящей из последовательных и параллельных элементарных р-ций, имеется лимитирующая элементарная р-ция (р-ция с макс. характерным временем), то ее энергия активации является и энергией активации сложной р-ции. В макроскопич. хим. кинетике энергия активации-энергетич. параметр Еа, входящий в Аррениуса уравнение:  где к - константа скорости; А - предэкспоненциальный множитель (постоянная или слабо зависящая от т-ры величина); k - константа Больцмана; Т - абс. т-ра. График зависимости lnk от 1/kT (аррениусов график) - прямая линия. Наблюдаемая энергия активации вычисляется из тангенса угла наклона этой прямой. В общем случае сложных р-ций параметр Еа в ур-нии Аррениуса является ф-цией энергии активации отдельных стадий, и определяемая энергия активации наз. эффективной (эмпирической, кажущейся).
где к - константа скорости; А - предэкспоненциальный множитель (постоянная или слабо зависящая от т-ры величина); k - константа Больцмана; Т - абс. т-ра. График зависимости lnk от 1/kT (аррениусов график) - прямая линия. Наблюдаемая энергия активации вычисляется из тангенса угла наклона этой прямой. В общем случае сложных р-ций параметр Еа в ур-нии Аррениуса является ф-цией энергии активации отдельных стадий, и определяемая энергия активации наз. эффективной (эмпирической, кажущейся).
Любой процесс, сопровождающийся к.-л. изменением энергии, является экзотермическим в одном направлении и эндотермическим в другом. Энергии активации экзотермич. и эндотермич. направлений р-ции, обозначаемые соотв.  и
и  , связаны соотношением:
, связаны соотношением: 
где Q -.теплота р-ции при Т= 0.
Для р-ций рекомбинации своб. радикалов (в т. ч. и атомов), а также для широкого класса экзотермич. ионно-молекулярных реакций энергия активации равна нулю или очень мала по сравнению с типичными значениями энергий хим. связей Есв. Для р-ций, сопровождающихся одновременно разрывом одних и образованием других хим. связей,  составляет обычно от сотых до десятых долей Есв, если среди реагентов есть своб. радикалы, и сравнима с Есв , если реагенты - химически насыщенные молекулы.
составляет обычно от сотых до десятых долей Есв, если среди реагентов есть своб. радикалы, и сравнима с Есв , если реагенты - химически насыщенные молекулы. 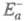 м. б. аномально большой (напр., больше энергии возбуждения атома Е*) в р-циях тушения электронного возбуждения при столкновениях атомов: А* + А
м. б. аномально большой (напр., больше энергии возбуждения атома Е*) в р-циях тушения электронного возбуждения при столкновениях атомов: А* + А  А + А, если точка пересечения термов реагентов и продуктов р-ции расположена высоко по сравнению с Е* или термы не пересекаются.
А + А, если точка пересечения термов реагентов и продуктов р-ции расположена высоко по сравнению с Е* или термы не пересекаются.
Известны эмпирич. корреляции, устанавливающие приближенную связь между Еа и Q для однотипных р-ций, напр. правило Поляни-Семенова:

где Е0и 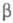 - константы. Теоретич. расчеты Еа производятся приближенными методами квантовой химии. Точные последовательные квантовомех. вычисления выполнены пока для систем, содержащих не более 3 электронов, напр. для 3 атомов водорода.
- константы. Теоретич. расчеты Еа производятся приближенными методами квантовой химии. Точные последовательные квантовомех. вычисления выполнены пока для систем, содержащих не более 3 электронов, напр. для 3 атомов водорода.
 2018-01-21
2018-01-21 405
405







