К ван-дер-ваальсовым силам относятся взаимодействия между диполями (постоянными и индуцированными). Название связано с тем фактом, что эти силы являются причиной поправки на внутреннее давление в уравнении состояния реального газа Ван-дер-Ваальса. Эти взаимодействия в основном определяют силы, ответственные за формирование пространственной структуры биологических макромолекул.
Ван-дер-ваальсовы силы также возникают между частицей (макроскопической частицей или наночастицей) и молекулой и между двумя частицами
Водородная связь — форма ассоциации между электроотрицательным атомом и атомом водорода H, связанным ковалентно с другим электроотрицательным атомом. В качестве электроотрицательных атомов могут выступать N, O или F. Водородные связи могут быть межмолекулярными или внутримолекулярными
Энергия водородной связи значительно меньше энергии обычной ковалентной связи (не превышает 40 кДж/моль). Однако этой энергии достаточно, чтобы вызвать ассоциацию молекул, то есть их объединение в димеры или полимеры. Именно ассоциация молекул служит причиной аномально высоких температур плавления и кипения таких веществ, как фтороводород, вода, аммиак.
Связь этого типа, хотя и слабее ионной и ковалентной связей, тем не менее играет очень важную роль во внутри- и межмолекулярных взаимодействиях. Водородные связи во многом обусловливают физические свойства воды и многих органических жидкостей (спирты, карбоновые кислоты, амиды карбоновых кислот, сложные эфиры).
Прочность водородной связи (энтальпия образования комплекса) зависит от полярности комплекса и колеблется от ~ 6 кДж/моль для комплексов молекул галогеноводородов с инертными газами до 160 кДж/моль для ион-молекулярных комплексов (AHB)±; так, для комплекса (H2O•H•OH2)+ образованного H2O и H3O+ — 132 кДж/моль в газовой фазе.
А)Термохимические уравнения включают в себя кроме химических формул тепловой эффект реакции. Числовое значение в уравнении реакции строго соответствует количествам веществ, участников реакции, т.е. коэффициентам. Благодаря этому соответствию, можно установить пропорциональные отношения между количеством вещества или массой и количеством теплоты в этой реакции.
Например: Термохимическое уравнение разложения малахита
(CuOH)2 CO3 = 2CuO + H 2 O + CO 2 - 47 кДж
Мы видим, что на разложение 1 моля малахита необходимо израсходовать 47 кДж, при этом образуется 2 моля оксида меди, 1 моль воды и 1 моль углекислого газа. Если мы затратим энергии в 2 раза больше, мы сумеем разложить 2 моля малахита, при этом получим 4 моля оксида меди, 2 моля воды и 2 моля углекислого газа.
Аналогично можно установить пропорциональные отношения, используя коэффициенты и молярные массы участников реакции. 47 кДж энергии затратится на разложение 94 г малахита, при этом выделится 160 г оксида меди, 18 г воды и 44 г углекислого газа. Пропорция несложная, но, используя массовые числа, учащиеся часто допускают расчетные ошибки, поэтому я рекомендую решать задачи с пропорциями через количество вещества.б) Реакции, в которых выделяется тепло, называются экзотермическими, реакции, в которых оно поглощается, — эндотермическими. Количество выделенного или поглощенного в ходе реакции тепла называется тепловым эффектом химической реакции и обозначается обычно символом Q. В случае, когда в ходе реакции меняется объем (например, при выделении или поглощении газов) тепловой эффект зависит от того, проводится реакция при постоянном объеме или постоянном давлении (то есть от того, совершается работа или нет). Поэтому для общности тепловые эффекты указываются для реакций при постоянном объеме. При этом тепловой эффект реакции совпадает по величине и противоположен по знаку разнице энтальпии (H) продуктов реакции и исходных веществ. Q=-H
Энтальпия Н — это функция состояния вещества, то есть определенное его свойство, постоянное для одного количества одного и того же вещества при одних и тех же условиях. Она является мерой внутренней энергии вещества при постоянном объеме. Соответственно изменение энтальпии в реакции является численной характеристикой разницы внутренней энергии продуктов реакции и исходных веществ.
При экзотермических реакциях (тепло выделяется) H отрицательно, при эндотермических - положительно. С использованием величины изменения энтальпии термохимические уравнения записываются следующим образом:
Н2+Сl2=2НСl, H=-184.6 кДж
В справочных таблицах приводятся энтальпии образования веществ при стандартных условиях (Т=298 К, P=105 Па).
Энтальпией образования вещества называется изменение энтальпии при реакции образования одного моля этого вещества из простых веществ в их самых стабильных аллотропных модификациях при стандартных условиях.
Из этого определения следует, что энтальпия образования простых веществ (в наиболее стабильных аллотропных модификациях) всегда равна нулю.
При написании термохимических уравнений всегда указывается агрегатное состояние вещества, поскольку энтальпия образования одного и того же вещества различна для различных его агрегатных состояний.
А) В основе термохимических расчетов лежит закон, открытый русским ученым Г. И. Гессом в 1840 г. Закон гласит: тепловой эффект реакции зависит от вида и состояния исходных веществ и конечных продуктов, но не зависит от пути перехода (из начального состояния в конечное).
Или иначе: тепловое эффект реакции равен алгебраической сумме тепловых эффектов всех его промежуточных стадий:
ΔН = ΔН1 + ΔН2.
Следствия из закона Гесса:
Если в результате последовательных химических реакций система приходит в состояние, полностью совпадающее с исходным (круговой процесс), то сумма тепловых эффектов этих реакций будет равна нулю.
2. Тепловой эффект реакций (ΔНх.р.) равен сумме теплот образования (или ΔНобр.) конечных веществ (ΔНконеч. в-в) за вычетом суммы теплот образования исходных веществ (ΔНисх. в-в):
ΔНх.р. = Σ ΔНпрод. р-ции – Σ ΔНисх. в-в.
б) Наиболее важное для практики следствие закона Гесса: - энтальпия химической реакции равна разности между суммой энтальпий образования продуктов реакции минус и суммой энтальпийи образования исходных веществ (реагентов).  (2.6)
(2.6)
Например, значение энтальпии реакции между растворами сильной кислоты и сильного основания может быть получено по табличным данным энтальпий образования исходных веществ., если представить эту реакцию:, например HCl (р-р) + NaOH (р-р) = NaCl (р-р) + Н2О ж может быть получено по табулированным энтальпиям образования в виде реакций между ионами, поскольку эта реакция в действительности является реакцией между ионами H+ и OH–: H+ (р-р) + OH– (р-р) = Н2О ж (2.7) Уравнение (2.7) - это уравнение реакции нейтрализации. Оно справедливо для всех реакций между сильной кислотой и сильным основанием, а следовательно и энтальпия этих реакцийодно и тоже для будет одна и та же.Табличные значения энтальпий образования (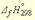 ) ионов Н+ и ОН– и молекулы Н2О ж известны и соответственно равны 0, –229,94 и –285,84 кДж/моль, соответственно. Тогда, по формуле (2.6) тепловой эффект реакции нейтрализации:
) ионов Н+ и ОН– и молекулы Н2О ж известны и соответственно равны 0, –229,94 и –285,84 кДж/моль, соответственно. Тогда, по формуле (2.6) тепловой эффект реакции нейтрализации:
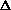 rHо =
rHо = 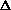 fH (H2O ж) –
fH (H2O ж) – 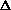 fH (H+ р-р) –
fH (H+ р-р) –  fH (OH– р-р) =–285,84 – (–229,94) = –55,9 кДж/моль
fH (OH– р-р) =–285,84 – (–229,94) = –55,9 кДж/моль
19)а) Л. Больцман определил энтропию как термодинамическую вероятность состояния (беспорядок) системы W. Энтропия связана с термодинамической вероятностью соотношением:
|
Размерность энтропии 1 моля вещества совпадает с размерностью газовой постоянной R и равна Дж∙моль–1∙K–1. Изменение энтропии *) в необратимых и обратимых процессах передается соотношениями Δ S > Q / T и Δ S = Q / T. Например, изменение энтропии плавления равно теплоте (энтальпии) плавления Δ S пл = Δ H пл/ T пл. Для химической реакции изменение энтропии аналогично изменению энтальпии
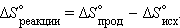
|
*) термин энтропия был введен Клаузиусом (1865 г.) через отношение Q / T (приведенное тепло).
Здесь Δ S ° соответствует энтропии стандартного состояния. Стандартные энтропии простых веществ не равны нулю. В отличие от других термодинамических функций энтропия идеально кристаллического тела при абсолютном нуле равна нулю (постулат Планка), поскольку W = 1.
Энтропия вещества или системы тел при определенной температуре является абсолютной величиной. В табл. 4.1 приведены стандартные энтропии S ° некоторых веществ.
|
Из табл. следует, что энтропия зависит от:
- агрегатного состояния вещества. Энтропия увеличивается при переходе от твердого к жидкому и особенно к газообразному состоянию (вода, лед, пар).
- изотопного состава (H2O и D2O).
- молекулярной массы однотипных соединений (CH4, C2H6, н-C4H10).
- строения молекулы (н-C4H10, изо-C4H10).
- кристаллической структуры (аллотропии) – алмаз, графит.
Наконец, рис. 4.3 иллюстрирует зависимость энтропии от температуры.

|
| Зависимость энтропии от температуры для свинца:Δ S пл = 8 Дж·моль–1·К–1; T пл = 600,5 К;Δ S кип = 88 Дж·моль–1·К–1; T кип = 2013 К |
Следовательно, стремление системы к беспорядку проявляется тем больше, чем выше температура. Произведение изменения энтропии системы на температуру T Δ S количественно оценивает эту тендецию и называется энтропийным фактором.
б) Для реакции, протекающей в изобарно- изотермических условиях, в некотором неравновесном исходном состоянии энергии Гиббса или химические потенциалы реагирующих веществ и продуктов реакции в общем случае не одинаковы, их разность (ΔGT) может быть рассчитана по уравнению:

где 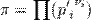 — отношение парциальных давлений участников реакции в исходном состоянии в степенях, равных их стехиометрическим коэффициентам; R —универсальная газовая постоянная.
— отношение парциальных давлений участников реакции в исходном состоянии в степенях, равных их стехиометрическим коэффициентам; R —универсальная газовая постоянная.
Это уравнение называют уравнением изотермы химической реакции. Оно позволяет рассчитать изменение энергии Гиббса при протекании процесса и определить направление протекания реакции:
при 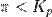
 — реакция идёт в прямом направлении, слева направо;
— реакция идёт в прямом направлении, слева направо;
при 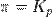
 — реакция достигла равновесного состояния;
— реакция достигла равновесного состояния;
при 
 — реакция идёт в обратном направлении.
— реакция идёт в обратном направлении.
Стандартная константа равновесия связана со стандартной энергией Гиббса реакции соотношением:
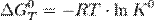
 2018-01-21
2018-01-21 318
318

 (Дж∙моль–1∙K–1)
(Дж∙моль–1∙K–1)







