Азотная кислота (HNO3) — сильная одноосновная кислота. Бесцветная, дымящая на воздухе жидкость. Она смешивается с водой в любых соотношениях. В водных растворах она практически полностью диссоциирует на ионы. Известны два твёрдых гидрата: моногидрат (HNO3·H2O) и тригидрат (HNO3·3H2O).
Способ её производства основан на каталитическом окислении синтетического аммиака на платино-родиевых катализаторах до смеси оксидов азота, с дальнейшим поглощением их водой
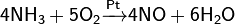

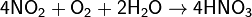
Концентрация полученной таким методом азотной кислоты колеблется в зависимости от технологического оформления процесса от 45 до 58 %. Для получения концентрированной азотной кислоты либо смещают равновесие в третьей реакции путём повышения давления до 50 атмосфер, либо в разбавленную азотную кислоту добавляют серную кислоту и нагревают, при этом азотная кислота, в отличие от воды и серной кислоты, испаряется.
Чистую азотную кислоту получил впервые Иоганн Рудольф Глаубер, действуя на селитру концентрированной серной кислотой:

Дальнейшей дистилляцией может быть получена т. н. «дымящая азотная кислота», практически не содержащая воды.
Применение
· в производстве минеральных удобрений;
· в военной промышленности (дымящая — в производстве взрывчатых веществ, как окислитель ракетного топлива, разбавленная — в синтезе различных веществ, в том числе отравляющих);
· в производстве красителей и лекарств (нитроглицерин).
· в ювелирном деле — основной способ определения золота в золотом сплаве.
Химические свойства.
Высококонцентрированная HNO3 имеет обычно бурую окраску вследствие происходящего на свету процесса разложения.
HNO3 как сильная одноосновная кислота взаимодействует:
а) с основными и амфотерными оксидами и основаниями.
в) вытесняет слабые кислоты из их солей.
Азотная кислота в любой концентрации проявляет свойства кислоты-окислителя.
Смесь трех объёмов соляной кислоты и одного объёма азотной называется «царской водкой». Царская водка растворяет большинство металлов, в том числе золото и платину. Её сильные окислительные способности обусловлены образующимся атомарным хлором и хлоридом нитрозила:



 2018-01-21
2018-01-21 1960
1960
