Произведение растворимости (ПР, Ksp) — произведение концентрации ионов малорастворимого электролита в его насыщенном растворе при постоянной температуре и давлении. Произведение растворимости — величина постоянная.
При постоянной температуре в насыщенных водных растворах малорастворимых электролитов устанавливается равновесие между твердым веществом и ионами, образующими это вещество.
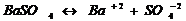 ;
; 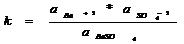 ;
; 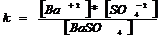 ;
; 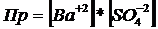
31) Степень окисления элемента.
Сте́пень окисле́ния (окислительное число, формальный заряд) — вспомогательная условная величина для записи процессов окисления, восстановления и окислительно-восстановительных реакций, численная величина электрического заряда, приписываемого атому в молекуле в предположении, что электронные пары, осуществляющие связь, полностью смещены в сторону более электроотрицательных атомов.
Представления о степени окисления положены в основу классификации и номенклатуры неорганических соединений.
Степень окисления соответствует заряду иона или формальному заряду атома в молекуле или в химической формальной единице, например:
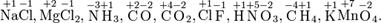
Степень окисления указывается сверху над символом элемента. В отличие от указания заряда иона, при указании степени окисления первым ставится знак, а потом численное значение, а не наоборот:
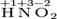 — степень окисления,
— степень окисления,
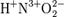 — заряды.
— заряды.
Степень окисления атома в простом веществе равна нулю, например:
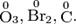
Алгебраическая сумма степеней окисления атомов в молекуле всегда равна нулю:
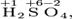
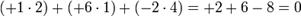
32) Окислительные и восстановительные свойства простых веществ и химических соединений.
Окислительно-восстановительные реакции (ОВР) – это хим. Реакции в ходе которых происходят изменения степени окисления атомов входящих в состав реагирующих веществ.
Окисление и восстановление – это 2 противоположных и взаимносвязанных процессов.
Понижение и восстановление степени окис. Атомов отражается в электронных ур-ях. О способности того или иного вещ-ва проявлять восст или двойственные (окис и восст) св-ва можно судить по степени окис. Элементов.
1) Атом элемента проявляет т-о окис св-ва, если он нах-ся в высшей степени окис-я (т.е. он не может ее повысить и отдать электрон)
2) Атом элемента проявляет только восст-ые св-ва если элемент нах-ся в низшей стаепени окисления (т.е. атом не может понижать степень окисления и принимать электрон)
3) Атом проявляет двойственные св-ва,если он нах-ся в промежутчной степени окисления.
 2018-01-21
2018-01-21 754
754








