Электролитические процессы- это окислительно-восстановительные реакции, которые протекают под воздействием эл.тока или сопровождаются возникновением эл.тока.
Гальв.элемент: Он состоит из медной пластины, погруженной в раствор CuSO4 и цинковой пластины, погруженной в раствор ZnSO4. На поверхности цинковой и медной пластин возникает двойной электрический слой и устанавливается равновесие, характеризующееся определенными значениями ЭП.
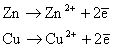
Вследствие большей активности цинка с его поверхности уходит больше ионов и на поверхности металлической пластины возникает больший избыток электронов. Поэтому при замыкании внешней цепи, т.е. при соединении цинка с медью металлическим проводником, электроны будут переходить от цинка к меди. В результате этого процесса равновесие на цинковом электроде сместится вправо, поэтому в раствор перейдет дополнительное количество ионов цинка. В то же время равновесие на медном электроде сместится влево и произойдет разряд дополнительного количества ионов меди.
Таким образом, при замыкании внешней цепи возникают самопроизвольные процессы растворения цинка на цинковом электроде и выделения меди на медном электроде. (Чтобы предотвратить явление, известное как “запирание ГЭ”, т.е. дать возможность ионам соли свободно перемещаться из одного раствора в другой, используют солевой мостик. Он представляет собой изогнутую (U- образную) стеклянную трубку, заполненную насыщенным раствором хлорида калия. Данные процессы будут продолжаться до тех пор, пока не выровняются потенциалы электродов или не растворится цинковая пластина (или не высадятся из раствора все ионы меди).
Итак, при работе медно-цинкового элемента протекают следующие основные процессы:
1) реакция окисления цинка

Процессы окисления в электрохимии получили название анодных процессов, а электроды, на которых идут процессы окисления, называют анодами;
2) реакция восстановления ионов меди

Процессы восстановления в электрохимии получили название катодных процессов, а электроды, на которых идут процессы восстановления, называют катодами;
3) движение электронов во внешней цепи;
4) движение ионов в растворе.
Суммируя электродные реакции, получаем:
Zn + Cu2+ = Cu + Zn2+
Вследствие этой химической реакции в ГЭ возникает электрический ток, поэтому ее называют токообразующей.
(-) A Zn | Zn2+ || Cu2+ | Cu K (+)
 2018-01-21
2018-01-21 1620
1620








