Биосинтез гумулонов и лупулонов. спросить
Механизм превращения гумулонов в изогумолны в пивоварении:

Механизм превращения горьких веществ при хранении:

Химический состав хмеля
В составе хмеля различают общие составные части, свойственные любому растению, и специфические, характерные только для хмеля. К общим составным частям относятся протеиновые вещества, жир, воск безазотистые экстрактивные вещества, клетчатка и минеральные вещества. Для пивоварения исключительную ценность представляют специфические составные части хмеля, не встречающиеся в подобной форме в других растениях - горькие вещества, хмелевое масло и дубильные вещества.
Средние значения химического состава сухого хмеля
| Название вещества | % | Название вещества | % |
| вода | 12,5 | эфирные масла | 0,4 |
| зола | 7,5 | эфирная вытяжка | 18,3 |
| клетчатка | 13,3 | дубильные вещества | 3,0 |
| азотистые вещества | 17,5 | безазотистые экстрактивные вещества | 27,5 |
Гумулоны. Растворяясь в кипятке образует коллоидный раствор при охлаждении часть выпадает и кристаллизуется. Растворимость его в воде зависит от активной кислотности. Без кислород в обычных условиях гумулон стабилен. При окислении под действием кислорода воздуха гумулон переходит в мягкую a-кислоту. При наличии воды процессы окисления идут быстрее. Гумолон является хорошим пенообразователем. Пенообразующая способность выше чем у лупулонов. Обладает антисептическим действием.
Лупулон. Растворимость меньше чем у гумулона. Также лупулон менее стабилен, при действии кислорода. При окислении даёт β-смолу. Горечь и пенообразование ниже, чем у гумулона. Антисептическая активность выше.
Мягкие смолы. Образуются в хмеле при хранении. Растворимы в сусле и образуют коллоидные растворы. Мягкие смолы у которых горечь слабее и антисептические свойства ниже в силу своей высокой растворимости в сусле и пиве представляют большую ценность. Оказывая влияние на стойкость пены. Подавляют жизнедеятельность молочно-кислых, масляно-кислых бактерий. Не оказывают влияние на жизнедеятельность дрожжей.
 Он относится к сесквитерпенам и является главной составной частью хмелевого масла. При окислении гумулен переходит в диметилянтарную кислоту.
Мирцен (СНз)2С=СНСН2СН2С(=СН2)СН=СН2 является терпеном и представляет собой бесцветную легкоподвижную жидкость с резким запахом. При окислении мирцена получается янтарная кислота.
Свежеперегнанное хмелевое масло на 80-90 % состоит из гумулена и мирцена, остальное приходится на линалоол (С10Н16О), его эфир с изониловой кислотой C10H18О2 и гераниол (С10Н18О) следующего строения: (СНз)2С=СНСН2СН2С(СН3)=СНСН2ОН.
Линалоолявляется структурным изомером гераниола и имеет формулу (СН3)2С=СН(СН2)2С(СН3)(ОН)СН=СН2. Линалоол так же, как и гераниол, является ненасыщенным. Он представляет собой бесцветное масло с запахом, напоминающим аромат ландыша. Несмотря на то что линалоол в хмелевом масле содержится в небольшом количестве, он оказывает большое влияние на аромат хмеля.
Кариофиллен является бициклическим сесквитерпеном и представляет собой смесь нескольких изомеров, различающихся по расположению двойных связей:
Он относится к сесквитерпенам и является главной составной частью хмелевого масла. При окислении гумулен переходит в диметилянтарную кислоту.
Мирцен (СНз)2С=СНСН2СН2С(=СН2)СН=СН2 является терпеном и представляет собой бесцветную легкоподвижную жидкость с резким запахом. При окислении мирцена получается янтарная кислота.
Свежеперегнанное хмелевое масло на 80-90 % состоит из гумулена и мирцена, остальное приходится на линалоол (С10Н16О), его эфир с изониловой кислотой C10H18О2 и гераниол (С10Н18О) следующего строения: (СНз)2С=СНСН2СН2С(СН3)=СНСН2ОН.
Линалоолявляется структурным изомером гераниола и имеет формулу (СН3)2С=СН(СН2)2С(СН3)(ОН)СН=СН2. Линалоол так же, как и гераниол, является ненасыщенным. Он представляет собой бесцветное масло с запахом, напоминающим аромат ландыша. Несмотря на то что линалоол в хмелевом масле содержится в небольшом количестве, он оказывает большое влияние на аромат хмеля.
Кариофиллен является бициклическим сесквитерпеном и представляет собой смесь нескольких изомеров, различающихся по расположению двойных связей:
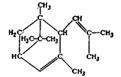 Содержание кариофиллена в масле хмеля колеблется в пределах 10—20 %.
Тяжелые фракции хмелевого масла представлены кислотами, которые со спиртами образуют эфиры, сообщающие хмелю разные оттенки аромата. Фракции хмелевого масла, еще более тяжелые, содержат изовалериановую кислоту и разные альдегиды, главным образом формальдегид.
Наряду сприятным ароматом хмелевое масло обладает весьма ценным свойством задерживать превращения мягких смол в малоценные твердые смолы. Легко окисляясь, хмелевое масло предохраняет от окисления горькие и дубильные вещества хмеля.
Содержание кариофиллена в масле хмеля колеблется в пределах 10—20 %.
Тяжелые фракции хмелевого масла представлены кислотами, которые со спиртами образуют эфиры, сообщающие хмелю разные оттенки аромата. Фракции хмелевого масла, еще более тяжелые, содержат изовалериановую кислоту и разные альдегиды, главным образом формальдегид.
Наряду сприятным ароматом хмелевое масло обладает весьма ценным свойством задерживать превращения мягких смол в малоценные твердые смолы. Легко окисляясь, хмелевое масло предохраняет от окисления горькие и дубильные вещества хмеля.
6 Углеводы играют важную роль в формировании вкуса и аромата спиртных напитков. Под действием ферментов дрожжей углеводы сбраживаются с образованием этилового спирта. Который является неотъемлемой частью всех спиртных напитков. Так же участвуют в формировании органолептических качеств спиртных напитков.
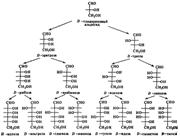
 Сахаромицеты способны сбраживать такие гексозы: альдозы – манноза, глюкоза, галактоза и фруктоза относящаяся к кетозам. Отличие кетоз от альдоз положением корбонильной группы. Если карбонильная группа находится в конце цепи то это альдоза, если в любом другом то это кетоза. Два сахара, отличающихся только по конфигурации относительно одного определенного атома углерода, называются эпимерами. Так, D-глюкоза и D-манноза являются эпимерами по 2-му атому углерода, а D-глюкоза и D-галактоза — эпимерами по С-4.
Разбавленные водные растворы оснований при комнатной температуре вызывают перегруппировки относительно аномерного атома углерода и соседнего с ним углерода, не затрагивая замещающие группы при других углеродных атомах. Так, например, в результате обработки D-глюкозы разбавленной щелочью образуется равновесная смесь D-глюкозы, D-фруктозы и D-маннозы. Считается, что в ходе этих реакций образуются также енольные формы оксиальдегидных и оксикетонных структур при С-1 и С-2; эти енольные формы называются ендиолами:
Сахаромицеты способны сбраживать такие гексозы: альдозы – манноза, глюкоза, галактоза и фруктоза относящаяся к кетозам. Отличие кетоз от альдоз положением корбонильной группы. Если карбонильная группа находится в конце цепи то это альдоза, если в любом другом то это кетоза. Два сахара, отличающихся только по конфигурации относительно одного определенного атома углерода, называются эпимерами. Так, D-глюкоза и D-манноза являются эпимерами по 2-му атому углерода, а D-глюкоза и D-галактоза — эпимерами по С-4.
Разбавленные водные растворы оснований при комнатной температуре вызывают перегруппировки относительно аномерного атома углерода и соседнего с ним углерода, не затрагивая замещающие группы при других углеродных атомах. Так, например, в результате обработки D-глюкозы разбавленной щелочью образуется равновесная смесь D-глюкозы, D-фруктозы и D-маннозы. Считается, что в ходе этих реакций образуются также енольные формы оксиальдегидных и оксикетонных структур при С-1 и С-2; эти енольные формы называются ендиолами:
 При высоких температурах или высоких концентрациях щелочей свободные моносахариды подвергаются перегруппировкам, расщеплению и полимеризации. Некоторые полисахариды устойчивы к действию щелочей.
При высоких температурах или высоких концентрациях щелочей свободные моносахариды подвергаются перегруппировкам, расщеплению и полимеризации. Некоторые полисахариды устойчивы к действию щелочей.
| 7 Углеводы играют важную роль в формировании вкуса и аромата спиртных напитков. Под действием ферментов дрожжей углеводы сбраживаются с образованием этилового спирта. Который является неотъемлемой частью всех спиртных напитков. Так же участвуют в формировании органолептических качеств спиртных напитков.
 Формулы Хеуорса. Для циклических форм моносахаридов приняты перспективные формулы Хеуорса, в которых циклы изображаются в виде плоских многоугольников, лежащих перпендикулярно плоскости рисунка. Атом кислорода располагается в пиранозном цикле в дальнем правом углу, в фуранозном — за плоскостью цикла. Символы атомов углерода в циклах не пишутся.
Формулы Хеуорса. Для циклических форм моносахаридов приняты перспективные формулы Хеуорса, в которых циклы изображаются в виде плоских многоугольников, лежащих перпендикулярно плоскости рисунка. Атом кислорода располагается в пиранозном цикле в дальнем правом углу, в фуранозном — за плоскостью цикла. Символы атомов углерода в циклах не пишутся.
 При написании формул Хеуорса руководствуются следующими правилами. В фишеровской проекционной формуле моносахарида производят две перестановки заместителей при том асимметрическом атоме углерода, гидроксильная группа которого примет участие в образовании оксидного цикла (что не меняет конфигурации этого атома углерода). Перестановки производят с условием, чтобы данная гидроксильная группа оказалась внизу, т. е. на одной проекционной линии с атомами углерода. Затем замыкают оксидный цикл.
При написании формул Хеуорса руководствуются следующими правилами. В фишеровской проекционной формуле моносахарида производят две перестановки заместителей при том асимметрическом атоме углерода, гидроксильная группа которого примет участие в образовании оксидного цикла (что не меняет конфигурации этого атома углерода). Перестановки производят с условием, чтобы данная гидроксильная группа оказалась внизу, т. е. на одной проекционной линии с атомами углерода. Затем замыкают оксидный цикл.

|
| 7.2 От преобразованной таким образом фишеровской проекционной формулы переходят к формуле Хеуорса. Заместители, находящиеся слева от углеродной цепи в фишеровской проекции, в формуле Хеуорса располагают над плоскостью цикла; заместители, расположенные справа, — под плоскостью. Мутаротация. Аномерия. Многие моносахариды в водном растворе ведут себя так, как будто число содержащихся в них асимметрических центров больше, чем это следует из их структурных формул, соответствующих открытой цепи. D-глюкоза может существовать в виде двух различных изомерных форм: a-D-глюкозы, для которой [a]D20 = +112,2°, и b-D-глюкозы, для которой [a]D20 = + 18,7°. Оба эти соединения были выделены в чистом виде; оказалось, что они не различаются по своему элементарному составу. При растворении a и b изомеров D-глюкозы в воде оптическое вращение раствора постепенно меняется и в конце концов достигает равновесного значения [a]d20= + 52,7°. Это явление, называемое мутаротацией, обусловлено образованием равновесной смеси, которая при 25 °С состоит примерно на одну треть из a-D-глюкозы и на две трети из b-D-глюкозы. Исходя из различных химических соображений был сделан вывод, что эти a и b изомеры D-глюкозы не являются структурами с открытой цепью, а представляют собой замкнутые шестичленные кольца, образовавшиеся в результате реакции между спиртовой гидроксильной группой при С-5 и альдегидной группой при С-1. Из-за наличия в молекуле асимметрического атома углерода D-глюкопираноза может существовать в виде двух различных стереоизомеров (их обозначают буквами a и b). Изомерные формы моносахаридов, отличающиеся друг от друга лишь по конфигурации относительно полуацетального атома углерода, называются аномерами, а сам полуацеталъный атом углерода в этом случае называется аномерным углеродом | 7.3 Образовывать устойчивые кольца и существовать в виде аномерных форм способны только моносахариды, содержащие пять или большее число атомов углерода. Тетрозы и триозы в водном растворе могут иметь лишь структуру с открытой цепью.
Конформационное строение моносахаридов обуславливает формирование пространственного строения длинных полисахаридных цепей.
 а – аксиальная связь, э – экваториальная связь
Номенклатура кетоз.
а – аксиальная связь, э – экваториальная связь
Номенклатура кетоз.

|
8 Углеводы играют важную роль в формировании вкуса и аромата спиртных напитков. Под действием ферментов дрожжей углеводы сбраживаются с образованием этилового спирта. Который является неотъемлемой частью всех спиртных напитков. Так же участвуют в формировании органолептических качеств спиртных напитков.
  Механизмы образования фурфурола и оксиметилфурфурола
Механизмы образования фурфурола и оксиметилфурфурола
 
| 9 Углеводы играют важную роль в формировании вкуса и аромата спиртных напитков. Под действием ферментов дрожжей углеводы сбраживаются с образованием этилового спирта, который является неотъемлемой частью всех спиртных напитков. Так же участвуют в формировании органолептических качеств спиртных напитков.
  Крахмал представляет собой смесь двух полисахаридов, построенных из D-глюкопиранозы: амилозы (от10 до 20 %) и амилопектина (от 80 до 90 %). Линейную фракцию называют амилозой, нелинейную - амилопектином. Цепочковидная молекула амилозы, где глюкозные остатки связаны между собой в основном связью a-1-4, дает в чистом виде синее окрашивание с йодным раствором.
Крахмал представляет собой смесь двух полисахаридов, построенных из D-глюкопиранозы: амилозы (от10 до 20 %) и амилопектина (от 80 до 90 %). Линейную фракцию называют амилозой, нелинейную - амилопектином. Цепочковидная молекула амилозы, где глюкозные остатки связаны между собой в основном связью a-1-4, дает в чистом виде синее окрашивание с йодным раствором.
 Амилопектин имеет многократно разветвленную молекулу, также состоящую из глюкозидных остатков. В цепочках амилопектина молекулы связаны a-1-4-глюкозидной связью, а в точках ветвления имеется связь a-1-6, которая разрушается примерно в четыре раза труднее, чем связь a-1-4. При ферментативном гидролизе b-амилаза разрушает только наружные цепочковидные отростки молекулы амилопектина, имеющие связи a-1-4, и не может разрушить связи a-1-6 в точках ветвления. Остающаяся часть (сердцевина) молекулы амилопектина называется остаточными декстринами или b-декстринами.
Амилопектин, отделенный от амилозы, дает с йодом фиолетово-красное окрашивание.
Амилопектин имеет многократно разветвленную молекулу, также состоящую из глюкозидных остатков. В цепочках амилопектина молекулы связаны a-1-4-глюкозидной связью, а в точках ветвления имеется связь a-1-6, которая разрушается примерно в четыре раза труднее, чем связь a-1-4. При ферментативном гидролизе b-амилаза разрушает только наружные цепочковидные отростки молекулы амилопектина, имеющие связи a-1-4, и не может разрушить связи a-1-6 в точках ветвления. Остающаяся часть (сердцевина) молекулы амилопектина называется остаточными декстринами или b-декстринами.
Амилопектин, отделенный от амилозы, дает с йодом фиолетово-красное окрашивание.
 Углеводы сусла могут получиться либо под действием ферментов солода, либо под действием грибных амилаз. При осахаривании солодом и грибными амилазами состав сахаридов сильно отличается друг от друга. При осахаривании ферментами солода в сусле находидся мальтоза, основное кол – во кот. образуется в первые 30 мин, осахаривание в дальнейшем возрастает незначительно небольшим изменениям подвергаются декстрины и трисахариды. Содержание глюкозы остается постоянным.
При осахаривании ферментами грибов характерно изменение состава сложнее за 30 мин. возрастает кол-во всех сахаридов, причём содержание декстринов максимально через 10 мин. а затем плавно уменьшается содержание трисахаридов максимально ч\з 1-2 часа. Содержание продолжает увеличиваться до 5 часов а затем падает. Содержание глюкозы постоянно увеличивается.
Углеводы сусла могут получиться либо под действием ферментов солода, либо под действием грибных амилаз. При осахаривании солодом и грибными амилазами состав сахаридов сильно отличается друг от друга. При осахаривании ферментами солода в сусле находидся мальтоза, основное кол – во кот. образуется в первые 30 мин, осахаривание в дальнейшем возрастает незначительно небольшим изменениям подвергаются декстрины и трисахариды. Содержание глюкозы остается постоянным.
При осахаривании ферментами грибов характерно изменение состава сложнее за 30 мин. возрастает кол-во всех сахаридов, причём содержание декстринов максимально через 10 мин. а затем плавно уменьшается содержание трисахаридов максимально ч\з 1-2 часа. Содержание продолжает увеличиваться до 5 часов а затем падает. Содержание глюкозы постоянно увеличивается.
|
10 Углеводы играют важную роль в формировании вкуса и аромата спиртных напитков. Под действием ферментов дрожжей углеводы сбраживаются с образованием этилового спирта, который является неотъемлемой частью всех спиртных напитков. Так же участвуют в формировании органолептических качеств спиртных напитков.

 Дисахариды
Среди дисахаридов особенно широко известны мальтоза, лактоза, целлобиоза и сахароза. Мальтоза, образующаяся в качестве промежуточного продукта при действии амилаз на крахмал, содержит два остатка D – глюкопиранозы, связанных 1 – 4 гликозидной связью. Лактоза содержится в молоке, построена из остатков D – галактопиранозы и D – глюкопиранозы связанных 1 – 4 гликозидной связью. Целлобиоза как и мальтоза состоит из двух D – глюкопиранозильных остатков связанных 1 – 4 гликозидной связью. Отличие лишь в том что аномерный атом углерода, участвующий в образовании гликозидной связи имеет β-конфигурацию, получают путём не полного гидролиза целлюлозы. Все эти дисахара относят восстанавливающим. Сахарозу относят к не восстанавливающим. В её состав входят D – глюкопираноза и D – фруктофураноза. Гликозидная связь между ними образуется за счёт гидроксильных групп при аномерных атомах углерода. Содержится в троснике, свекле, соках растений и плодах. Отсюдо можно сделать вывод что данные дисахариды широко распростанены в природе.
Дисахариды
Среди дисахаридов особенно широко известны мальтоза, лактоза, целлобиоза и сахароза. Мальтоза, образующаяся в качестве промежуточного продукта при действии амилаз на крахмал, содержит два остатка D – глюкопиранозы, связанных 1 – 4 гликозидной связью. Лактоза содержится в молоке, построена из остатков D – галактопиранозы и D – глюкопиранозы связанных 1 – 4 гликозидной связью. Целлобиоза как и мальтоза состоит из двух D – глюкопиранозильных остатков связанных 1 – 4 гликозидной связью. Отличие лишь в том что аномерный атом углерода, участвующий в образовании гликозидной связи имеет β-конфигурацию, получают путём не полного гидролиза целлюлозы. Все эти дисахара относят восстанавливающим. Сахарозу относят к не восстанавливающим. В её состав входят D – глюкопираноза и D – фруктофураноза. Гликозидная связь между ними образуется за счёт гидроксильных групп при аномерных атомах углерода. Содержится в троснике, свекле, соках растений и плодах. Отсюдо можно сделать вывод что данные дисахариды широко распростанены в природе.
 мальтоза мальтоза
 лактоза лактоза
 сахароза
Восстанавливающие дисахариды. В них один из моносахаридных остатков участвует в образовании гликозидной связи за счёт гидроксильной группы чаще всего при С-4 или С-6, реже при С-3. В дисахариде имеется свободная полуацетальная гидроксильная группа, вследствие чего сохраняется способность к раскрытию цикла. Возможностью осуществления цикло-оксо-таутомерии обусловлены восстановительные свойства таких дисахаридов и мутаротация их растворов. В сахарозе отсутствуют свободные полуацетальные гидроксильные группы, поэтому она не способна к цикло-оксо-таутомерии и растворы её не мутаротируют, вследствии чего сахароза является не восстанавливающим сахаром. сахароза
Восстанавливающие дисахариды. В них один из моносахаридных остатков участвует в образовании гликозидной связи за счёт гидроксильной группы чаще всего при С-4 или С-6, реже при С-3. В дисахариде имеется свободная полуацетальная гидроксильная группа, вследствие чего сохраняется способность к раскрытию цикла. Возможностью осуществления цикло-оксо-таутомерии обусловлены восстановительные свойства таких дисахаридов и мутаротация их растворов. В сахарозе отсутствуют свободные полуацетальные гидроксильные группы, поэтому она не способна к цикло-оксо-таутомерии и растворы её не мутаротируют, вследствии чего сахароза является не восстанавливающим сахаром.
| 11. Углеводы играют важную роль в формировании вкуса и аромата спиртных напитков. Под действием ферментов дрожжей углеводы сбраживаются с образованием этилового спирта, который является неотъемлемой частью всех спиртных напитков. Так же участвуют в формировании органолептических качеств спиртных напитков.
  Взаимосвязь. Формулы Хеуорса. Для циклических форм моносахаридов приняты перспективные формулы Хеуорса, в которых циклы изображаются в виде плоских многоугольников, лежащих перпендикулярно плоскости рисунка. Атом кислорода располагается в пиранозном цикле в дальнем правом углу, в фуранозном — за плоскостью цикла. Символы атомов углерода в циклах не пишутся.
Взаимосвязь. Формулы Хеуорса. Для циклических форм моносахаридов приняты перспективные формулы Хеуорса, в которых циклы изображаются в виде плоских многоугольников, лежащих перпендикулярно плоскости рисунка. Атом кислорода располагается в пиранозном цикле в дальнем правом углу, в фуранозном — за плоскостью цикла. Символы атомов углерода в циклах не пишутся.
 При написании формул Хеуорса руководствуются следующими правилами. В фишеровской проекционной формуле моносахарида производят две перестановки заместителей при том асимметрическом атоме углерода, гидроксильная группа которого примет участие в образовании оксидного цикла (что не меняет конфигурации этого атома углерода). Перестановки производят с условием, чтобы данная гидроксильная группа оказалась внизу, т. е. на одной проекционной линии с атомами углерода. Затем замыкают оксидный цикл.
При написании формул Хеуорса руководствуются следующими правилами. В фишеровской проекционной формуле моносахарида производят две перестановки заместителей при том асимметрическом атоме углерода, гидроксильная группа которого примет участие в образовании оксидного цикла (что не меняет конфигурации этого атома углерода). Перестановки производят с условием, чтобы данная гидроксильная группа оказалась внизу, т. е. на одной проекционной линии с атомами углерода. Затем замыкают оксидный цикл.
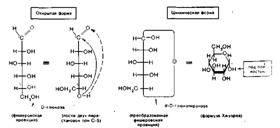 От преобразованной таким образом фишеровской проекционной формулы переходят к формуле Хеуорса. Заместители, находящиеся слева от углеродной цепи в фишеровской проекции, в формуле Хеуорса располагают над плоскостью цикла; заместители, расположенные справа, — под плоскостью.
Конформационное строение моносахаридов обуславливает формирование пространственного строения длинных полисахаридных цепей.
От преобразованной таким образом фишеровской проекционной формулы переходят к формуле Хеуорса. Заместители, находящиеся слева от углеродной цепи в фишеровской проекции, в формуле Хеуорса располагают над плоскостью цикла; заместители, расположенные справа, — под плоскостью.
Конформационное строение моносахаридов обуславливает формирование пространственного строения длинных полисахаридных цепей.
|
11.1
 а – аксиальная связь, э – экваториальная связь
При взаимодействии глюкозы и фруктозы с фенилгидрозином образуется один и тот же продукт – фенилозазон D – глюкозы:
а – аксиальная связь, э – экваториальная связь
При взаимодействии глюкозы и фруктозы с фенилгидрозином образуется один и тот же продукт – фенилозазон D – глюкозы:
 Сахароза с фенилгидразином не взаимодействует т.к. является не редуцирующим сахаром.
Сахароза с фенилгидразином не взаимодействует т.к. является не редуцирующим сахаром.
| 11.2
Лактоза:
 Механизм образования озазонов:
Фенилгидразин не является окисляющим агентом. Главной определяющей стадией реакции является диспропорционирование фенилгидразона II, которое приводит к образованию соединения III в результате миграции двух атомов водорода от вторичной спиртовой группы к двойной связи C = N:
Механизм образования озазонов:
Фенилгидразин не является окисляющим агентом. Главной определяющей стадией реакции является диспропорционирование фенилгидразона II, которое приводит к образованию соединения III в результате миграции двух атомов водорода от вторичной спиртовой группы к двойной связи C = N:
 Далее кетон III конденсируется с фенилгидразином, давая соединение IV, которое в результате аллильной перегруппировки прев-ся в V. В результате 1,4-элиминирования анилина получается соед-е VI или VII, либо вместе. Последующая конденсация имина с фенилгидразином приводит к образованию фенилозазона и аммиака.
Далее кетон III конденсируется с фенилгидразином, давая соединение IV, которое в результате аллильной перегруппировки прев-ся в V. В результате 1,4-элиминирования анилина получается соед-е VI или VII, либо вместе. Последующая конденсация имина с фенилгидразином приводит к образованию фенилозазона и аммиака.

|
12. Под действием ферментов белки гидролизуются на: альбумозы – первые продукты расщепления белка при кипячении не выделяются, а выделяются насыщенным раствором  ; пептоны – при кипячении не выделяется, осаждается фосфорномолибденовой кислотой или танином; полипетиды – продукты более глубокого расщепления по сравнению с пептонами; пептиды и а.к. – являются заключительными продуктами ферментативного гидролиза.
Рациональной химической классификации белков пока не существует. В основу наиболее распространенной системы классификации, положены два принципа: степень сложности и характер растворимости. По сложности строения белки разделяют на две большие группы — протеины (простые белки) и протеиды (сложные белки). Часть азота входит в состав не белковых соединений.
Протеины — белки, дающие при гидролитическом расщеплении только аминокислоты. Это запасные, скелетные (опорные) и ферментные белки. При изучении протеинов (растительныхбелков) используют метод извлечения их фракций по растворимости (альбумины, глобулины, проламины и глютелины), и предложенный американским исследователем Осборном.
Альбумины растворяются в воде, их можно выделить из раствора в виде сгустка денатурированного белка при кипячении. Из водных растворов альбумины осаждают также высаливанием при насыщении солями (сульфатом; аммония и др.). Альбуминный комплекс зерна в основном состоит из ферментов,
Глобулины растворяются в водных растворах различных солей (применяют обычно 5... 10%-ный раствор NaCl). В чистой воде они нерастворимы. Для выделения глобулина из солевого раствора применяют диализ с помощью полупроницаемых мембран или разбавляют большим количеством воды. Глобулины составляют большую часть семян бобовых культур. Проламины — наиболее характерные белки для зерна большинства злаковых культур. Они растворяются в 60...80%-ном растворе этанола. К проламинам относят глиадин из зерна пшеницы и ржи (составная часть клейковины), гордеин — ячменя, зеин — кукурузы, авенин — овса.
Глютелины растворяются в растворах щелочей (0,1...0,2%). Они мало изучены, так как их трудно выделить в чистом виде. Наиболее изучены глютелин зерна пшеницы (составная часть клейковины), оризенин риса и глютелин кукурузы. Разделение протеинов по растворимости носит условный характер.
Современными методами установлена гетерогенность каждой из названных белковых фракций. Каждая из них состоит из нескольких, во многих случаях из многих десятков различных белков, имеющих некоторые общие свойства.
Протеиды (сложные белки). Так называют вещества, состоящие из белка и соединения небелковой природы — простетической группы. По химической природе такие соединения подразделяют на липопротеиды, хромопротеиды, гликопротеиды и нуклеопротеиды.
Липопротеиды, кроме белка, содержат липиды. Липопротеиды в большом количестве входят в состав пластид растительной клетки, (хлоропласты), содержатся в протоплазме, особенно в мембранах. Хромопротеиды — разнообразная группа, в которую входит гемоглобин крови. В гемоглобине белок глобин связан со сложным азотистым соединением, содержащим железо. Это соединение является простетической группой и называется гемом. Гликопротеиды играют важную роль в построении протоплазмы. Они содержат различные углеводы.
Нуклеопротеиды имеют огромное значение в наследственности. Высоко содержание нуклеопротеидов в зародыше зерна. В нуклеопротеидах белок, связан с нуклеиновыми кислотами. Нуклеиновые кислоты наряду с белками относят к. наиболее важным биополимерам, образующим протоплазму живой клетки. Нуклеиновые кислоты представляют собой высокомолекулярные органические, кислоты, растворяющиеся в щелочных растворах и осаждающиеся при подкислении.
При гидролизе нуклеиновые кислоты распадаются на пуриновые основания, пиримидиновые основания, сахара, и, фосфорную кислоту. В состав нуклеиновых кислот входят пуриновые основания аденин и гуанин. ; пептоны – при кипячении не выделяется, осаждается фосфорномолибденовой кислотой или танином; полипетиды – продукты более глубокого расщепления по сравнению с пептонами; пептиды и а.к. – являются заключительными продуктами ферментативного гидролиза.
Рациональной химической классификации белков пока не существует. В основу наиболее распространенной системы классификации, положены два принципа: степень сложности и характер растворимости. По сложности строения белки разделяют на две большие группы — протеины (простые белки) и протеиды (сложные белки). Часть азота входит в состав не белковых соединений.
Протеины — белки, дающие при гидролитическом расщеплении только аминокислоты. Это запасные, скелетные (опорные) и ферментные белки. При изучении протеинов (растительныхбелков) используют метод извлечения их фракций по растворимости (альбумины, глобулины, проламины и глютелины), и предложенный американским исследователем Осборном.
Альбумины растворяются в воде, их можно выделить из раствора в виде сгустка денатурированного белка при кипячении. Из водных растворов альбумины осаждают также высаливанием при насыщении солями (сульфатом; аммония и др.). Альбуминный комплекс зерна в основном состоит из ферментов,
Глобулины растворяются в водных растворах различных солей (применяют обычно 5... 10%-ный раствор NaCl). В чистой воде они нерастворимы. Для выделения глобулина из солевого раствора применяют диализ с помощью полупроницаемых мембран или разбавляют большим количеством воды. Глобулины составляют большую часть семян бобовых культур. Проламины — наиболее характерные белки для зерна большинства злаковых культур. Они растворяются в 60...80%-ном растворе этанола. К проламинам относят глиадин из зерна пшеницы и ржи (составная часть клейковины), гордеин — ячменя, зеин — кукурузы, авенин — овса.
Глютелины растворяются в растворах щелочей (0,1...0,2%). Они мало изучены, так как их трудно выделить в чистом виде. Наиболее изучены глютелин зерна пшеницы (составная часть клейковины), оризенин риса и глютелин кукурузы. Разделение протеинов по растворимости носит условный характер.
Современными методами установлена гетерогенность каждой из названных белковых фракций. Каждая из них состоит из нескольких, во многих случаях из многих десятков различных белков, имеющих некоторые общие свойства.
Протеиды (сложные белки). Так называют вещества, состоящие из белка и соединения небелковой природы — простетической группы. По химической природе такие соединения подразделяют на липопротеиды, хромопротеиды, гликопротеиды и нуклеопротеиды.
Липопротеиды, кроме белка, содержат липиды. Липопротеиды в большом количестве входят в состав пластид растительной клетки, (хлоропласты), содержатся в протоплазме, особенно в мембранах. Хромопротеиды — разнообразная группа, в которую входит гемоглобин крови. В гемоглобине белок глобин связан со сложным азотистым соединением, содержащим железо. Это соединение является простетической группой и называется гемом. Гликопротеиды играют важную роль в построении протоплазмы. Они содержат различные углеводы.
Нуклеопротеиды имеют огромное значение в наследственности. Высоко содержание нуклеопротеидов в зародыше зерна. В нуклеопротеидах белок, связан с нуклеиновыми кислотами. Нуклеиновые кислоты наряду с белками относят к. наиболее важным биополимерам, образующим протоплазму живой клетки. Нуклеиновые кислоты представляют собой высокомолекулярные органические, кислоты, растворяющиеся в щелочных растворах и осаждающиеся при подкислении.
При гидролизе нуклеиновые кислоты распадаются на пуриновые основания, пиримидиновые основания, сахара, и, фосфорную кислоту. В состав нуклеиновых кислот входят пуриновые основания аденин и гуанин.
| 13 При гидролизе любых белков всегда встречаются только 20 аминокислот, хотя общее их количество выделенных из различных объектов живой природы перевалило за сотню. По определению аминокислоты содержит – СО2Н карбоксильную и - NH2 аминогруппу. В зависимости от того, на сколько аминогруппа удалена от карбоксильной, аминокислоты обозначают a-, b-,g- и т.д. (по буквам греческого алфавита)
 
 Те 20 аминокислот, о которых упоминалось, относятся к a- аминокислотам и имеют общую формулу
Те 20 аминокислот, о которых упоминалось, относятся к a- аминокислотам и имеют общую формулу
 Где литерой R обозначен заместитель у a- углеродного атома (их называют боковыми радикалами).
Кроме того, что аминокислоты играют роль «строительных блоков» (первичных метаболитов) в построение белков и пептидов, они несут и другие важные функции: боковые радикалы придают участкам белков гигрофильные или гидрофильные свойства, обеспечивают «сшивки» между белковыми молекулами и внутри них, играют роль депо резервного азота в растениях и т.д.
Глицин
Где литерой R обозначен заместитель у a- углеродного атома (их называют боковыми радикалами).
Кроме того, что аминокислоты играют роль «строительных блоков» (первичных метаболитов) в построение белков и пептидов, они несут и другие важные функции: боковые радикалы придают участкам белков гигрофильные или гидрофильные свойства, обеспечивают «сшивки» между белковыми молекулами и внутри них, играют роль депо резервного азота в растениях и т.д.
Глицин  ГИДРОФОБНЫЕ
Аланин
ГИДРОФОБНЫЕ
Аланин  Валин Валин  Лейцин Лейцин 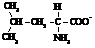 Изолейцин
Изолейцин  Пролин Пролин  Триптофан
Триптофан  Фенилаланин Фенилаланин  Метионин
Метионин  ГИДРОФИЛЬНЫЕ
Серин
ГИДРОФИЛЬНЫЕ
Серин  Треонин Треонин  Аспарагин
Аспарагин  Глутамин Глутамин  Лизин
Лизин  Aргинин Aргинин  Гистидин
Гистидин  Аспарагиновая кислота Аспарагиновая кислота  Глутаминовая кислота
Глутаминовая кислота  Цистеин Цистеин  Тирозин
Тирозин 
|
13.1 Общий азот – весь азот содержащийся в исследуемом объекте и всех его формах. Общий азот делят на белковый и небелковый(аминный, амидный, аммиачный, минеральный). Амидный азот – азот который входит в аминокислоты в виде амидной группы.  Аминный азот – азот аминокислот. Аминный азот – азот аминокислот.  Аммиачный азот – азот находящийся в форме солей орг. кис-т. Минеральный азот – относят соли азотной кислоты или нитраты. Аммиачный азот – азот находящийся в форме солей орг. кис-т. Минеральный азот – относят соли азотной кислоты или нитраты.
| 14 При гидролизе любых белков всегда встречаются только 20 аминокислот, хотя общее их количество выделенных из различных объектов живой природы перевалило за сотню. По определению аминокислоты содержит – СО2Н карбоксильную и - NH2 аминогруппу. В зависимости от того, на сколько аминогруппа удалена от карбоксильной, аминокислоты обозначают a-, b-,g- и т.д. (по буквам греческого алфавита)
 
 Те 20 аминокислот, о которых упоминалось, относятся к a- аминокислотам и имеют общую формулу
Те 20 аминокислот, о которых упоминалось, относятся к a- аминокислотам и имеют общую формулу
 Где литерой R обозначен заместитель у a- углеродного атома (их называют боковыми радикалами).
Кроме того, что аминокислоты играют роль «строительных блоков» (первичных метаболитов) в построение белков и пептидов, они несут и другие важные функции: боковые радикалы придают участкам белков гигрофильные или гидрофильные свойства, обеспечивают «сшивки» между белковыми молекулами и внутри них, играют роль депо резервного азота в растениях и т.д.
Глицин
Где литерой R обозначен заместитель у a- углеродного атома (их называют боковыми радикалами).
Кроме того, что аминокислоты играют роль «строительных блоков» (первичных метаболитов) в построение белков и пептидов, они несут и другие важные функции: боковые радикалы придают участкам белков гигрофильные или гидрофильные свойства, обеспечивают «сшивки» между белковыми молекулами и внутри них, играют роль депо резервного азота в растениях и т.д.
Глицин  ГИДРОФОБНЫЕ
Аланин
ГИДРОФОБНЫЕ
Аланин  Валин Валин  Лейцин Лейцин 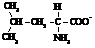 Изолейцин
Изолейцин  Пролин Пролин  Триптофан
Триптофан  Фенилаланин Фенилаланин  Метионин
Метионин  ГИДРОФИЛЬНЫЕ
Серин
ГИДРОФИЛЬНЫЕ
Серин  Треонин Треонин  Аспарагин
Аспарагин  Глутамин Глутамин  Лизин
Лизин  Aргинин Aргинин  Гистидин
Гистидин  Аспарагиновая кислота Аспарагиновая кислота  Глутаминовая кислота
Глутаминовая кислота  Цистеин Цистеин  Тирозин
Тирозин 
|
14.1 Аминокислоты способны переходить в высшие спирты.

| 15 Органические кислоты – соединения содержащие карбоксильную группу соед-ю с алкильной и арильной группой. Номенклатура: Муравьиная НСООН, уксусная СН3СООН, пропионовая СН3СН2СООН, масляная СН3(СН2)2СООН, валериановая СН3(СН2)3СООН, капроновая С6Н12О2; энантовая С7Н14О2; каприловая С8Н16О2; пеларгоновая С9Н18О2; каприновая С10Н20О2; ундециловая С11Н22О2; лауриновая С12Н24О2; тридециловая С13Н26О2; меристиновая С14Н28О2; пентадециловая С15Н30О2; пальметиновая С16Н32О2; маргариновая С17Н34О2; стеариновая С18Н36О2. Летучие кислоты –органические кислоты (муравьиная, уксусная и.т.д) среди них в винах преобладают уксусная, остальные в виде примесей. Общее количество кислот в здоровых винах не должно превышать 2 г\л. Общая кислотность –общее содержание кислот в винах, включая летучую, титруемую, активную. |
16 Органические кислоты – соединения содержащие карбоксильную группу соед-ю с алкильной и арильной группой. Номенклатура: щавелевая НООС–СООН, малоновая НООС–СН2–СООН, янтарная НООС–(СН2)2–СООН, глутаровая НООС–(СН2)3–СООН, адепиновая НООС–(СН2)4–СООН. Кислотность вин определяют следующие оксикислоты – винная, яблочная, лимонная, глюконовая. Единицы измерения данных кислот в вине г/л, кислотность в винах из винограда производят пересчёт на винную, в п\я на яблочную либо лимонную.
    Это производят, так как кислот в винах достаточно много, но содержатся в небольших количествах, они оказывают влияние на кислотность. Поэтому для упрощения пересчитывают на преобладающую кислоту.
Это производят, так как кислот в винах достаточно много, но содержатся в небольших количествах, они оказывают влияние на кислотность. Поэтому для упрощения пересчитывают на преобладающую кислоту.
| 17 При гидролизе любых белков всегда встречаются только 20 аминокислот, хотя общее их количество выделенных из различных объектов живой природы перевалило за сотню. По определению аминокислоты содержит – СО2Н карбоксильную и - NH2 аминогруппу. В зависимости от того, на сколько аминогруппа удалена от карбоксильной, аминокислоты обозначают a-, b-,g- и т.д. (по буквам греческого алфавита)
 
 Те 20 аминокислот, о которых упоминалось, относятся к a- аминокислотам и имеют общую формулу
Те 20 аминокислот, о которых упоминалось, относятся к a- аминокислотам и имеют общую формулу
 Где литерой R обозначен заместитель у a- углеродного атома (их называют боковыми радикалами).
Кроме того, что аминокислоты играют роль «строительных блоков» (первичных метаболитов) в построение белков и пептидов, они несут и другие важные функции: боковые радикалы придают участкам белков гигрофильные или гидрофильные свойства, обеспечивают «сшивки» между белковыми молекулами и внутри них, играют роль депо резервного азота в растениях и т.д.
Глицин
Где литерой R обозначен заместитель у a- углеродного атома (их называют боковыми радикалами).
Кроме того, что аминокислоты играют роль «строительных блоков» (первичных метаболитов) в построение белков и пептидов, они несут и другие важные функции: боковые радикалы придают участкам белков гигрофильные или гидрофильные свойства, обеспечивают «сшивки» между белковыми молекулами и внутри них, играют роль депо резервного азота в растениях и т.д.
Глицин  ГИДРОФОБНЫЕ
Аланин
ГИДРОФОБНЫЕ
Аланин  Валин Валин  Лейцин Лейцин 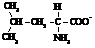 Изолейцин
Изолейцин  Пролин Пролин  Триптофан
Триптофан  Фенилаланин Фенилаланин  Метионин
Метионин 
|
17. 1 ГИДРОФИЛЬНЫЕ
Серин  Треонин Треонин  Аспарагин
Аспарагин  Глутамин Глутамин  Лизин
Лизин  Aргинин Aргинин  Гистидин
Гистидин  Аспарагиновая кислота Аспарагиновая кислота  Глутаминовая кислота
Глутаминовая кислота  Цистеин Цистеин  Тирозин
Тирозин  Аминокислоты способны переходить в высшие спирты.
Аминокислоты способны переходить в высшие спирты.

| 18 Роль хмеля в производстве пива. Для пивоварения наибольший интерес и ценность представляют горькие вещества хмеля, хмелевое масло, дубильные вещества. Горькие вещества предают пиву горечь, обладают антисептическими свойствами. Присутствующие в хмеле полифенолы, эфирные масла, хмелевые смолы участвуют в формировании вкуса и качества пива. Полифенолы в комплексе с горькими веществами способствуют пеностойкости.
В хмеле так же, как и в ячмене, при хранении протекает ряд химических изменений. Под действием кислорода воздуха гумулон превращается в мягкую α-смолу. В присутствии воды и при повышении температуры процесс осмоления протекает с большей скоростью. По отношению к кислороду лупулон менее устойчив, чем гумулон. Под влиянием кислорода он превращается в β-смолу, которая обладает большей растворимостью.
Вследствие сильной окисляемости лупулона значительная часть его при хранении изменяется. В первой стадии окисления гумулона и лупулона происходит образование мягких α- и β-смол. Содержание мягких смол в хмеле при хранении постепенно возрастает. Ценным свойством мягких смол является их антисептическое действие. Они подавляют жизнедеятельность молочно- и маслянокислых бактерий. На дрожжи мягкие смолы никакого действия не оказывают.
При хранении хмеля в нем происходит накопление твердых смол в результате изменения мягких смол и горьких кислот. Компонент хмелевого масла гумулен при хранении окисляется и переходит в диметилянтарную кислоту, другой компонент мирцен также может окисляться и переходить в янтарную кислоту, а валерол превращается в валериановую кислоту.
Мягкая смола, образующаяся при кипячении сусла из гумулона:
 состоит преимущественно из изогумулона. Изогумулон является более сильной кислотой, чем гумулон, и этим объясняется его более высокая растворимость в сусле и пиве. Если при достаточном введении хмеля раствор становится насыщенным горькими кислотами и рН его снижается, то часть растворившихся горьких кислот снова выпадает в осадок. Выделение их происходит в коллоидной форме.
При хранении хмеля даже в благоприятных условиях его качество постепенно ухудшается. Кроме того, охмеление шишковым хмелем экономически неэффективно, так как при этом теряется 70-80% горьких веществ. В последнее время широко используют продукты переработки хмеля, позволяющие повысить степень использования горьких веществ, стойкость ценных компонентов в процессе хранения хмельных препаратов, сократить расходы на хранение и транспортирование, упростить способ применения и, наконец, улучшить стабильность и качество охмеления сусла и пива.
Продуктами переработки хмеля — хмелепродуктами — являются молотый брикетированный хмель, гранулированный хмель, хмелевые экстракты (неизомеризованные и изомеризован-ные), комбинированные препараты хмеля.
состоит преимущественно из изогумулона. Изогумулон является более сильной кислотой, чем гумулон, и этим объясняется его более высокая растворимость в сусле и пиве. Если при достаточном введении хмеля раствор становится насыщенным горькими кислотами и рН его снижается, то часть растворившихся горьких кислот снова выпадает в осадок. Выделение их происходит в коллоидной форме.
При хранении хмеля даже в благоприятных условиях его качество постепенно ухудшается. Кроме того, охмеление шишковым хмелем экономически неэффективно, так как при этом теряется 70-80% горьких веществ. В последнее время широко используют продукты переработки хмеля, позволяющие повысить степень использования горьких веществ, стойкость ценных компонентов в процессе хранения хмельных препаратов, сократить расходы на хранение и транспортирование, упростить способ применения и, наконец, улучшить стабильность и качество охмеления сусла и пива.
Продуктами переработки хмеля — хмелепродуктами — являются молотый брикетированный хмель, гранулированный хмель, хмелевые экстракты (неизомеризованные и изомеризован-ные), комбинированные препараты хмеля.
|
 2018-01-21
2018-01-21 1935
1935






