При решении многих практических вопросов необходимо знать количество воздуха, расходуемого на горение единицы массы или объѐма горючего вещества, количество образовавшихся продуктов горения и их процентный состав. Рассмотрим расчѐтные методы определения отдельных составляющих материального баланса процессов горения.
Методика расчѐта объѐма воздуха для горения зависит от состава горючего вещества, его агрегатного состояния и условий горения. По своей природе горючие вещества могут быть индивидуальными химическими соединениями и смесями сложных химических соединений. К индивидуальным химическим соединениям относятся такие вещества, которые имеют постоянное химическое строение и постоянную химическую формулу, например, бензол (С6Н6), пропанол (С3Н7ОН), уксусная кислота (СН3СООН) и др. Смеси сложных химических соединений – вещества, не имеющие определѐнного химического строения, и их состав одной химической формулой выразить нельзя. К этой группе веществ относятся уголь, нефть, древесина, жиры и др. Состав этих веществ выражается в процентном содержании отдельных элементов или газов (C, S, H, и др. или СО, СН4, Н2S и др.).
Различают объѐм воздуха, теоретически необходимый для горения
(V Втеор), и объѐм воздуха, действительно (практически) израсходованный на горение (V Вдейств). При этом
| V действ | V теор . | (2) |
| В | В |

Множитель  называется коэффициентом избытка воздуха. Коэффициент избытка воздуха показывает, во сколько раз объѐм воздуха, поступивший на горение, больше теоретического объѐма воздуха, необходимого для полного сгорания единицы количества вещества в стехиометрической смеси.
называется коэффициентом избытка воздуха. Коэффициент избытка воздуха показывает, во сколько раз объѐм воздуха, поступивший на горение, больше теоретического объѐма воздуха, необходимого для полного сгорания единицы количества вещества в стехиометрической смеси.
Разность между действительным и теоретически необходимым

| количеством воздуха называется избытком воздуха ( | V В). | ||
| V | V действ | V теор . | (3) |
| В | В | В |

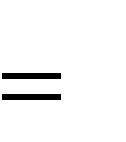

Объѐм продуктов горения, образовавшихся при сжигании единицы горючего (1 кг, 1 м3, 1 кмоль) в теоретическом количестве воздуха, равен сумме объѐмов углекислого газа, паров воды и азота:
| V | теор | V | V | V | теор . | (4) |
| ПГ | CO2 | H 2O | N 2 |



Полный, действительный объѐм продуктов горения рассчитывается с учѐтом избытка воздуха:
| V | действ | V | теор | V | V | теор | ( | 1) V теор. | (5) |
| ПГ | ПГ | В | ПГ | В |



Для удобства расчѐтов горючие вещества разделяют на следующие группы (табл. 16): индивидуальные химические соединения (в газообразном и конденсированном состоянии); вещества сложного состава (древесина, торф, нефть и т. п.); смесь газов (генераторный, попутный газы и т. п.).
Таблица 16
Расчѐтные формулы для определения теоретического количества воздуха,
необходимого для сгорания веществ
| Группа горючих веществ | Расчѐтные формулы | Размер- | |||||||||||||||||
| ность | |||||||||||||||||||
| Индивидуальное горючее | теор | n O 2 | n N 2 | ||||||||||||||||
| вещество в газообразном | V В | (6) | м3/м3 | ||||||||||||||||
| n ГВ | |||||||||||||||||||
| состоянии | |||||||||||||||||||
| Индивидуальное горючее | (n O 2 | n N 2 ) Vt | |||||||||||||||||
| вещество в | V теор | (7) | |||||||||||||||||
| конденсированном | В | n ГВ | М ГВ | м /кг | |||||||||||||||
| состоянии | |||||||||||||||||||
| теор | β | i | О 2 | (8) | |||||||||||||||
| Смесь газов | V В | м3/м3 | |||||||||||||||||
| Вещество сложного | С | S | O | ||||||||||||||||
| состава в | V теор | 0,269 | Н | (9) | |||||||||||||||
| конденсированном | В | м /кг | |||||||||||||||||
| состоянии | |||||||||||||||||||
| Примечание: | |||||||||||||||||||
| n ГВ, n O 2, n N 2-количество | горючего, | кислорода | и | азота, | получаемые из |








уравнения реакции горения, кмоль/кмоль; М ГВ–молекулярная масса горючего вещества;
Vt –молярный объѐм газа при заданных условиях,м3/кмоль;
C, H, S, O – весовое содержание соответствующих элементов в составе горючего вещества, % масс.;

β i  i –сумма произведений стехиометрического коэффициента реакций
i –сумма произведений стехиометрического коэффициента реакций

горения каждого компонента горючей смеси (i) на процентное содержание этого компонента (i) в смеси;


О2 – процентное содержание кислорода в сложном горючем газе.
Для газообразных горючих веществ расчѐт объѐмов воздуха и продуктов горения проводят в м3/м3. Так как 1 кмоль любого газа в одинаковых условиях занимает один и тот же объѐм (при нормальных условиях 22,4 м3), то объѐм, рассчитанный в м3/м3, численно будет таким же, как и в кмоль/кмоль.
Если горючее вещество находится в конденсированном состоянии (жидком или твѐрдом), то, как правило, расчѐты объѐмов воздуха и продуктов горения проводят в м3/кг.
Для определения объѐма воздуха при горении в условиях, отличных от нормальных, пользуются объединѐнным газовым законом:


| P | V | P | V | ||||
| , | (10) | ||||||
| T 0 | T 1 |
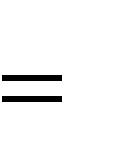
где Р 0 – нормальное давление, Па;
Т 0–нормальная температура,К;
V 0–объѐм воздуха при нормальных условиях(м3или м3/кмоль);
P 1, T 1, V 1–соответственно давление,объѐм и температура воздуха,характеризующие заданные условия горения.
Иногда на практике приходится решать обратную задачу – по известному процентному содержанию кислорода в продуктах горения находить коэффициент избытка воздуха:
| О 2 | V ПГ | теор | |||||||
| α | . | (11) | |||||||
| теор | |||||||||
| V | (21 | О 2 | ) | ||||||
| В |




Для веществ, у которых объѐм продуктов горения равен объѐму израсходованного воздуха (например горение углерода, серы), эта формула упрощается:

α. (12)
21 О 2
При расчѐте объѐма продуктов горения пользуются формулами, приведѐнными в табл. 17.
Таблица 17
Расчѐтные формулы для определения теоретического объѐма продуктов горения
| Группа горючих | Раз- | ||||||||||||||||||||||||||||||||
| Расчѐтные формулы | мер- | ||||||||||||||||||||||||||||||||
| веществ | |||||||||||||||||||||||||||||||||
| ность | |||||||||||||||||||||||||||||||||
| Индивидуальное | |||||||||||||||||||||||||||||||||
| горючее | теор | n ПГ | (13) | ||||||||||||||||||||||||||||||
| вещество в | V ПГ | ||||||||||||||||||||||||||||||||
| газообразном | n ГВ | м /м | |||||||||||||||||||||||||||||||
| состоянии | |||||||||||||||||||||||||||||||||
| Индивидуальное | |||||||||||||||||||||||||||||||||
| горючее | теор | n ПГ | Vt | (14) | |||||||||||||||||||||||||||||
| вещество в | V ПГ | ||||||||||||||||||||||||||||||||
| конденсирован- | n ГВ М | ГВ | м /кг | ||||||||||||||||||||||||||||||
| ном состоянии | |||||||||||||||||||||||||||||||||
| теор | n ПГ i | ГВ i | НЕГОР | (15) | |||||||||||||||||||||||||||||
| Смесь газов | V ПГ | м3/м3 | |||||||||||||||||||||||||||||||
| n ГВ i 100 | |||||||||||||||||||||||||||||||||
| Вещество | теор | С | Н | W | S | ||||||||||||||||||||||||||||
| сложного | V ПГ | 1,86 | (11,2 | 1,24 | ) | 0,7 | |||||||||||||||||||||||||||
| 100 (16) | |||||||||||||||||||||||||||||||||
| состава в | |||||||||||||||||||||||||||||||||
| O | |||||||||||||||||||||||||||||||||
| конденсирован- | 7C 21(H | ) | 2,63S | 0,8N | НЕГОР | м /кг | |||||||||||||||||||||||||||
| ном состоянии | |||||||||||||||||||||||||||||||||

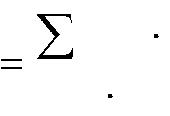



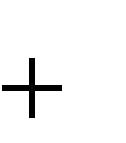




Расчѐт объѐма продуктов горения (СО2, Н2О, SO2, N2) при горении веществ сложного состава проводится по следующим формулам:
| V | 1,86 | С | ; | (17) | |||||||
| CO 2 | |||||||||||
| V | 11,2 | Н | 1,24 | W | ; | (18) | |||||
| H 2O |







| V N | 7 C | 21 (H | O | ) 2,6 S 0,8 N; | (19) | ||||||
| V | 0,7 | S | . | (20) | |||||||
| SO 2 | |||||||||||










Процентный состав продуктов горения рассчитывается исходя из количества молей продуктов горения. Например, процентное содержание паров воды в продуктах горения составит, %

| n Н | О 100 | ||||
| %Н2О | . | (21) | |||
| n ПГ |

Если горение протекает с избытком воздуха, то при расчѐте количества молей продуктов горения учитывается избыточное число молей кислорода и азота (n O2 и n N 2), %



| %Н 2О | n Н | О 100 | |||||
| , | (22) | ||||||
| n ПГ | n O 2 | ||||||
| n N 2 | |||||||
| где | n O 2 | n O 2 | (α 1), | (23) | |||
| n N 2 | n N 2 | ( | 1). | (24) |




Рассмотрим примеры решения задач на расчѐт объѐма воздуха, объѐма и состава продуктов горения.
ПРИМЕР: Сгорает4м3пропана (С3Н8). Рассчитать теоретические объѐмывоздуха, объѐм и состав (в объѐмных %) продуктов горения. Условия нормальные.
Решение.
Сгорает индивидуальное горючее вещество, находящееся в газообразном состоянии.
1. Запишем уравнение реакции горения пропана в воздухе:


С3Н8 + 5 (О2 + 3,76N2) = 3 CО2 + 4 Н2О + 3,76 5 N2.
2. Рассчитаем теоретические объѐмы воздуха и продуктов горения по формулам (6) и (13) в расчѐте на 1 м3 горючего вещества:


| V теор | 5 (1 | 3,76) | 23,8 (м3/м3); | ||||
| в | |||||||
| V | теор | 4 5 3,76 | 25,8 (м3/м3). | ||||
| ПГ | |||||||

3. Учитывая, что сгорает не 1 м3 газа, а 4 м3, находим действительные объѐмы воздуха и продуктов горения:
V В23,8  4 95,2 (м3);
4 95,2 (м3);


V ПГ 25,8  4 103,2 (м3).
4 103,2 (м3).


4. Рассчитаем состав продуктов горения, %

| %СО 2 | n CO 2 100 | 3 100 | 11,6 | ; | |||||||||||||||
| n CO 2 | n H 2O | n N 2 | 4 5 3,76 | ||||||||||||||||
| n Н О100 | 4 100 | 15,5; | |||||||||||||||||
| %Н 2 | О | ||||||||||||||||||
| n CO | n H O | n N | 5 3,76 | ||||||||||||||||
| %N 2 | n N2100 | 3,76 | 5 100 | 72,9. | |||||||||||||||
| n CO | n H O | n N | 5 3,76 | ||||||||||||||||



Ответ: на сгорание4м3пропана необходимо95,2м3воздуха,при этомобразуется 103,2 м3 продуктов горения, из которых СО2 – 11,6 %, Н2О – 15,5 %, N2 – 72,9 %.
ПРИМЕР: Сгорает100кг ацетона.Рассчитать действительные объѐмывоздуха и продуктов горения и процентное содержание углекислого газа (СО2), если коэффициент избытка воздуха равен 2. Условия нормальные.
Решение.
Сгорает индивидуальное химическое соединение в конденсированном состоянии.
1. Составляем уравнение реакции горения ацетона в воздухе:
С3Н6О + 4(О2 + 3,76 N2) = 3 CО2 + 3 Н2О + 4 3,76 N2.

2. Объѐм воздуха, необходимый для сгорания 1 кг ацетона, рассчитываем по формуле (7), учитывая при этом, что масса одного киломоля ацетона составляет 58 кг/кмоль:


| V В | теор (n O 2 | n N 2 ) Vt | (4 4 3,76)22,4 | 7,4 | ||||
| (м /кг). | ||||||||
| n ГВ | М ГВ | 1 58 | ||||||




3. Действительный объѐм воздуха, пошедшего на сгорание 1 кг ацетона,

рассчитывается с учѐтом коэффициента избытка воздуха:
V Вдейств α  V Втеор 2
V Втеор 2  7,4 14,8 (м3/кг).
7,4 14,8 (м3/кг).
4. Избыток воздуха составит:
V В V Вдейств V Втеор 14,8 7,4 7,4 (м3/кг).



5. Теоретический объѐм продуктов горения рассчитываем по формуле
(14):



| теор | n ПГ Vt | (3 3 4 3,76) 22,4 | ||||
| V ПГ | 8,1 | (м /кг). | ||||
| n ГВ М ГВ | 1 58 | |||||

6. Действительный объѐм продуктов горения составит:
V ПГдейств V Втеор  V В8,1 7,4 15,5(м3/кг).
V В8,1 7,4 15,5(м3/кг).


7. Объѐм воздуха, теоретически необходимого для сгорания 100 кг ацетона, составит соответственно 740 м3 (7,4  100), при этом выделится 1 550 м3 продуктов сгорания.
100), при этом выделится 1 550 м3 продуктов сгорания.
8. Процентное содержание углекислого газа рассчитывается по
формуле, %

| %СО 2 | n СО 2 100 | 3 100 | 7,48 % | |||||
| n ПГ | n O | n N | 3 3 4 3,76 4(2 1) 4 3,76(2 1) | |||||


Ответ: При сгорании100кг ацетона объѐм воздуха при нормальных условияхсоставит 1480 м3, а объѐм продуктов горения – 1550 м3, процентное содержание углекислого газа в продуктах горения составило 7,48 %.
Примечание. Если в процессе горения были заданы условия,отличные отнормальных (Т 273 К, Р 101,3 кПа), то объѐм продуктов горения и воздуха рассчитывается с учѐтом объѐма, который занимает один кмоль газа при заданной температуре:


| Vt | 22,4 | P 0 | T | ||
| , | (25) | ||||
| T 0 | P | ||||
 2017-10-25
2017-10-25 1511
1511
